DNS molekula, struktūras pazīmes un funkcijas. DNS struktūra: pazīmes, shēma
Pirmie pierādījumi par DNS kā organismu iedzimtās informācijas nesēja lomu piesaistīja lielu uzmanību nukleīnskābju izpētei. 1869. gadā F. Mišers no šūnu kodoliem izdalīja īpašu vielu, ko nosauca par nukleīnu. Pēc 20 gadiem šis nosaukums tika aizstāts ar terminu nukleīnskābe. 1924. gadā R. Felgens izstrādāja metodi nukleīnskābju citoloģiskai atpazīšanai ar to specifisko iekrāsošanu un parādīja, ka DNS ir lokalizēta šūnu kodolos, bet RNS – citoplazmā. 1936. gadā A.N. Belozerskis un I.I. Dubrovskaja izolēja tīru DNS no augu šūnu kodoliem. Līdz 30. gadu sākumam. tika noskaidroti nukleīnskābju cukuru uzbūves ķīmiskie pamatprincipi, un 1953. gadā tika izveidots DNS strukturālais modelis.
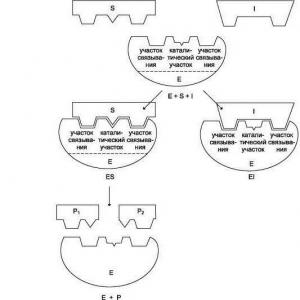
Nukleīnskābju galvenā struktūrvienība ir nukleotīds, kas sastāv no trim ķīmiski atšķirīgām daļām, kas savienotas ar kovalentām saitēm (5.2. att.).
Rīsi. 5.2. Strukturālās formulas: a- nukleotīdi; b- DNS; v - RNS (sk. arī 110. lpp.)

Rīsi. 5.2. Beigas. Strukturālās formulas: a- nukleotīdi; 6 - DNS; v- RNS
Pirmā daļa ir cukurs, kas satur piecus oglekļa atomus: dezoksiriboze DNS un riboze RNS sastāvā.
Otrā nukleotīda daļa - purīna vai pirimidīna slāpekļa bāze, kovalenti piesaistīta cukura pirmajam oglekļa atomam, veido struktūru, t.s. nukleozīds. DNS satur purīna bāzes - adenīns(A) un guanīns(D) - un pirimidīna bāzes - timīns(T) un citozīns(C). Attiecīgos nukleozīdus sauc par deoksiadenozīnu, deoksiguanozīnu, deoksitimidīnu un deoksicitidīnu. RNS satur tādas pašas purīna bāzes kā DNS, pirimidīna bāze citozīns, un timīna vietā tas satur uracils(U); atbilstošos nukleozīdus sauc par adenozīnu, guanozīnu, uridīnu un citidīnu.
Trešā nukleotīda daļa ir fosfātu grupa, kas savieno blakus esošos nukleozīdus polimēra ķēdē caur fosfodiestera saitēm starp viena cukura 5-oglekļa atomu un cita cukura 3" oglekļa atomu (5.2. att., b, v). Nukleotīdi sauc par nukleozīdiem ar vienu vai vairākām fosfātu grupām, kas ar estersaitēm pievienotas cukura 3" vai 5 oglekļa atomiem. Nukleotīdu sintēze notiek attiecīgi pirms nukleīnskābju sintēzes, nukleotīdi ir nukleīnskābju ķīmiskās vai fermentatīvās hidrolīzes produkti.
Nukleīnskābes ir ļoti garas polimēru ķēdes, kas sastāv no mononukleotīdiem, kas savienoti ar 5- un 3'-fosfodiestera saitēm. Neskarta DNS molekula satur, atkarībā no organisma veida, no vairākiem tūkstošiem līdz daudziem miljoniem nukleotīdu, neskarta RNS molekula – no 100 līdz 100 tūkstošiem vai vairāk nukleotīdu.
E. Šargafa dažādu sugu DNS nukleotīdu sastāva analīžu rezultāti parādīja, ka dažādu slāpekļa bāzu - adenīna, guanīna, timīna, citozīna - molekulārā attiecība ir ļoti atšķirīga. Līdz ar to tika pierādīts, ka DNS nebūt nav monotons polimērs, kas sastāv no identiskiem tetranukleotīdiem, kā tika pieņemts pagājušā gadsimta 40. gados. XX gadsimtiem, un ka tai pilnībā piemīt sarežģītība, kas nepieciešama iedzimtas informācijas saglabāšanai un pārsūtīšanai noteiktas nukleotīdu bāzes secības veidā.
E. Šargafa pētījumi atklāja arī pazīmi, kas raksturīga visām DNS molekulām: adenīna molārais saturs ir vienāds ar timīna saturu, bet guanīna molārais saturs ir vienāds ar citozīna saturu. Šīs vienādības sauc par Chargaff ekvivalences likumu: [A] = [T], [G] = [C]; purīnu skaits ir vienāds ar pirimidīnu skaitu. Atkarībā no sugas mainās tikai attiecība ([A] + [T]) / ([G] + [C]) (5.1. tabula).
|
Pamatu sastāvs |
Attieksme |
Asimetrija |
|||||
|
pamatojums |
|||||||
|
(A+T)/(G+C) |
|||||||
|
Dzīvnieki |
|||||||
|
Bruņurupucis |
|||||||
|
jūras krabis |
|||||||
|
Jūras ezis |
|||||||
|
Augi, sēnes |
|||||||
|
kviešu dīgļi |
|||||||
|
Sēne Aspergillus niger |
|||||||
|
baktērijas |
|||||||
|
Escherichia coli |
|||||||
|
Staphylococcus aureus |
|||||||
|
Clostridium perfringens |
|||||||
|
Brucela abortus |
|||||||
|
Sarcina lutea |
|||||||
|
bakteriofāgi |
|||||||
|
FH 174 (vīrusu forma) |
|||||||
|
FH 174 (replikācijas forma) |
|||||||
Bāzes koeficientu sauc nukleotīds(konkrēts) specifika. Chargaff atklājumā tika formulēta svarīga DNS strukturālā iezīme, kas vēlāk tika atspoguļota J. Watson un F. Crick (1953) DNS strukturālajā modelī, kas faktiski parādīja, ka Chargaff noteikumi neuzliek nekādus ierobežojumus iespējamajam skaitam. dažādu bāzes secību kombinācijas, kas var veidot DNS molekulas.
Nostāja par nukleotīdu specifiku veidoja pamatu jaunai bioloģijas nozarei - gēnu sistemātika, kas darbojas, salīdzinot nukleīnskābju sastāvu un struktūru, lai izveidotu dabisku organismu sistēmu.
Saskaņā ar Vatsona-Krika modeli DNS molekula sastāv no divām polinukleotīdu ķēdēm (virknēm, pavedieniem), kas savienotas viena ar otru ar šķērsvirziena ūdeņraža saitēm starp slāpekļa bāzēm saskaņā ar komplementāro principu (vienas ķēdes adenīns ir savienots ar divām ūdeņraža saitēm ar timīnu pretējās ķēdes, un dažādu ķēžu guanīns un citozīns ir savienoti viens ar otru ar trim ūdeņraža saitēm). Šajā gadījumā vienas molekulas divas Polinukleotīdu ķēdes ir pretparalēlas, t.i., pretī 3 "vienas ķēdes gals ir otras ķēdes 5" gals un otrādi (5.3. att.). Tomēr jāpatur prātā pašreizējie dati, ka dažu vīrusu ģenētisko materiālu attēlo vienpavedienu (vienpavedienu) DNS molekulas. Pamatojoties uz DNS rentgenstaru difrakcijas analīzes datiem, J. Vatsons un F. Kriks arī secināja, ka tās divpavedienu molekulai ir sekundāra struktūra spirāles veidā, kas savīti virzienā no kreisās puses uz labo, kas vēlāk. kļuva pazīstama kā 5-forma (5.4. att.). Līdz šim ir pierādīts, ka papildus visizplatītākajai 5-formai ir iespējams noteikt DNS segmentus, kuriem ir atšķirīga konfigurācija - kā labo roku (formas A, C), un savīti no labās puses uz kreiso (kreisais, jeb Z-forma) (5.4. att.). Pastāv zināmas atšķirības starp šīm DNS sekundārās struktūras formām (5.2. tabula). Tā, piemēram, attālumu starp diviem blakus esošajiem slāpekļa bāzu pāriem divpavedienu spirālē, kas izteikts nanometros (nm), 5-formai un Z-formai raksturo dažādas vērtības (0,34 un 0,38 nm, attiecīgi). Uz att. 5.5 parāda mūsdienīgus trīsdimensiju DNS "kreiso" un "labo roku" formu modeļus.

Rīsi. 5.3. divpavedienu DNS molekulas fragmenta primārās struktūras shematisks attēlojums: A - adenīns; G - guanīns; T - timīns; C - citozīns

Rīsi. 5.4.

5.2. tabula
Dažādu formu DNS dubultspirāles īpašības
RNS molekulas atkarībā no to strukturālajām un funkcionālajām iezīmēm iedala vairākos veidos: informatīvā (matricas) RNS (mRNS jeb mRNS), ribosomu RNS (rRNS), pārneses RNS (tRNS), mazā kodola RNS (snRNS) utt. Atšķirībā no DNS, RNS molekulas vienmēr ir vienpavedienu (vienpavedienu). Tomēr tie var veidot sarežģītākas (sekundārās) konfigurācijas, jo šādas ķēdes atsevišķas sadaļas ir savstarpēji papildinošas, pamatojoties uz komplementāru slāpekļa bāzu (A-U un G-C) mijiedarbību. Kā piemēru aplūkosim āboliņa lapu konfigurāciju fenilalanīna pārneses RNS molekulai (5.6. att.).

Rīsi. 5.6.
1953. gadā D. Vatsons un F. Kriks ierosināja DNS struktūras modeli, kas balstījās uz šādiem postulātiem:
- 1. DNS ir polimērs, kas sastāv no nukleotīdiem, kas savienoti ar 3"- un 5"-fosfodiestera saitēm.
- 2. DNS nukleotīdu sastāvs atbilst Šargafa noteikumiem.
- 3. DNS molekulai ir dubultspirāles struktūra, kas atgādina spirālveida kāpnes, par ko liecina DNS virkņu rentgena modeļi, kurus pirmo reizi ieguva M. Vilkinss un R. Franklins.
- 4. Polimēra struktūru, kā liecina dabiskās (dabīgās) DNS skābes-bāzes titrēšana, stabilizē ūdeņraža saites. Dabiskās DNS titrēšana un karsēšana izraisa ievērojamas izmaiņas tās fizikālajās īpašībās, jo īpaši viskozitātē, pārvēršot to denaturētā formā, un netiek iznīcinātas kovalentās saites.
Saturs
Šūnu DNS saīsinājums daudziem ir pazīstams no skolas bioloģijas kursa, taču daži var viegli atbildēt, kas tas ir. Tūlīt pēc skolas beigšanas atmiņā paliek tikai neskaidrs priekšstats par iedzimtību un ģenētiku. Zināt, kas ir DNS un kāda ir tās ietekme uz mūsu dzīvi, dažkārt var būt ļoti nepieciešama.
DNS molekula
Bioķīmiķi izšķir trīs veidu makromolekulas: DNS, RNS un olbaltumvielas. Dezoksiribonukleīnskābe ir biopolimērs, kas ir atbildīgs par datu pārraidi par sugas iedzimtajām iezīmēm, īpašībām un attīstību no paaudzes paaudzē. Tās monomērs ir nukleotīds. Kas ir DNS molekulas? Tā ir galvenā hromosomu sastāvdaļa un satur ģenētisko kodu.
DNS struktūra
Iepriekš zinātnieki iztēlojās, ka DNS struktūras modelis ir periodisks, kur atkārtojas vienas un tās pašas nukleotīdu grupas (fosfātu un cukura molekulu kombinācijas). Noteikta nukleotīdu secības kombinācija nodrošina iespēju "kodēt" informāciju. Pateicoties pētījumiem, izrādījās, ka dažādu organismu uzbūve ir atšķirīga.
Amerikāņu zinātnieki Aleksandrs Ričs, Deivids Deiviss un Gerijs Felsenfelds ir īpaši slaveni, pētot jautājumu par to, kas ir DNS. 1957. gadā viņi iepazīstināja ar trīs spirāles nukleīnskābes aprakstu. Pēc 28 gadiem zinātnieks Maksims Davidovičs Franks-Kamenitskis demonstrēja, kā dezoksiribonukleīnskābe, kas sastāv no divām spirālēm, tiek salocīta H-veida formā, kas sastāv no 3 pavedieniem.
Dezoksiribonukleīnskābes struktūra ir divpavedienu. Tajā nukleotīdi ir savienoti pa pāriem, veidojot garas polinukleotīdu ķēdes. Šīs ķēdes, izmantojot ūdeņraža saites, ļauj izveidot dubultspirāli. Izņēmums ir vīrusi, kuriem ir vienpavedienu genoms. Ir lineāra DNS (daži vīrusi, baktērijas) un cirkulāra (mitohondriji, hloroplasti).
DNS sastāvs
Nezinot, no kā sastāv DNS, medicīnā nebūtu nekādu sasniegumu. Katrs nukleotīds sastāv no trim daļām: pentozes cukura atlikuma, slāpekļa bāzes un fosforskābes atlikuma. Pamatojoties uz savienojuma īpašībām, skābes var saukt par dezoksiribonukleīnskābes vai ribonukleīnskābes. DNS satur milzīgu skaitu mononukleotīdu no divām bāzēm: citozīna un timīna. Turklāt tas satur pirimidīna atvasinājumus, adenīnu un guanīnu.
Bioloģijā ir DNS definīcija – junk DNS. Tās funkcija joprojām nav zināma. Alternatīva nosaukuma versija ir "nekodēts", kas nav taisnība, jo tajā ir kodējoši proteīni, transpozoni, taču arī to mērķis ir noslēpums. Viena no darba hipotēzēm liecina, ka noteikts daudzums šīs makromolekulas veicina genoma strukturālo stabilizāciju saistībā ar mutācijām.
Kur ir
Atrašanās vieta šūnā ir atkarīga no sugas īpašībām. Vienšūnu DNS atrodas membrānā. Citās dzīvās būtnēs tas atrodas kodolā, plastidos un mitohondrijās. Ja runājam par cilvēka DNS, tad to sauc par hromosomu. Tiesa, tā nav gluži taisnība, jo hromosomas ir hromatīna un dezoksiribonukleīnskābes komplekss.
Loma būrī
DNS galvenā loma šūnās ir iedzimto gēnu pārnešana un nākamo paaudžu izdzīvošana. No tā ir atkarīgi ne tikai topošā indivīda ārējie dati, bet arī raksturs un veselība. Dezoksiribonukleīnskābe ir superspirālā stāvoklī, bet kvalitatīvam dzīves procesam tai jābūt nesagrieztai. Ar to viņai palīdz enzīmi - topoizomerāzes un helikāzes.
Topoizomerāzes ir nukleāzes, tās spēj mainīt vērpšanas pakāpi. Vēl viena to funkcija ir dalība transkripcijā un replikācijā (šūnu dalīšanās). Helikāzes sarauj ūdeņraža saites starp bāzēm. Ir ligāzes enzīmi, kas “šķērso” sarautās saites, un polimerāzes, kas ir iesaistītas jaunu polinukleotīdu ķēžu sintēzē.

Kā tiek atšifrēta DNS
Šis bioloģijas saīsinājums ir pazīstams. DNS pilns nosaukums ir dezoksiribonukleīnskābe. Ne visi to var pateikt pirmo reizi, tāpēc DNS dekodēšana runā bieži tiek izlaista. Ir arī jēdziens RNS - ribonukleīnskābe, kas sastāv no aminoskābju sekvencēm olbaltumvielās. Tie ir tieši saistīti, un RNS ir otrā svarīgākā makromolekula.
Cilvēka DNS
Cilvēka hromosomas kodolā ir atdalītas, padarot cilvēka DNS par stabilāko, pilnīgāko informācijas nesēju. Ģenētiskās rekombinācijas laikā spirāles tiek atdalītas, notiek vietņu apmaiņa un pēc tam savienojums tiek atjaunots. DNS bojājumu dēļ veidojas jaunas kombinācijas un raksti. Viss mehānisms veicina dabisko atlasi. Joprojām nav zināms, cik ilgi viņa ir atbildīga par genoma nodošanu un kāda ir viņas vielmaiņas evolūcija.
Kas atklāja
Pirmie DNS struktūras atklājumi tiek piedēvēti angļu biologiem Džeimsam Vatsonam un Frensisam Krikam, kuri 1953. gadā atklāja molekulas strukturālās iezīmes. 1869. gadā to atrada Šveices ārsts Frīdrihs Mišers. Viņš pētīja dzīvnieku šūnu ķīmisko sastāvu ar leikocītu palīdzību, kas masveidā uzkrājas strutainos bojājumos.
Mišers pētīja veidus, kā mazgāt leikocītus, izolētus proteīnus, kad atklāja, ka bez tiem ir vēl kaut kas. Apstrādes laikā trauku dibenā izveidojās pārslu nogulsnes. Izpētījis šīs nogulsnes mikroskopā, jaunais ārsts atklāja kodolus, kas palikuši pēc apstrādes ar sālsskābi. Tajā bija savienojums, ko Frīdrihs sauca par nukleīnu (no latīņu valodas nucleus — kodols).
MASKAVA, 25. aprīlis - RIA Novosti, Tatjana Pičugina. Tieši pirms 65 gadiem britu zinātnieki Džeimss Vatsons un Frensiss Kriks publicēja rakstu par DNS struktūras atšifrēšanu, liekot pamatus jaunai zinātnei – molekulārajai bioloģijai. Šis atklājums daudz ko mainīja cilvēces dzīvē. RIA Novosti stāsta par DNS molekulas īpašībām un to, kāpēc tā ir tik svarīga.
19. gadsimta otrajā pusē bioloģija bija ļoti jauna zinātne. Zinātnieki tikai sāka pētīt šūnu, un iedzimtības jēdziens, lai gan to jau formulēja Gregors Mendels, netika plaši pieņemts.
1868. gada pavasarī Tībingenes Universitātē (Vācija) ieradās jauns Šveices ārsts Frīdrihs Mišers, lai veiktu zinātnisku darbu. Viņš bija iecerējis noskaidrot, no kādām vielām šūna sastāv. Eksperimentiem izvēlējos leikocītus, kurus viegli iegūt no strutas.
Atdalot kodolu no protoplazmas, olbaltumvielām un taukiem, Mišers atklāja savienojumu ar augstu fosfora saturu. Viņš šo molekulu sauca par nukleīnu ("kodols" latīņu valodā - kodols).
Šim savienojumam bija skābas īpašības, tāpēc tika izveidots termins "nukleīnskābe". Tās prefikss "dezoksiribo" nozīmē, ka molekula satur H grupas un cukurus. Tad izrādījās, ka patiesībā tā ir sāls, bet nosaukums netika mainīts.
20. gadsimta sākumā zinātnieki jau zināja, ka nukleīns ir polimērs (tas ir, ļoti gara, elastīga atkārtotu vienību molekula), vienības sastāv no četrām slāpekļa bāzēm (adenīna, timīna, guanīna un citozīna) un nukleīns ir ietverts hromosomās - kompaktās struktūrās, kas rodas dalīšanās šūnās. Viņu spēju pārnēsāt iedzimtas iezīmes pierādīja amerikāņu ģenētiķis Tomass Morgans eksperimentos ar Drosophila.
Modelis, kas izskaidro gēnus
Bet ko dezoksiribonukleīnskābe, saīsināti DNS, dara šūnas kodolā, ilgu laiku nebija saprotams. Tika uzskatīts, ka tam ir kāda strukturāla loma hromosomās. Iedzimtības vienības - gēni - tika attiecinātas uz olbaltumvielu dabu. Izrāvienu veica amerikāņu pētnieks Osvalds Eiverijs, kurš eksperimentāli pierādīja, ka ģenētiskais materiāls tiek pārnests no baktērijas uz baktēriju caur DNS.
Kļuva skaidrs, ka DNS ir jāpēta. Bet kā? Tolaik zinātniekiem bija pieejami tikai rentgena stari. Lai spīdētu cauri bioloģiskajām molekulām, tās bija jākristalizē, kas ir grūti. Olbaltumvielu molekulu struktūras atšifrēšana no rentgenstaru modeļiem tika veikta Cavendish laboratorijā (Kembridža, Apvienotā Karaliste). Tur strādājošajiem jaunajiem pētniekiem Džeimsam Vatsonam un Frensisam Krikam nebija savu eksperimentālo datu par DNS, tāpēc viņi izmantoja King's College kolēģu Morisa Vilkinsa un Rozalindas Franklinas rentgenstarus.
Vatsons un Kriks ierosināja DNS struktūras modeli, kas precīzi atbilst rentgenstaru modeļiem: divas paralēlas dzīslas ir savītas labās puses spirālē. Katra ķēde sastāv no patvaļīga slāpekļa bāzu kopuma, kas savērtas uz to cukuru un fosfātu mugurkaula un tiek turētas kopā ar ūdeņraža saitēm, kas izstieptas starp bāzēm. Turklāt adenīns savienojas tikai ar timīnu, bet guanīns - ar citozīnu. Šo noteikumu sauc par komplementaritātes principu.
Vatsona un Krika modelis izskaidroja četras galvenās DNS funkcijas: ģenētiskā materiāla replikāciju, tā specifiku, informācijas glabāšanu molekulā un spēju mutēt.
Zinātnieki publicēja savu atklājumu žurnālā Nature 1953. gada 25. aprīlī. Pēc desmit gadiem kopā ar Morisu Vilkinsu viņiem tika piešķirta Nobela prēmija bioloģijā (Rozalinda Franklina nomira 1958. gadā no vēža 37 gadu vecumā).
"Tagad, vairāk nekā pusgadsimtu vēlāk, var apgalvot, ka DNS struktūras atklāšana bioloģijas attīstībā spēlēja tādu pašu lomu kā atoma kodola atklāšana fizikā. Atoma struktūras noskaidrošana noveda pie jaunas, kvantu fizikas dzimšana un DNS struktūras atklāšana noveda pie jaunas, molekulārās bioloģijas dzimšanas,” raksta izcilais ģenētiķis, DNS pētnieks, grāmatas “Svarīgākais” autors Maksims Franks-Kameneckis. Molekula”.
Ģenētiskais kods
Tagad atlika noskaidrot, kā šī molekula darbojas. Zināms, ka DNS satur instrukcijas šūnu proteīnu sintēzei, kas veic visu darbu šūnā. Olbaltumvielas ir polimēri, kas sastāv no atkārtotiem aminoskābju komplektiem (sekvencēm). Turklāt ir tikai divdesmit aminoskābes. Dzīvnieku sugas atšķiras viena no otras ar olbaltumvielu komplektu šūnās, tas ir, dažādās aminoskābju secībās. Ģenētika apgalvoja, ka šīs sekvences nosaka gēni, kas, kā toreiz tika uzskatīts, kalpo kā pirmie dzīvības celtniecības bloki. Bet kas ir gēni, neviens īsti nezināja.
Skaidrību ieviesa Lielā sprādziena teorijas autors, Džordža Vašingtona universitātes (ASV) darbinieks fiziķis Georgijs Gamovs. Pamatojoties uz Vatsona un Krika divpavedienu DNS spirāles modeli, viņš ierosināja, ka gēns ir DNS daļa, tas ir, noteikta saišu secība – nukleotīdi. Tā kā katrs nukleotīds ir viena no četrām slāpekļa bāzēm, atliek tikai noskaidrot, kā četri elementi kodē divdesmit. Tā bija ģenētiskā koda ideja.
Līdz 1960. gadu sākumam tika noteikts, ka olbaltumvielas tiek sintezētas no aminoskābēm ribosomās - sava veida "rūpnīcā" šūnas iekšienē. Lai sāktu proteīnu sintēzi, enzīms tuvojas DNS, atpazīst noteiktu apgabalu gēna sākumā, sintezē gēna kopiju nelielas RNS formā (to sauc par matricu), pēc tam no aminoskābēm tiek izaudzēts proteīns. ribosoma.
Viņi arī uzzināja, ka ģenētiskais kods ir trīs burtu. Tas nozīmē, ka vienai aminoskābei atbilst trīs nukleotīdi. Koda vienību sauc par kodonu. Ribosomā informāciju no mRNS secīgi nolasa pa kodonam pa kodonam. Un katrs no tiem atbilst vairākām aminoskābēm. Kā izskatās šifrs?
Uz šo jautājumu atbildēja Māršals Nirenbergs un Heinrihs Matejs no ASV. 1961. gadā viņi pirmo reizi ziņoja par saviem rezultātiem bioķīmijas kongresā Maskavā. Līdz 1967. gadam ģenētiskais kods bija pilnībā atšifrēts. Tas izrādījās universāls visām visu organismu šūnām, kam bija tālejošas sekas zinātnei.
DNS struktūras un ģenētiskā koda atklāšana ir pilnībā pārorientējusi bioloģiskos pētījumus. Fakts, ka katram indivīdam ir unikāla DNS secība, ir krasi mainījis kriminālistikas zinātni. Cilvēka genoma atšifrēšana ir devusi antropologiem pilnīgi jaunu veidu, kā pētīt mūsu sugas evolūciju. Nesen izgudrotais CRISPR-Cas DNS redaktors ir ievērojami uzlabojis gēnu inženieriju. Acīmredzot šī molekula glabā risinājumu arī cilvēces aktuālākajām problēmām: vēzis, ģenētiskās slimības, novecošanās.
Nukleīnskābes ir lielmolekulāras vielas, kas sastāv no mononukleotīdiem, kas ir savienoti viens ar otru polimēra ķēdē, izmantojot 3",5" - fosfodiestera saites un noteiktā veidā iepakotas šūnās.
Nukleīnskābes ir divu veidu biopolimēri: ribonukleīnskābe (RNS) un dezoksiribonukleīnskābe (DNS). Katrs biopolimērs sastāv no nukleotīdiem, kas atšķiras pēc ogļhidrātu atlikuma (ribozes, dezoksiribozes) un vienas no slāpekļa bāzēm (uracils, timīns). Attiecīgi nukleīnskābes ieguva savu nosaukumu.
Dezoksiribonukleīnskābes struktūra
Nukleīnskābēm ir primārā, sekundārā un terciārā struktūra.
DNS primārā struktūra
DNS primārā struktūra ir lineāra polinukleotīdu ķēde, kurā mononukleotīdi ir savienoti ar 3", 5" fosfodiestera saitēm. Izejmateriāls nukleīnskābes ķēdes montāžai šūnā ir nukleozīda 5'-trifosfāts, kas fosforskābes β un γ atlikumu noņemšanas rezultātā spēj piesaistīt cita nukleozīda 3'-oglekļa atomu. . Tādējādi vienas dezoksiribozes 3" oglekļa atoms kovalenti saistās ar citas dezoksiribozes 5" oglekļa atomu caur vienu fosforskābes atlikumu un veido lineāru nukleīnskābes polinukleotīdu ķēdi. Līdz ar to nosaukums: 3", 5"-fosfodiestera saites. Slāpekļa bāzes nepiedalās vienas ķēdes nukleotīdu savienošanā (1. att.).
Šāds savienojums starp viena nukleotīda fosforskābes molekulu un otra ogļhidrātu noved pie polinukleotīda molekulas pentozes-fosfāta mugurkaula veidošanās, uz kura no sāniem vienu pēc otras tiek pievienotas slāpekļa bāzes. To secība nukleīnskābju molekulu ķēdēs ir stingri specifiska dažādu organismu šūnām, t.i. ir specifisks raksturs (Čargafa noteikums).
Lineārai DNS ķēdei, kuras garums ir atkarīgs no ķēdē iekļauto nukleotīdu skaita, ir divi gali: vienu sauc par 3 "galu un tajā ir brīva hidroksilgrupa, bet otrs, 5" gals, satur fosforskābi. atlikumu. Ķēde ir polāra un var būt 5"->3" un 3"->5". Izņēmums ir apļveida DNS.
DNS ģenētisko "tekstu" veido koda "vārdi" - nukleotīdu tripleti, ko sauc par kodoniem. DNS segmentus, kas satur informāciju par visu veidu RNS primāro struktūru, sauc par strukturālajiem gēniem.
Polinukleodītiskās DNS ķēdes sasniedz milzīgus izmērus, tāpēc šūnā tās ir iepakotas noteiktā veidā.
Pētot DNS sastāvu, Chargaff (1949) konstatēja svarīgas likumsakarības attiecībā uz atsevišķu DNS bāzu saturu. Viņi palīdzēja atklāt DNS sekundāro struktūru. Šos modeļus sauc par Chargaff noteikumiem. Chargaff noteikumi
Šie noteikumi saka, ka, veidojot DNS, ir jāievēro diezgan stingra atbilstība (sairošana) nevis purīna un pirimidīna bāzēm kopumā, bet gan konkrēti timīnam ar adenīnu un citozīnam ar guanīnu. Pamatojoties uz šiem noteikumiem, cita starpā, 1953. gadā Vatsons un Kriks ierosināja DNS sekundārās struktūras modeli, ko sauc par dubulto spirāli (att.). |

DNS sekundārā struktūra
DNS sekundārā struktūra ir dubultspirāle, kuras modeli 1953. gadā ierosināja D. Vatsons un F. Kriks.
DNS modeļa izveides priekšnosacījumi
Sākotnējās analīzes rezultātā radās ideja, ka jebkuras izcelsmes DNS satur visus četrus nukleotīdus vienādos molāros daudzumos. Taču 20. gadsimta 40. gados E. Šargafs un viņa kolēģi no dažādiem organismiem izolētas DNS analīzes rezultātā skaidri parādīja, ka slāpekļa bāzes tajos ir ietvertas dažādās kvantitatīvās attiecībās. Chargaff atklāja, ka, lai gan šīs attiecības ir vienādas DNS no visām vienas un tās pašas organismu sugas šūnām, dažādu sugu DNS dažu nukleotīdu saturs var ievērojami atšķirties. Tas liecināja, ka atšķirības slāpekļa bāzu attiecībās varētu būt saistītas ar kādu bioloģisko kodu. Lai gan atsevišķo purīna un pirimidīna bāzu attiecība dažādos DNS paraugos nebija vienāda, salīdzinot analīžu rezultātus, atklājās konkrēts modelis: visos paraugos kopējais purīnu daudzums bija vienāds ar kopējo pirimidīnu daudzumu ( A + G = T + C), adenīna daudzums bija vienāds ar timīna daudzumu (A = T), bet guanīna daudzums - citozīna daudzumu (G = C). DNS, kas izolēta no zīdītāju šūnām, parasti bija bagātāka ar adenīnu un timīnu un salīdzinoši nabadzīgāka ar guanīnu un citozīnu, savukārt baktēriju DNS bija bagātāka ar guanīnu un citozīnu un salīdzinoši nabadzīgāka ar adenīnu un timīnu. Šie dati veidoja būtisku daļu no faktiskā materiāla, uz kura pamata vēlāk tika uzbūvēts Vatsona-Krika DNS struktūras modelis.
Vēl viena svarīga netieša norāde uz iespējamo DNS struktūru bija L. Paulinga dati par olbaltumvielu molekulu uzbūvi. Paulings parādīja, ka proteīna molekulā ir iespējamas vairākas dažādas stabilas aminoskābju ķēdes konfigurācijas. Viena no izplatītākajām peptīdu ķēdes konfigurācijām - α-spirāle - ir regulāra spirālveida struktūra. Ar šādu struktūru ir iespējama ūdeņraža saišu veidošanās starp aminoskābēm, kas atrodas blakus esošajos ķēdes pagriezienos. Polings aprakstīja polipeptīdu ķēdes α-spirālveida konfigurāciju 1950. gadā un ierosināja, ka arī DNS molekulām, iespējams, ir spirālveida struktūra, kas fiksēta ar ūdeņraža saitēm.
Taču visvērtīgāko informāciju par DNS molekulas uzbūvi sniedza rentgenstaru difrakcijas analīzes rezultāti. Rentgenstari, kas iziet cauri DNS kristālam, tiek pakļauti difrakcijai, tas ir, tie tiek novirzīti noteiktos virzienos. Staru novirzes pakāpe un raksturs ir atkarīgs no pašu molekulu struktūras. Rentgenstaru difrakcijas modelis (3. att.) sniedz pieredzējušai acij vairākas netiešas norādes par pētāmās vielas molekulu uzbūvi. DNS rentgenstaru difrakcijas modeļu analīze ļāva secināt, ka slāpekļa bāzes (ar plakanu formu) ir sakrautas kā plākšņu kaudze. Rentgenstaru modeļi ļāva identificēt trīs galvenos periodus kristāliskās DNS struktūrā: 0,34, 2 un 3,4 nm.

Vatsona-Krick DNS modelis
Sākot no Čārgafa analītiskajiem datiem, Vilkinsa rentgena un ķīmiķa pētījumiem, kas sniedza informāciju par precīzu attālumu starp atomiem molekulā, par leņķiem starp dotā atoma saitēm un par atomu izmēriem, Vatsons un Kriks. sāka veidot atsevišķus DNS molekulas komponentu fiziskus modeļus noteiktā mērogā.un "pielāgot" tos viens otram tā, lai iegūtā sistēma atbilstu dažādiem eksperimentāliem datiem. [rādīt] .
Pat agrāk bija zināms, ka blakus esošie nukleotīdi DNS ķēdē ir savienoti ar fosfodiestera tiltiem, kas savieno viena nukleotīda dezoksiribozes 5'-oglekļa atomu ar nākamā nukleotīda dezoksiribozes 3'-oglekļa atomu. Vatsonam un Krikam nebija šaubu, ka 0,34 nm periods atbilst attālumam starp secīgiem nukleotīdiem DNS virknē. Turklāt varētu pieņemt, ka 2 nm periods atbilst ķēdes biezumam. Un, lai izskaidrotu, kādai reālajai struktūrai atbilst 3,4 nm periods, Vatsons un Kriks, kā arī Polings iepriekš pieņēma, ka ķēde ir savīta spirāles formā (vai, precīzāk, veido spirāli, jo spirāle šī vārda tiešā nozīmē tiek iegūts, kad pagriezieni telpā veido konisku, nevis cilindrisku virsmu). Tad periods 3,4 nm atbildīs attālumam starp šīs spirāles secīgiem pagriezieniem. Šāda spirāle var būt ļoti blīva vai nedaudz izstiepta, t.i., tās pagriezieni var būt plakani vai stāvi. Tā kā 3,4 nm periods ir tieši 10 reizes lielāks par attālumu starp secīgiem nukleotīdiem (0,34 nm), ir skaidrs, ka katrs pilns spirāles pagrieziens satur 10 nukleotīdus. No šiem datiem Vatsons un Kriks spēja aprēķināt polinukleotīdu ķēdes blīvumu, kas savīti spirālē ar diametru 2 nm, ar attālumu starp pagriezieniem 3, 4 nm. Izrādījās, ka šādas virknes blīvums būtu uz pusi mazāks nekā faktiskais DNS blīvums, kas jau bija zināms. Man bija jāpieņem, ka DNS molekula sastāv no divām ķēdēm – ka tā ir nukleotīdu dubultspirāle.
Nākamais uzdevums, protams, bija noskaidrot telpiskās attiecības starp diviem pavedieniem, kas veido dubulto spirāli. Izmēģinājuši vairākus ķēžu izkārtojuma variantus savā fiziskajā modelī, Vatsons un Kriks atklāja, ka visiem pieejamajiem datiem vislabāk atbilst tāda, kurā divas polinukleotīdu spirāles iet pretējos virzienos; šajā gadījumā ķēdes, kas sastāv no cukura un fosfātu atlikumiem, veido dubultās spirāles virsmu, un iekšpusē atrodas purīni un pirimidīni. Bāzes, kas atrodas viena otrai pretī un pieder pie divām ķēdēm, ir savienotas pa pāriem ar ūdeņraža saitēm; tieši šīs ūdeņraža saites satur ķēdes kopā, tādējādi fiksējot kopējo molekulas konfigurāciju.
DNS dubulto spirāli var uzskatīt par spirālveida virvju kāpnēm, kuru pakāpieni paliek horizontāli. Tad divas garenvirziena virves atbildīs cukura un fosfāta atlieku ķēdēm, bet šķērsstieņi – slāpekļa bāzu pāriem, kas savienoti ar ūdeņraža saitēm.
Iespējamo modeļu turpmākās izpētes rezultātā Vatsons un Kriks nonāca pie secinājuma, ka katram "šķērsstienim" jāsastāv no viena purīna un viena pirimidīna; 2 nm periodā (atbilst dubultās spirāles diametram) diviem purīniem nepietiktu vietas, un abi pirimidīni nevarētu atrasties pietiekami tuvu viens otram, lai veidotu pareizas ūdeņraža saites. Detalizētā modeļa padziļināta izpēte parādīja, ka adenīnu un citozīnu, kas veido pareizā izmēra kombināciju, joprojām nevarēja sakārtot tā, lai starp tiem veidotos ūdeņraža saites. Līdzīgi ziņojumi arī lika izslēgt guanīna-timīna kombināciju, savukārt adenīna-timīna un guanīna-citozīna kombinācijas tika atzītas par diezgan pieņemamām. Ūdeņraža saišu raksturs ir tāds, ka adenīns savienojas ar timīnu, bet guanīns - ar citozīnu. Šī specifiskās bāzes savienošanas koncepcija ļāva izskaidrot "Chargaff likumu", saskaņā ar kuru jebkurā DNS molekulā adenīna daudzums vienmēr ir vienāds ar timīna saturu, bet guanīna daudzums vienmēr ir vienāds ar citozīna daudzumu. . Starp adenīnu un timīnu veidojas divas ūdeņraža saites, bet starp guanīnu un citozīnu - trīs. Sakarā ar šo specifiku ūdeņraža saišu veidošanā pret katru adenīnu vienā ķēdē, timīns atrodas otrā; tāpat pret katru guanīnu var likt tikai citozīnu. Tādējādi ķēdes ir viena otru komplementāras, tas ir, nukleotīdu secība vienā ķēdē unikāli nosaka to secību otrā. Abas ķēdes darbojas pretējos virzienos, un to fosfātu gala grupas atrodas dubultās spirāles pretējos galos.
Pētījumu rezultātā Vatsons un Kriks 1953. gadā ierosināja DNS molekulas struktūras modeli (3. att.), kas joprojām ir aktuāls līdz mūsdienām. Saskaņā ar modeli DNS molekula sastāv no divām komplementārām polinukleotīdu ķēdēm. Katra DNS virkne ir polinukleotīds, kas sastāv no vairākiem desmitiem tūkstošu nukleotīdu. Tajā blakus esošie nukleotīdi veido regulāru pentozes-fosfāta mugurkaulu, pateicoties spēcīgai kovalentai saitei, ko izraisa fosforskābes atlikums un dezoksiriboze. Vienas polinukleotīdu ķēdes slāpekļa bāzes ir izvietotas stingri noteiktā secībā pret otras ķēdes slāpekļa bāzēm. Slāpekļa bāzu maiņa polinukleotīdu ķēdē ir neregulāra.
Slāpekļa bāzu izkārtojums DNS ķēdē ir komplementārs (no grieķu "komplements" - pievienošana), t.i. pret adenīnu (A) vienmēr ir timīns (T), bet pret guanīnu (G) - tikai citozīns (C). Tas izskaidrojams ar to, ka A un T, kā arī G un C stingri atbilst viens otram, t.i. papildina viens otru. Šo atbilstību nodrošina bāzu ķīmiskā struktūra, kas ļauj veidot ūdeņraža saites purīna un pirimidīna pārī. Starp A un T ir divas saites, starp G un C - trīs. Šīs saites nodrošina daļēju DNS molekulas stabilizāciju telpā. Dubultās spirāles stabilitāte ir tieši proporcionāla G≡C saišu skaitam, kas ir stabilākas par A=T saitēm.
Zināmā nukleotīdu secība vienā DNS virknē ļauj pēc komplementaritātes principa noteikt citas virknes nukleotīdus.
Turklāt ir konstatēts, ka slāpekļa bāzes ar aromātisku struktūru ūdens šķīdumā atrodas viena virs otras, veidojot it kā monētu kaudzi. Šo organisko molekulu kaudzes veidošanas procesu sauc par sakraušanu. Aplūkotā Vatsona-Krika modeļa DNS molekulas polinukleotīdu ķēdēm ir līdzīgs fizikāli ķīmiskais stāvoklis, to slāpekļa bāzes ir sakārtotas monētu kaudzes veidā, starp kuru plaknēm notiek van der Vālsa mijiedarbība (kraušanas mijiedarbība).
Ūdeņraža saites starp komplementārām bāzēm (horizontāli) un sakraujoša mijiedarbība starp bāzes plaknēm polinukleotīdu ķēdē van der Vāla spēku dēļ (vertikāli) nodrošina DNS molekulai papildu stabilizāciju telpā.
Abu ķēžu cukura-fosfāta mugurkauli ir pagriezti uz āru, un pamatnes ir uz iekšu, viena pret otru. DNS virkņu virziens ir pretparalēls (vienai no tām ir virziens 5"->3", otrai - 3"->5", ti, vienas virknes 3" gals atrodas pretī 5" galam. no otras.). Ķēdes veido taisnas spirāles ar kopīgu asi. Viens spirāles apgrieziens ir 10 nukleotīdi, pagrieziena izmērs ir 3,4 nm, katra nukleotīda augstums ir 0,34 nm, spirāles diametrs ir 2,0 nm. Vienas virknes rotācijas rezultātā ap otru DNS dubultajā spirālē veidojas liela rieva (apmēram 20 Å diametrā) un neliela rieva (apmēram 12 Å). Šo Vatsona-Krika dubultās spirāles formu vēlāk sauca par B formu. Šūnās DNS parasti pastāv B formā, kas ir visstabilākā.
DNS funkcijas
Ierosinātais modelis izskaidro daudzas dezoksiribonukleīnskābes bioloģiskās īpašības, tostarp ģenētiskās informācijas uzglabāšanu un gēnu daudzveidību, ko nodrošina daudzas secīgas 4 nukleotīdu kombinācijas un ģenētiskā koda esamības faktu, spēju pašreproducēt un pārraidīt ģenētisko informāciju, ko nodrošina replikācijas process, un ģenētiskās informācijas realizācija proteīnu veidā, kā arī jebkuri citi savienojumi, kas veidojas ar fermentu proteīnu palīdzību.
DNS pamatfunkcijas.
- DNS ir ģenētiskās informācijas nesējs, ko nodrošina ģenētiskā koda esamības fakts.
- Reprodukcija un pārraidīta ģenētiskā informācija šūnu un organismu paaudzēs. Šo funkciju nodrošina replikācijas process.
- Ģenētiskās informācijas realizācija proteīnu veidā, kā arī jebkuri citi savienojumi, kas veidojas ar fermentu proteīnu palīdzību. Šo funkciju nodrošina transkripcijas un tulkošanas procesi.

Divpavedienu DNS organizācijas formas
DNS var veidot vairāku veidu dubultspirāles (4. att.). Šobrīd jau zināmas sešas formas (no A līdz E un Z-forma).
DNS strukturālās formas, kā to noteica Rosalind Franklin, ir atkarīgas no nukleīnskābes molekulas piesātinājuma ar ūdeni. DNS šķiedru pētījumos, izmantojot rentgenstaru difrakcijas analīzi, tika parādīts, ka rentgenstaru difrakcijas attēls radikāli ir atkarīgs no tā, pie kāda relatīvā mitruma, pie kādas šīs šķiedras ūdens piesātinājuma pakāpes notiek eksperiments. Ja šķiedra bija pietiekami piesātināta ar ūdeni, tad tika iegūta viena rentgenogramma. Žāvējot, parādījās pavisam cits rentgena attēls, kas ļoti atšķiras no augstas mitruma šķiedras rentgena attēla.
Augsta mitruma DNS molekulu sauc par B formu. Fizioloģiskos apstākļos (zema sāls koncentrācija, augsta hidratācijas pakāpe) dominējošais DNS strukturālais tips ir B forma (galvenā divpavedienu DNS forma ir Vatsona-Krika modelis). Šādas molekulas spirāles solis ir 3,4 nm. Vienā gājienā ir 10 papildinoši pāri savītu "monētu" kaudžu veidā - slāpekļa bāzes. Kaudzītes tiek turētas kopā ar ūdeņraža saitēm starp divām pretējām skursteņu "monētām", un tās ir "aptītas" ar divām fosfodiestera mugurkaula lentēm, kas savītas labās puses spirālē. Slāpekļa pamatu plaknes ir perpendikulāras spirāles asij. Kaimiņos esošie komplementārie pāri ir pagriezti viens pret otru par 36°. Spirāles diametrs ir 20Å, purīna nukleotīds aizņem 12Å un pirimidīna nukleotīds aizņem 8Å.
Zemāka mitruma DNS molekulu sauc par A formu. A forma veidojas mazāk augsta hidratācijas apstākļos un pie lielāka Na + vai K + jonu satura. Šai plašākai labās puses uzbūvei ir 11 bāzes pāri vienā pagriezienā. Slāpekļa pamatu plaknēm ir spēcīgāks slīpums pret spirāles asi, tās novirzās no normālās uz spirāles asi par 20°. Tas nozīmē, ka ir iekšējs tukšums ar diametru 5 Å. Attālums starp blakus esošajiem nukleotīdiem ir 0,23 nm, spoles garums ir 2,5 nm, un spirāles diametrs ir 2,3 nm.
Sākotnēji tika uzskatīts, ka DNS A forma ir mazāk svarīga. Taču vēlāk izrādījās, ka DNS A formai, tāpat kā B formai, ir liela bioloģiskā nozīme. RNS-DNS spirālei veidnes-sēklu kompleksā, kā arī RNS-RNS spirāles un RNS matadata struktūrām ir A forma (ribozes 2'-hidroksilgrupa neļauj RNS molekulām veidot B formu) . DNS A forma ir atrodama sporās. Ir noskaidrots, ka DNS A forma ir 10 reizes izturīgāka pret UV stariem nekā B forma.
A formu un B formu sauc par DNS kanoniskajām formām.
Veidlapas C-E arī labroči, to veidošanos var novērot tikai īpašos eksperimentos, un, acīmredzot, tie neeksistē in vivo. DNS C formai ir līdzīga struktūra kā B-DNS. Bāzes pāru skaits vienā apgriezienā ir 9,33, un spirāles garums ir 3,1 nm. Bāzes pāri ir slīpi 8 grādu leņķī attiecībā pret perpendikulāro stāvokli asij. Rievu izmērs ir tuvu B-DNS rievām. Šajā gadījumā galvenā rieva ir nedaudz mazāka, un mazākā rieva ir dziļāka. Dabiskie un sintētiskie DNS polinukleotīdi var nonākt C formā.
| 1. tabula. Dažu veidu DNS struktūru raksturojums | |||
| Spirālveida tips | A | B | Z |
| Spirālveida solis | 0,32 nm | 3,38 nm | 4,46 nm |
| Spirālveida vērpjot | Taisnība | Taisnība | Pa kreisi |
| Bāzes pāru skaits vienā apgriezienā | 11 | 10 | 12 |
| Attālums starp bāzes plaknēm | 0,256 nm | 0,338 nm | 0,371 nm |
| Glikozīdiskās saites konformācija | anti | anti | anti-C sin-G |
| Furanozes gredzena uzbūve | C3 "-endo | C2 "-endo | C3 "-endo-G C2 "-endo-C |
| Rievu platums, mazs/liels | 1,11/0,22 nm | 0,57/1,17 nm | 0,2/0,88 nm |
| Rievu dziļums, mazs/liels | 0,26/1,30 nm | 0,82/0,85 nm | 1,38/0,37 nm |
| Spirāles diametrs | 2,3 nm | 2,0 nm | 1,8 nm |
DNS strukturālie elementi
(nekanoniskas DNS struktūras)
DNS strukturālie elementi ietver neparastas struktūras, ko ierobežo dažas īpašas sekvences:
|

DNS Z-forma tika atklāts 1979. gadā, pētot heksanukleotīdu d(CG)3 - . To atklāja MIT profesors Aleksandrs Ričs un viņa darbinieki. Z-forma ir kļuvusi par vienu no svarīgākajiem DNS strukturālajiem elementiem, jo tās veidošanās tika novērota DNS reģionos, kur purīni mijas ar pirimidīniem (piemēram, 5'-HCHCHC-3'), vai atkārtojumos 5'. -CHCHCH-3', kas satur metilētu citozīnu. Būtisks nosacījums Z-DNS veidošanai un stabilizācijai bija purīna nukleotīdu klātbūtne tajā sin-konformācijā, kas mijās ar pirimidīna bāzēm antikonformācijā.
Dabiskās DNS molekulas lielākoties pastāv pareizajā B formā, ja vien tās nesatur tādas sekvences kā (CG)n. Taču, ja šādas sekvences ir daļa no DNS, tad šie reģioni, kad šķīduma jonu stiprums vai katjoni, kas neitralizē fosfodiestera mugurkaula negatīvo lādiņu, var mainīties Z formā, bet pārējie DNS reģioni ķēdē paliek. klasiskajā B formā. Šādas pārejas iespēja norāda, ka abas DNS dubultās spirāles virknes atrodas dinamiskā stāvoklī un var atvienoties viena pret otru, pārejot no labās formas uz kreiso un otrādi. Šīs labilitātes bioloģiskās sekas, kas ļauj veikt DNS struktūras konformācijas transformācijas, vēl nav pilnībā izprastas. Tiek uzskatīts, ka Z-DNS reģioniem ir nozīme noteiktu gēnu ekspresijas regulēšanā un tie piedalās ģenētiskajā rekombinācijā.
DNS Z-forma ir kreisās puses dubultspirāle, kurā fosfodiestera mugurkauls ir zigzaga veidā pa molekulas asi. Līdz ar to molekulas nosaukums (zigzags)-DNS. Z-DNS ir vismazāk savīti (12 bāzes pāri vienā pagriezienā) un plānākā zināmā dabā. Attālums starp blakus esošajiem nukleotīdiem ir 0,38 nm, spoles garums ir 4,56 nm, un Z-DNS diametrs ir 1,8 nm. Turklāt šīs DNS molekulas izskats izceļas ar vienas rievas klātbūtni.
DNS Z forma ir atrasta prokariotu un eikariotu šūnās. Līdz šim ir iegūtas antivielas, kas spēj atšķirt DNS Z formu un B formu. Šīs antivielas saistās ar specifiskiem Drosophila (Dr. melanogaster) siekalu dziedzeru šūnu milzu hromosomu reģioniem. Saistīšanās reakcijai ir viegli sekot, pateicoties šo hromosomu neparastajai struktūrai, kurā blīvāki reģioni (diski) kontrastē ar mazāk blīviem reģioniem (starpdiski). Z-DNS reģioni atrodas starpdiskos. No tā izriet, ka Z-forma faktiski eksistē dabiskos apstākļos, lai gan Z-formas atsevišķu posmu izmēri vēl nav zināmi.

(shifters) - slavenākās un biežāk sastopamās bāzes sekvences DNS. Palindroms ir vārds vai frāze, kas skan no kreisās puses uz labo un otrādi tādā pašā veidā. Šādu vārdu vai frāžu piemēri ir: BŪDA, KAZAKS, PLŪDI UN UZ AZORA KĒPĀM NOKRITUSI ROZE. Piemērojot DNS sekcijām, šis termins (palindroms) nozīmē to pašu nukleotīdu maiņu ķēdē no labās uz kreiso un no kreisās puses uz labo (tāpat kā burti vārdā "būda" utt.).
Palindromu raksturo apgrieztu bāzes secību atkārtojumu klātbūtne ar otrās kārtas simetriju attiecībā pret divām DNS virknēm. Šādas sekvences acīmredzamu iemeslu dēļ ir sevi papildinošas un mēdz veidot matadatas vai krustveida struktūras (att.). Matadatas palīdz regulējošajiem proteīniem atpazīt vietu, kur tiek kopēts hromosomu DNS ģenētiskais teksts.
Gadījumos, kad vienā un tajā pašā DNS virknē ir apgriezts atkārtojums, šādu secību sauc par spoguļatkārtojumu. Spoguļatkārtojumiem nav sevi papildinošu īpašību, un tāpēc tie nespēj veidot matadatas vai krustveida struktūras. Šāda veida sekvences ir atrodamas gandrīz visās lielajās DNS molekulās, un tās var būt no dažiem bāzes pāriem līdz vairākiem tūkstošiem bāzu pāru.
Palindromu klātbūtne krustveida struktūru veidā eikariotu šūnās nav pierādīta, lai gan E. coli šūnās in vivo ir konstatētas vairākas krustveida struktūras. Paškomplementāru sekvenču klātbūtne RNS vai vienpavedienu DNS ir galvenais iemesls nukleīna ķēdes locīšanai šķīdumos noteiktā telpiskā struktūrā, ko raksturo daudzu "matadatu" veidošanās.

DNS H-forma- šī ir spirāle, ko veido trīs DNS pavedieni - DNS trīskāršā spirāle. Tas ir Vatsona-Krika dubultspirāles komplekss ar trešo vienpavedienu DNS virkni, kas iekļaujas tās lielajā rievā, veidojot tā saukto Hoogstīna pāri.
Šāda tripleksa veidošanās notiek DNS dubultspirāles pievienošanas rezultātā tā, ka puse no tās sadaļas paliek dubultspirāles formā, bet otrā puse ir atvienota. Šajā gadījumā viena no atvienotajām spirālēm veido jaunu struktūru ar dubultās spirāles pirmo pusi - trīskāršo spirāli, un otrā izrādās nestrukturēta, viena pavediena sekcijas veidā. Šīs strukturālās pārejas iezīme ir asa atkarība no vides pH, kura protoni stabilizē jauno struktūru. Šīs iezīmes dēļ jauno struktūru nosauca par DNS H formu, kuras veidošanās tika konstatēta superspirētās plazmīdās, kas satur homopurīna-homopirimidīna reģionus, kas ir spoguļatkārtojums.
Turpmākajos pētījumos tika noteikta dažu homopurīna-homopirimidīna divpavedienu polinukleotīdu strukturālas pārejas iespēja, veidojot trīspavedienu struktūru, kas satur:
- viena homopurīna un divas homopirimidīna pavedieni ( Py-Pu-Py triplekss) [Hoogsteen mijiedarbība].
Py-Pu-Py tripleksa bloki ir kanoniski izomorfi CGC+ un TAT triādes. Tripleksa stabilizēšanai nepieciešama CGC+ triādes protonēšana, tāpēc šie tripleksi ir atkarīgi no šķīduma pH.
- viena homopirimidīna un divas homopurīna pavedieni ( Py-Pu-Pu triplekss) [apgrieztā Hoogstīna mijiedarbība].
Py-Pu-Pu tripleksa bloki ir kanoniskās izomorfās CGG un TAA triādes. Būtiska Py-Pu-Pu tripleksu īpašība ir to stabilitātes atkarība no divkārši lādētu jonu klātbūtnes, un ir nepieciešami dažādi joni, lai stabilizētu dažādu secību tripleksus. Tā kā Py-Pu-Pu tripleksu veidošanai nav nepieciešama to sastāvā esošo nukleotīdu protonēšana, šādi tripleksi var pastāvēt pie neitrāla pH.
Piezīme: tiešā un apgrieztā Hoogstīna mijiedarbība ir izskaidrojama ar 1-metiltimīna simetriju: 180 ° rotācija noved pie tā, ka O4 atoma vietu aizņem O2 atoms, bet ūdeņraža saišu sistēma tiek saglabāta.
Ir divu veidu trīskāršās spirāles:
- paralēlas trīskāršas spirāles, kurās trešās daļas polaritāte ir tāda pati kā Vatsona-Krick dupleksa homopurīna ķēdes polaritātei
- antiparalēlas trīskāršās spirāles, kurās trešās un homopurīna ķēdes polaritātes ir pretējas.

G-kvadruplekss- 4-pavedienu DNS. Šāda struktūra veidojas, ja ir četri guanīni, kas veido tā saukto G-kvadrupleksu – četru guanīnu apaļo deju.
Pirmie mājieni par šādu struktūru veidošanās iespējamību tika iegūti ilgi pirms Vatsona un Krika izrāviena darba - jau 1910. gadā. Tad vācu ķīmiķis Ivars Bangs atklāja, ka viena no DNS sastāvdaļām – guanozīnskābe – lielās koncentrācijās veido želejas, savukārt citām DNS sastāvdaļām šīs īpašības nav.
1962. gadā, izmantojot rentgenstaru difrakcijas metodi, izdevās noteikt šī gēla šūnu struktūru. Izrādījās, ka tas sastāv no četriem guanīna atlikumiem, kas savieno viens otru aplī un veido raksturīgu kvadrātu. Centrā saiti atbalsta metāla jons (Na, K, Mg). Tādas pašas struktūras var veidoties DNS, ja tajā ir daudz guanīna. Šie plakanie kvadrāti (G kvarteti) ir sakrauti, lai veidotu diezgan stabilas, blīvas struktūras (G kvadrupleksi).
Četras atsevišķas DNS virknes var ieaust četrpavedienu kompleksos, taču tas drīzāk ir izņēmums. Biežāk viena nukleīnskābes virkne tiek vienkārši sasieta mezglā, veidojot raksturīgus sabiezējumus (piemēram, hromosomu galos), vai arī divpavedienu DNS veido lokālu kvadrupleksu kādā ar guanīnu bagātā vietā.
Visvairāk pētīta ir kvadrupleksu esamība hromosomu galos – uz telomēriem un onkopromoteros. Tomēr pilnīga izpratne par šādas DNS lokalizāciju cilvēka hromosomās joprojām nav zināma.
Visas šīs neparastās DNS struktūras lineārajā formā ir nestabilas salīdzinājumā ar DNS B formu. Tomēr DNS bieži vien pastāv topoloģiskā spriedzes gredzena formā, kad tai ir tā sauktā superspirāle. Šādos apstākļos viegli veidojas nekanoniskas DNS struktūras: Z formas, "krusti" un "matadatas", H formas, guanīna kvadrupleksi un i-motīvs.
- Supercoiled forma – tiek atzīmēta, atbrīvojoties no šūnas kodola, nesabojājot pentozes-fosfāta mugurkaulu. Tam ir supervītu slēgtu gredzenu forma. Supervītā stāvoklī DNS dubultspirāle vismaz vienu reizi tiek "savīta uz sevi", t.i., tajā ir vismaz viena superspirāle (pieņem astotnieka formu).
- Atslābināts DNS stāvoklis - novērots ar vienu pārtraukumu (vienas virknes pārtraukums). Šajā gadījumā superspirāles pazūd, un DNS iegūst slēgta gredzena formu.
- DNS lineārā forma tiek novērota, kad tiek salauzti divi dubultās spirāles pavedieni.
DNS terciārā struktūra
DNS terciārā struktūra veidojas divpavedienu molekulas papildus savīšanas rezultātā telpā - tās superspirāles rezultātā. DNS molekulas superspirācija eikariotu šūnās, atšķirībā no prokariotiem, tiek veikta kompleksu veidā ar olbaltumvielām.
Gandrīz visa eikariotu DNS atrodas kodolu hromosomās, tikai neliels tās daudzums ir atrodams mitohondrijās, augos un plastidos. Eikariotu šūnu (tostarp cilvēka hromosomu) hromosomu galvenā viela ir hromatīns, kas sastāv no divpavedienu DNS, histona un nehistona proteīniem.
Hromatīna histonu proteīni
Histoni ir vienkārši proteīni, kas veido līdz 50% hromatīna. Visās pētītajās dzīvnieku un augu šūnās tika konstatētas piecas galvenās histonu klases: H1, H2A, H2B, H3, H4, kas atšķiras pēc izmēra, aminoskābju sastāva un lādiņa (vienmēr pozitīvs).
Zīdītāju histons H1 sastāv no vienas polipeptīda ķēdes, kas satur aptuveni 215 aminoskābes; citu histonu izmēri svārstās no 100 līdz 135 aminoskābēm. Visi no tiem ir spiralizēti un savīti globulā ar diametru aptuveni 2,5 nm, satur neparasti lielu daudzumu pozitīvi lādētu aminoskābju lizīna un arginīna. Histoni var būt acetilēti, metilēti, fosforilēti, poli(ADP)-ribosilēti, un histoni H2A un H2B var būt kovalenti saistīti ar ubikvitīnu. Kāda ir šādu modifikāciju nozīme histonu struktūras veidošanā un funkciju veikšanā, vēl nav pilnībā noskaidrota. Tiek pieņemts, ka tā ir viņu spēja mijiedarboties ar DNS un nodrošināt vienu no gēnu darbības regulēšanas mehānismiem.
Histoni mijiedarbojas ar DNS galvenokārt caur jonu saitēm (sāls tiltiem), kas veidojas starp negatīvi lādētām DNS fosfātu grupām un histonu pozitīvi lādētajām lizīna un arginīna atliekām.
Hromatīna nehistona proteīni
Nehistona proteīni, atšķirībā no histoniem, ir ļoti dažādi. Ir izolētas līdz 590 dažādām DNS saistošo nehistona proteīnu frakcijām. Tos sauc arī par skābiem proteīniem, jo to struktūrā dominē skābās aminoskābes (tie ir polianjoni). Hromatīna aktivitātes specifiskā regulēšana ir saistīta ar dažādiem nehistona proteīniem. Piemēram, fermenti, kas ir būtiski DNS replikācijai un ekspresijai, var īslaicīgi saistīties ar hromatīnu. Citi proteīni, piemēram, tie, kas iesaistīti dažādos regulējošos procesos, saistās ar DNS tikai konkrētos audos vai noteiktos diferenciācijas posmos. Katrs proteīns ir komplementārs ar noteiktu DNS nukleotīdu secību (DNS vietu). Šajā grupā ietilpst:
- vietai raksturīgu cinka pirkstu proteīnu saime. Katrs "cinka pirksts" atpazīst noteiktu vietu, kas sastāv no 5 nukleotīdu pāriem.
- vietai raksturīgo proteīnu saime – homodimēri. Šāda proteīna fragmentam, kas saskaras ar DNS, ir struktūra "spirāle-pagrieziens-spirāle".
- augstas mobilitātes proteīni (HMG proteins - no angļu valodas, high mobility gel proteins) ir strukturālo un regulējošo proteīnu grupa, kas pastāvīgi ir saistīta ar hromatīnu. To molekulmasa ir mazāka par 30 kD, un tiem raksturīgs augsts lādētu aminoskābju saturs. Zemās molekulmasas dēļ HMG proteīni ir ļoti mobili poliakrilamīda gēla elektroforēzes laikā.
- replikācijas, transkripcijas un labošanas enzīmi.
Piedaloties DNS un RNS sintēzē iesaistītajiem strukturālajiem, regulējošajiem proteīniem un fermentiem, nukleosomu pavediens tiek pārveidots par ļoti kondensētu proteīnu un DNS kompleksu. Iegūtā struktūra ir 10 000 reižu īsāka nekā sākotnējā DNS molekula.

Hromatīns
Hromatīns ir proteīnu komplekss ar kodola DNS un neorganiskām vielām. Lielākā daļa hromatīna ir neaktīvs. Tas satur blīvi iesaiņotu, kondensētu DNS. Tas ir heterohromatīns. Ir konstitutīvs, ģenētiski neaktīvs hromatīns (satelīta DNS), kas sastāv no neizteiktiem reģioniem, un fakultatīvs - neaktīvs vairākās paaudzēs, bet noteiktos apstākļos spēj izteikties.
Aktīvais hromatīns (eihromatīns) ir nekondensēts, t.i. iesaiņots mazāk cieši. Dažādās šūnās tā saturs svārstās no 2 līdz 11%. Smadzeņu šūnās tas ir visvairāk - 10-11%, aknu šūnās - 3-4 un nierēs - 2-3%. Notiek aktīva eihromatīna transkripcija. Tajā pašā laikā tā strukturālā organizācija ļauj specializētās šūnās dažādos veidos izmantot vienu un to pašu DNS ģenētisko informāciju, kas raksturīga noteikta veida organismam.
Elektronu mikroskopā hromatīna attēls atgādina lodītes: apmēram 10 nm lielus sfēriskus sabiezējumus, kas atdalīti ar pavedienveida tiltiņiem. Šos sfēriskos sabiezējumus sauc par nukleosomām. Nukleosoma ir hromatīna struktūrvienība. Katra nukleosoma satur 146 bp garu superspirālu DNS segmentu, kas veido 1,75 kreiso pagriezienu katrā nukleosomas kodolā. Nukleosomu kodols ir histona oktamērs, kas sastāv no H2A, H2B, H3 un H4 histoniem, divām katra veida molekulām (9. att.), kas izskatās kā disks 11 nm diametrā un 5,7 nm biezumā. Piektais histons, H1, nav daļa no nukleosomu kodola un nav iesaistīts DNS vijuma procesā ap histona oktamēru. Tas saskaras ar DNS punktos, kur dubultā spirāle ieiet un iziet no nukleosomu kodola. Tās ir DNS starpkodolu (linkera) sekcijas, kuru garums atkarībā no šūnas veida mainās no 40 līdz 50 nukleotīdu pāriem. Rezultātā mainās arī DNS fragmenta garums, kas ir daļa no nukleosomām (no 186 līdz 196 nukleotīdu pāriem).
Nukleosoma satur aptuveni 90% DNS, pārējā daļa ir saistītājs. Tiek uzskatīts, ka nukleosomas ir "klusā" hromatīna fragmenti, kamēr saistītājs ir aktīvs. Tomēr nukleosomas var izvērsties un kļūt lineāras. Atlocītās nukleosomas jau ir aktīvs hromatīns. Tas skaidri parāda funkcijas atkarību no struktūras. Var pieņemt, ka jo vairāk hromatīna ir lodveida nukleosomu sastāvā, jo mazāk aktīvs tas ir. Acīmredzot dažādās šūnās nevienlīdzīgā miera stāvoklī esošā hromatīna proporcija ir saistīta ar šādu nukleosomu skaitu.
Uz elektronu mikroskopiskām fotogrāfijām atkarībā no izolācijas apstākļiem un stiepšanās pakāpes hromatīns var izskatīties ne tikai kā garš pavediens ar sabiezējumiem - nukleosomu "krelles", bet arī kā īsāka un blīvāka fibrila (šķiedra) ar diametru 30 nm, kura veidošanās tiek novērota mijiedarbības histona H1 laikā, kas saistīts ar DNS linkera reģionu un histonu H3, kas noved pie sešu nukleosomu spirāles papildu savīšanas vienā apgriezienā, veidojoties solenoīdam ar diametru 30 nm . Šajā gadījumā histona proteīns var traucēt vairāku gēnu transkripciju un tādējādi regulēt to darbību.
Iepriekš aprakstītās DNS mijiedarbības ar histoniem rezultātā DNS dubultās spirāles segments, kas sastāv no 186 bāzes pāriem ar vidējo diametru 2 nm un garumu 57 nm, pārvēršas par spirāli ar diametru 10 nm un garumu. no 5 nm. Pēc tam šīs spirāles saspiešanas līdz šķiedrai ar diametru 30 nm kondensācijas pakāpe palielinās vēl sešas reizes.
Galu galā DNS dupleksa iepakojums ar pieciem histoniem rada 50 kārtīgu DNS kondensāciju. Tomēr pat tik augsta kondensācijas pakāpe nevar izskaidrot gandrīz 50 000-100 000 reižu DNS sablīvēšanos metafāzes hromosomā. Diemžēl sīkāka informācija par hromatīna tālāko iepakošanu līdz metafāzes hromosomai vēl nav zināma, tāpēc var aplūkot tikai šī procesa vispārīgās iezīmes.
DNS blīvēšanas līmeņi hromosomās
Katra DNS molekula ir iepakota atsevišķā hromosomā. Diploīdās cilvēka šūnas satur 46 hromosomas, kas atrodas šūnas kodolā. Šūnas visu hromosomu DNS kopējais garums ir 1,74 m, bet kodola diametrs, kurā ir iepakotas hromosomas, ir miljoniem reižu mazāks. Šādu kompaktu DNS iesaiņojumu hromosomās un hromosomās šūnas kodolā nodrošina dažādi histonu un nehistona proteīni, kas noteiktā secībā mijiedarbojas ar DNS (skatīt iepriekš). DNS sablīvēšanās hromosomās ļauj samazināt tās lineāros izmērus aptuveni 10 000 reižu - nosacīti no 5 cm līdz 5 mikroniem. Ir vairāki blīvēšanas līmeņi (10. att.).


- DNS dubultspirāle ir negatīvi lādēta molekula, kuras diametrs ir 2 nm un garums ir vairāki cm.
- nukleosomu līmenis- hromatīns elektronu mikroskopā izskatās kā "krelles" - nukleosomu - "uz pavediena" ķēde. Nukleosoma ir universāla struktūrvienība, kas atrodama gan eihromatīnā, gan heterohromatīnā, starpfāzu kodolā un metafāzes hromosomās.
Nukleosomu blīvēšanas līmeni nodrošina īpaši proteīni - histoni. Astoņi pozitīvi lādēti histona domēni veido nukleosomas kodolu (kodolu), ap kuru ir apvīts negatīvi lādētā DNS molekula. Tas nodrošina saīsinājumu par 7, bet diametrs palielinās no 2 līdz 11 nm.
- solenoīda līmenis
Hromosomu organizācijas solenoīda līmenim ir raksturīga nukleosomu pavediena savīšana un no tā veidojas biezākas fibrilus 20-35 nm diametrā - solenoīdus jeb superbids. Solenoīda solis ir 11 nm, un vienā apgriezienā ir apmēram 6-10 nukleosomas. Solenoīda iepakojums tiek uzskatīts par ticamāku nekā superbid iepakojums, saskaņā ar kuru hromatīna fibrila ar diametru 20–35 nm ir granulu ķēde jeb superbids, no kurām katra sastāv no astoņām nukleosomām. Solenoīda līmenī DNS lineārais izmērs tiek samazināts 6-10 reizes, diametrs palielinās līdz 30 nm.
- cilpas līmenis
Cilpas līmeni nodrošina vietnei nespecifiski DNS saistoši proteīni, kas atpazīst un saistās ar specifiskām DNS sekvencēm, veidojot aptuveni 30-300 kb cilpas. Cilpa nodrošina gēnu ekspresiju, t.i. cilpa ir ne tikai strukturāls, bet arī funkcionāls veidojums. Saīsināšana šajā līmenī notiek 20-30 reizes. Diametrs palielinās līdz 300 nm. Uz citoloģiskajiem preparātiem var redzēt cilpveida "lampas sukas" struktūras abinieku oocītos. Šķiet, ka šīs cilpas ir supercoilētas un attēlo DNS domēnus, kas, iespējams, atbilst hromatīna transkripcijas un replikācijas vienībām. Specifiski proteīni fiksē cilpu pamatnes un, iespējams, dažus to iekšējos reģionus. Cilpveida domēna organizācija atvieglo hromatīna locīšanu metafāzes hromosomās augstākās kārtas spirālveida struktūrās.
- domēna līmenī
Hromosomu organizācijas domēna līmenis nav pietiekami pētīts. Šajā līmenī tiek atzīmēta cilpas domēnu veidošanās - 25-30 nm biezu pavedienu (fibrilu) struktūras, kas satur 60% proteīna, 35% DNS un 5% RNS, ir praktiski neredzamas visās šūnu cikla fāzēs. izņēmums ir mitoze un ir nedaudz nejauši sadalīti pa šūnas kodolu. Uz citoloģiskajiem preparātiem var redzēt cilpveida "lampas sukas" struktūras abinieku oocītos.
Cilpas domēni ar savu pamatni ir pievienoti intranukleārajai proteīna matricai tā sauktajās iebūvētajās piestiprināšanas vietās, ko bieži dēvē par MAR / SAR sekvencēm (MAR, no angļu valodas matricas saistītā reģiona; SAR, no angļu sastatņu piestiprināšanas reģioniem) - DNS fragmenti vairāki simti garu bāzu pāru, kam raksturīgs augsts A/T bāzu pāru saturs (>65%). Šķiet, ka katram domēnam ir viens replikācijas avots, un tas darbojas kā autonoma supercoiled vienība. Jebkurš cilpas domēns satur daudzas transkripcijas vienības, kuru darbība, visticamāk, ir koordinēta – viss domēns ir vai nu aktīvā, vai neaktīvā stāvoklī.
Domēna līmenī secīgas hromatīna iepakošanas rezultātā DNS lineārie izmēri samazinās apmēram 200 reizes (700 nm).
- hromosomu līmenis
Hromosomu līmenī profāzes hromosoma kondensējas metafāzē, saspiežot cilpas domēnus ap nehistona proteīnu aksiālo karkasu. Šo superspolēšanu pavada visu šūnā esošo H1 molekulu fosforilēšanās. Rezultātā metafāzes hromosomu var attēlot kā blīvi iesaiņotas solenoīda cilpas, kas satītas stingrā spirālē. Tipiskā cilvēka hromosoma var saturēt līdz 2600 cilpām. Šādas struktūras biezums sasniedz 1400 nm (divas hromatīdas), savukārt DNS molekula tiek saīsināta 104 reizes, t.i. no 5 cm izstiepta DNS līdz 5 µm.
Hromosomu funkcijas
Mijiedarbojoties ar ārpushromosomu mehānismiem, hromosomas nodrošina
- iedzimtas informācijas glabāšana
- izmantojot šo informāciju, lai izveidotu un uzturētu šūnu organizāciju
- iedzimtības informācijas lasīšanas regulējums
- ģenētiskā materiāla pašdublēšanās
- ģenētiskā materiāla pārnešana no mātes šūnas uz meitas šūnām.
Ir pierādījumi, ka, aktivizējoties hromatīna reģionam, t.i. transkripcijas laikā no tā vispirms tiek atgriezeniski noņemts histons H1 un pēc tam histona oktets. Tas izraisa hromatīna dekondensāciju, 30 nm hromatīna fibrila secīgu pāreju uz 10 nm pavedienu un tā tālāku izvēršanos brīvos DNS reģionos, t.i. nukleosomu struktūras zudums.
Gandrīz visi ir dzirdējuši par DNS molekulu esamību dzīvās šūnās un zina, ka šī molekula ir atbildīga par iedzimtas informācijas pārraidi. Milzīgs ķekars dažādu filmu vienā vai otrā pakāpē veido savu sižetu uz mazas, bet lepnas, ļoti svarīgas molekulas īpašībām.
Tomēr daži cilvēki var vismaz aptuveni izskaidrot, kas īsti ir daļa no DNS molekulas un kā darbojas visas šīs informācijas nolasīšanas procesi par "visa organisma uzbūvi". Tikai daži spēj bez vilcināšanās izlasīt “dezoksiribonukleīnskābi”.
Mēģināsim izdomāt, no kā tā sastāv un kā tā izskatās kā vissvarīgākā molekula katram no mums.
Strukturālās saites struktūra - nukleotīds
DNS molekulas sastāvs ietver daudzas struktūrvienības, jo tā ir biopolimērs. Polimērs ir makromolekula, kas sastāv no daudziem maziem atkārtotiem fragmentiem, kas savienoti virknē. Tāpat kā ķēde sastāv no saitēm.
DNS makromolekulas struktūrvienība ir nukleotīds. DNS molekulas nukleotīdu sastāvā ir trīs vielu atliekas - fosforskābe, saharīds (dezoksiriboze) un viena no četrām iespējamām slāpekli saturošām bāzēm.
DNS molekulas sastāvā ietilpst slāpekļa bāzes: adenīns (A), guanīns (G), citozīns (C) un timīns (T).

Nukleotīdu ķēdes sastāvs tiek parādīts, mainoties tajā iekļautajām bāzēm: -AAGCGTTAGCACGT- utt. Secība var būt jebkura. Tas veido vienu DNS virkni.
Spirālveida molekula. Komplementaritātes fenomens
Cilvēka DNS molekulas izmērs ir milzīgs (protams, citu molekulu mērogā)! Vienas šūnas (46 hromosomas) genoms satur aptuveni 3,1 miljardu bāzes pāru. DNS ķēdes garums, kas sastāv no šāda skaita saišu, ir aptuveni divi metri. Ir grūti iedomāties, kā tik apjomīgu molekulu var ievietot mazā šūnā.
Taču daba parūpējās par kompaktāku iepakojumu un sava genoma aizsardzību – divas ķēdes ir savstarpēji saistītas ar slāpekļa bāzēm un veido labi zināmu dubultspirāli. Tādējādi ir iespējams samazināt molekulas garumu gandrīz sešas reizes.
Slāpekļa bāzu mijiedarbības secību stingri nosaka komplementaritātes fenomens. Adenīns var saistīties tikai ar timīnu, savukārt citozīns var saistīties tikai ar guanīnu. Šie papildinošie pāri sader kopā kā atslēga un slēdzene kā puzles gabaliņi.
Tagad aprēķināsim, cik daudz atmiņas datorā (nu vai zibatmiņas diskā) vajadzētu aizņemt visai informācijai par šo mazo (mūsu pasaules mērogā) molekulu. Bāzes pāru skaits ir 3,1x10 9 . Kopā ir 4 vērtības, kas nozīmē, ka vienam pārim pietiek ar 2 bitiem informācijas (2 2 vērtības). Mēs to visu reizinām viens ar otru un iegūstam 6200000000 bitu jeb 775000000 baitu, vai 775000 kilobaitu, jeb 775 megabaitus. Kas aptuveni atbilst CD diska ietilpībai vai kādas 40 minūšu filmu sērijas apjomam vidējā kvalitātē.
Hromosomu veidošanās. Cilvēka genoma noteikšana
Papildus spiralizācijai molekula tiek atkārtoti pakļauta blīvēšanai. Dubultā spirāle sāk vērpties kā vītnes lode – šo procesu sauc par superspirāli un notiek ar speciāla histona proteīna palīdzību, uz kura kā spole tiek uztīta ķēde.
Šis process samazina molekulas garumu vēl 25-30 reizes. Pakļaujot vēl vairākiem iepakojuma līmeņiem, arvien vairāk sablīvējoties, viena DNS molekula kopā ar palīgproteīniem veido hromosomu.

Visu informāciju, kas attiecas uz mūsu ķermeņa formu, veidu un funkcijām, nosaka gēnu kopums. Gēns ir stingri noteikta DNS molekulas sadaļa. Tas sastāv no nemainītas nukleotīdu secības. Turklāt gēnu stingri nosaka ne tikai tā sastāvs, bet arī tā atrašanās vieta attiecībā pret citām ķēdes daļām.
Ribonukleīnskābe un tās loma olbaltumvielu sintēzē
Papildus DNS ir arī citi nukleīnskābju veidi - kurjers, transports un ribosomu RNS (ribonukleīnskābe). RNS ķēdes ir daudz mazākas un īsākas, kas ļauj tām iekļūt kodola membrānā.
RNS molekula ir arī biopolimērs. Tās strukturālie fragmenti ir līdzīgi tiem, kas ir daļa no DNS, ar nelielu izņēmumu no saharīda (riboze dezoksiribozes vietā). Ir četru veidu slāpekļa bāzes: mums pazīstamās A, G, C un uracils (U) timīna vietā. Augšējā attēlā tas viss skaidri redzams.
DNS makromolekula spēj pārraidīt informāciju uz RNS nesavītā veidā. Spirāles attīšana notiek ar īpaša enzīma palīdzību, kas sadala dubulto spirāli atsevišķās ķēdēs - kā rāvējslēdzēja slēdzenes pusēs.
Tajā pašā laikā paralēli DNS ķēdei tiek izveidota komplementāra RNS ķēde. Pēc informācijas kopēšanas un nokļūšanas no kodola šūnas vidē RNS ķēde uzsāk gēna kodētā proteīna sintēzes procesus. Olbaltumvielu sintēze notiek īpašās šūnu organellās – ribosomās.
Ribosoma, nolasot ķēdi, nosaka, kādā secībā aminoskābes jāsavieno viena pēc otras - kā informācija tiek nolasīta RNS. Tad sintezētā aminoskābju ķēde iegūst noteiktu 3D formu.
Šī apjomīgā strukturālā molekula ir proteīns, kas spēj veikt kodētās fermentu, hormonu, receptoru un būvmateriālu funkcijas.
secinājumus
Jebkurai dzīvai būtnei tas ir proteīns (olbaltumviela), kas ir katra gēna gala produkts. Tieši olbaltumvielas nosaka visas mūsu šūnās šifrētās formas, īpašības un īpašības.
Cienījamie emuāra lasītāji, vai jūs zināt, kur atrodas DNS, atstājiet komentārus vai atsauksmes, kuras vēlaties uzzināt. Kādam tas būs ļoti noderīgi!