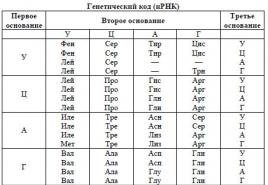
Keemilistes reaktsioonides on süsinik. Süsiniku keemilised omadused
Üksuse funktsioon
6 s 1s 2 2s 2 2p 2
Isotoobid: 12 C (98,892%); 13 C (1,108%); 14 C (radioaktiivne)
Clarki maapõues on 0,48 massiprotsenti. Leiu vormid:
vabas vormis (kivisüsi, teemandid);
karbonaatide (CaCO3, MgC03 jne) koostises;
põlevate mineraalide (kivisüsi, nafta, gaas) koostises;
cO 2 vormis atmosfääris (0,03 mahuprotsenti);
ookeanides - anioonide HCO 3 kujul -;
elusaine koostises (-18% süsinikku).
Süsinikuühendite keemia on peamiselt orgaaniline keemia. Anorgaanilise keemia käigus uuritakse järgmisi C-sisaldusega aineid: vaba süsinik, oksiidid (CO ja CO 2), süsihape, karbonaadid ja vesinikkarbonaadid.
Vaba süsinik. Allotroopia.
Vabas olekus moodustab süsinik 3 allotroopset modifikatsiooni: teemant, grafiit ja kunstlikult toodetud karbiin. Need süsiniku modifikatsioonid erinevad kristalli keemilise struktuuri ja füüsikaliste omaduste poolest.
Teemant
Teemantkristallides on iga süsinikuaatom tugevate kovalentsete sidemete abil seotud nelja teisega, mis asuvad selle ümber võrdsetel kaugustel.
Kõik süsinikuaatomid on sp 3 hübridisatsiooni olekus. Teemandi aatomkristallvõrel on tetraedriline struktuur.
Teemant on värvitu, läbipaistev, väga kerge murdumisvõimega aine. Sellel on kõigi teadaolevate ainete seas kõrgeim kõvadus. Teemant on habras, tulekindel, juhib halvasti soojust ja elektrivoolu. Väikesed vahemaad külgnevate süsinikuaatomite vahel (0,154 nm) põhjustavad teemandi üsna suure tiheduse (3,5 g / cm 3).
Grafiit
Grafiidi kristallvõres on iga süsinikuaatom sp2 hübridisatsiooni olekus ja moodustab samas kihis asuvad kolm tugevat kovalentset sidet süsinikuaatomitega. Nende ahelate moodustamises osalevad iga aatomi kolm elektroni, süsinik, ja neljas valentselektron moodustab л-sidemeid ja on suhteliselt vabad (liikuvad). Need määravad grafiidi elektrilise ja soojusjuhtivuse.
Samal tasapinnal asuvate külgnevate süsinikuaatomite vahelise kovalentse sideme pikkus on 0,152 nm ja C-aatomite vaheline kaugus erinevates kihtides on 2,5 korda suurem, seega on nendevahelised sidemed nõrgad.

Grafiit - läbipaistmatu, pehme, rasvane ja halli-musta värvi metalliline läige; juhib hästi soojust ja elektrivoolu. Grafiidil on teemandiga võrreldes väiksem tihedus, see jaguneb kergesti õhukesteks helvesteks.
Peenkristallilise grafiidi ebakorrektne struktuur põhineb amorfse süsiniku eri vormide struktuuril, millest olulisemad on koks, pruunid ja kõvad söed, tahma, aktiveeritud (aktiivne) süsinik.
Karabiin
See süsiniku allotroopne modifikatsioon saadakse atsetüleeni katalüütilise oksüdeerimise (dehüdropolükondensatsiooni) abil. Carbin on ahelpolümeer, millel on kaks vormi:
C \u003d C-C \u003d C -... ja ... \u003d C \u003d C \u003d C \u003d
Carbinal on pooljuhtide omadused.
Süsiniku keemilised omadused
Tavalistel temperatuuridel on mõlemad süsiniku modifikatsioonid (teemant ja grafiit) keemiliselt inertsed. Grafiidi peenkristallilised vormid - koks, tahma, aktiivsüsi - on reaktiivsemad, kuid reeglina pärast nende eelkuumutamist kõrgele temperatuurile.
C - aktiivne redutseerija:
1. Koostoime hapnikuga
С + O 2 \u003d СО 2 + 393,5 kJ (üle O 2)
2C + O 2 \u003d 2CO + 221 kJ (O 2 puudumisega)
Söe põletamine on üks olulisemaid energiaallikaid.
2. Koostoime fluori ja väävliga.
C + 2F2 \u003d CF4 süsiniktetrafluoriid
C + 2S \u003d CS2 süsinikdisulfiid
3. Koks on üks olulisemaid redutseerivaid aineid, mida tööstuses kasutatakse. Metallurgias kasutatakse seda metallide saamiseks oksiididest, näiteks:
ZS + Fe203 \u003d 2Fe + ZSO
C + ZnO \u003d Zn + CO
4. Süsiniku koostoimel leeliste ja leelismuldmetallide oksiididega moodustab redutseeritud metall koos süsinikuga karbiidi. Näiteks: ЗС + CaО \u003d CaС 2 + СО kaltsiumkarbiid
5. Koksi kasutatakse ka räni tootmiseks:
2C + Si02 \u003d Si + 2CO
6. Koksi liiaga moodustatakse ränikarbiidi (carborundum) SiC.
"Veegaasi" saamine (tahkete kütuste gaasistamine)
Veeauru juhtides läbi kuuma kivisöe saadakse CO ja H 2 põlev segu, mida nimetatakse vesigaasiks:
C + H20 \u003d CO + H2
7. Reaktsioonid oksüdeerivate hapetega.
Aktiveeritud või süsi kuumutamisel redutseerib kontsentreeritud hapetest NO 3 - ja SO 4 2-anioonid:
С + 4HNO 3 \u003d СО 2 + 4NO 2 + 2Н 2 О
С + 2H 2SO 4 \u003d СО 2 + 2SO 2 + 2Н 2 О
8. Reaktsioonid sulatatud leelismetalli nitraatidega
KNO 3 ja NaNO 3 sulades põleb purustatud kivisüsi intensiivselt pimestava leegi moodustumisega:
5С + 4KNO 3 \u003d 2К 2 СО 3 + ЗСO 2 + 2N 2
C - madala aktiivsusega oksüdeerija:
1. Aktiivsete metallidega soolalaadsete karbiidide moodustumine.
Süsiniku mittemetalliliste omaduste oluline nõrgenemine väljendub selles, et selle funktsioon oksüdeeriva ainena avaldub palju vähem kui redutseerimise funktsioonid.
2. Ainult reaktsioonides aktiivsete metallidega süsinikuaatomid liiguvad negatiivselt laetud ioonideks C -4 ja (C \u003d C) 2-, moodustades soolataolisi karbiide:
ZS + 4Al \u003d Al 4 C 3 alumiiniumkarbiid
2C + Ca \u003d CaC2 kaltsiumkarbiid
3. Ioon tüüpi karbiidid on väga ebastabiilsed ühendid, nad lagunevad happete ja vee mõjul kergesti, mis näitab negatiivselt laetud süsiniku anioonide ebastabiilsust:
Al4C3 + 12H20 \u003d CHF4 + 4Al (OH) 3
CaC2 + 2H20 \u003d C2H2 + Ca (OH) 2
4. Kovalentsete ühendite moodustumine metallidega
Süsiniku ja siirdemetallide segude sulatamisel moodustuvad karbiidid peamiselt kovalentse sidemega. Nende molekulid on varieeruva koostisega ja ained tervikuna on sulamite lähedal. Sellised karbiidid on väga stabiilsed, nad on vee, hapete, leeliste ja paljude muude reagentide suhtes keemiliselt inertsed.
5. Koostoime vesinikuga
Kõrge T ja P juures ühendab süsinik nikkelkatalüsaatori juuresolekul vesinikuga:
C + 2HH2 → CHH4
Reaktsioon on väga pöörduv ja sellel puudub praktiline tähendus.
Vaba süsinik on tüüpiline redutseerija. Kui hapnik oksüdeeritakse õhu ülejäägis, muutub see vingugaasiks (IV):
milles puudub süsinikmonooksiid (II):
Mõlemad reaktsioonid on väga eksotermilised.
Süsiniku kuumutamisel vingugaasi (IV) atmosfääris moodustub vingugaas:
Süsinik taastab nende oksiididest palju metalle:
Nii toimuvad reaktsioonid kaadmiumi, vase ja pliioksiididega. Süsiniku interaktsioonis leelismuldmetallide, alumiiniumi ja mõnede teiste metallide oksiididega moodustuvad karbiidid:

Seda seletatakse asjaoluga, et aktiivsed metallid on tugevamad redutseerijad kui süsinik, seetõttu oksüdeeruvad moodustunud metallid kuumutamisel süsiniku liigiga:

Süsinikoksiid (II).
Süsiniku mittetäieliku oksüdeerimisega moodustub vingugaas (II) CO - vingugaas. See on vees halvasti lahustuv. Süsiniku 2+ formaalne oksüdatsiooni olek ei kajasta CO molekuli struktuuri.
CO-molekulis on lisaks kaksiksidemele, mis on moodustatud süsiniku elektronide ja hapniku sotsialiseerumisel, veel üks kolmas side (noolega näidatud), mille moodustab doonori-vastuvõtja mehhanism üksiku hapniku elektronide paari tõttu
Selles suhtes on CO molekul äärmiselt tugev. Süsinikmonooksiid (II) moodustab soola, mis ei moodusta soola ja ei interakteeru normaaltingimustes vee, hapete ja leelistega. Kõrgendatud temperatuuridel on see kalduvus lisamisele ja redoksreaktsioonidele. Õhus põleb CO sinise leegiga:
See taastab metalle nende oksiididest:
![]()
Kiirguse mõjul otsese päikesevalguse käes või katalüsaatorite juuresolekul ühendab CO fosgeeni - äärmiselt mürgise gaasi - moodustumist:
Koos paljude metallidega moodustab CO lenduvaid karbonüüle:
Kovalentsed sidemed nikkelkarbonüülmolekulis moodustatakse doonori-aktseptori mehhanismi abil ja elektronide tihedus nihkub süsinikuaatomilt nikli aatomini. Negatiivse laengu suurenemine metalli aatomis kompenseeritakse selle d-elektronide osalemisega sidemes, seetõttu on metalli oksüdatsiooni olek 0. Kuumutamisel lagunevad metalli karbonüülid metalli ja süsinikmonooksiidiks (II), mida kasutatakse kõrge puhtusastmega metallide saamiseks.
Looduses vingugaasi (II) praktiliselt ei esine. See võib moodustuda sipelghappe dehüdratsiooni ajal (valmistamise laboratoorne meetod):
Viimase puhtalt formaalse muundamise põhjal võib CO-d käsitleda sipelghappe anhüdriidina. Seda kinnitab järgmine reaktsioon, mis toimub siis, kui CO juhitakse kõrgsurvel leelisulatusse:
Süsinikoksiid (IV) ja süsihape. Süsinikoksiid (IV) on süsinikanhüdriid ja sellel on kõik happeoksiidide omadused (vt § 8).
Vees lahustumisel moodustub osaliselt süsihape, samas kui lahuses on järgmine tasakaal.
süsinikuühendid halogeenidega. U. G. peetakse tavaliselt süsivesinike derivaatideks, milles vesinik on täielikult asendatud halogeeniga.
Lihtsamad U. G. on tetrahaliidid üldvalemiga CX4, mille molekulidel on tetraeedriline struktuur vahemaadega С-F, С-Сl, С-Br ja С-I: (Å) 1,36; 1,76; 1,94; 2.12 ja siduvad energiad ( kJ / mol): 487; 340: 285; 214 või sisse kcal / mol 116; 81; 68; 51. Tavalistes tingimustes on CF4 gaas (t kip -128 ° C), CCl4 on vedel (t pl - 22,9 ° C, t kip 76,8 ° C), CBr 4 ja Cl 4 on tahked ained ( t pl 93,7 ja 171 ° C). Kõik tetrahaliidid on vees praktiliselt lahustumatud ja orgaanilistes lahustites lahustuvad. Kooskõlas sidumisenergia vähenemisega väheneb CX4 stabiilsus ja fluori üleviimisel joodile suureneb keemiline aktiivsus. CF 4 ja CCl 4 on vastupidavad kuumusele ja õhu, valguse, hapete toimele. Cl 4 laguneb kuumutamisel kergesti. Ainult CF 4 saab otse elementide koostoimel. Üks CCl4 ja CBr4 sünteesi meetodeid on CS2 reaktsioon halogeenidega. Cl4 saadakse CCl4 reageerimisel alumiiniumi, vismuti ja teiste metallide jodiididega. Süsiniktetrahaliididest on kõige olulisem süsiniktetrakloriid. Tuntud on ka segatud USA, näiteks CClF3, CCBr2CI2, C2Br2F4. Paljusid U. G. kasutatakse laialdaselt erinevates tööstusharudes, näiteks difluorodiklorometaan CCl 2 F 2 ja triklorofluorometaan CCl 3 F külmutusagensitena külmutusseadmetes (freoonid), tetrafluoroetüleen C2F4 ja trifluorokloroetüleen C 2 ClF 3 - monomeerid fluoroplastide tootmisel (vt Fluoroplastid), heksakloroetaan C 2 Cl 6 - kamperisendajad, mõned fluorokloori sisaldavad U. - sünteetiliste õlide komponendid (vt Sünteetilised õlid).
Lit .: Akhmetov N.S., Anorganic Chemistry, 2. trükk, M., 1975.
B. A. Popovkin.
- - СО, muuli. m 28,01; gaas ilma värvi ja lõhnata ...
Keemiline entsüklopeedia
- - COS, öeldakse. m 60,076; värvitu madala lõhnaga gaas ...
Keemiline entsüklopeedia
- - CO2, süsinikku sisaldavate ühendite oksüdeerumisprodukt ...
Ökoloogiline sõnaraamat
- - süsiniku ringlus biosfääris. See on keeruline sündmuste ahel ...
Teaduslik ja tehniline entsüklopeediline sõnastik
- - vaata süsinikku ...
- - kem. halogeenühendid muude elementidega ...
Looduslugu. entsüklopeediline sõnaraamat
- - süsiniku ja hapniku segu, mis moodustub kehas orgaaniliste hapete dekarboksüleerimise tagajärjel ja kõigi orgaaniliste ainete oksüdeerimise lõppsaadusena ...
Suur meditsiiniline sõnastik
- - orgaaniliste ühendite mittetäielikul põlemisel tekkiv värvitu ja lõhnatu gaas ...
Suur meditsiiniline sõnastik
- - protsess, mis algab ökosüsteemides taimede tarbimisega õhust CO2 fotosünteesi käigus. Seejärel jõuab osa süsinikust loomade ja mikroorganismide fütomassiga ...
Ökoloogiline sõnaraamat
- - halogeenühendid koos teiste elementidega; mida looduses leidub mineraalide kujul, on suur praktilisus. väärtus ...
Suur entsüklopeediline polütehniline sõnaraamat
- - või süsivesikud. - Juba Lavoisier märkis, et tavalises suhkrus, mis on süsiniku, vesiniku ja hapniku segu, on kahe viimase elemendi suhe peaaegu sama kui vees ...
Entsüklopeediline sõnaraamat Brockhausi ja Euphroni kohta
- - karbonüülsulfiid, COS, tuleohtlik värvuse ja lõhnata gaas. Vedeldub temperatuuril -50,2 ° С, kõveneb temperatuuril -138,2 ° С. S. kell. lahustub süsinikdisulfiidis, tolueenis, alkoholis ...
Suur Nõukogude Entsüklopeedia
- - halogeenide keemilised ühendid koos teiste elementidega ...
Suur entsüklopeediline sõnaraamat
- - halogeniidid pl - Halogeenühendid koos teiste elementidega
Efraimi selgitav sõnaraamat
- - halogeen on "id, s, ühik h ..."
Vene õigekeelsussõnaraamat
- - halogeenühendi halogeniidid koos teiste elementidega on looduses mineraalide kujul; on suure praktilise tähtsusega ...
Vene keele võõrsõnade sõnastik
Raamatutes "süsinikhalogeniidid"
Fosforhalogeniidid
Raamatust Narkootikumid ja mürgid [psühhedeelilised ja mürgised ained, mürgised loomad ja taimed] autor Petrov Vassili IvanovitšFosforhalogeniidid Fosforhape Hapnik on terava lõhnaga vedelik. Suitsetab õhus. Hüdrolüüsub veega vesinikkloriid- ja fosforhappe moodustumisel. Väga lenduv. Agressiivne. Fosfortrikloriid on sööbiv, ebastabiilne vedelik. Väga lenduv, suits peal
Süsiniku tüüp
Raamatust Filosoofi homöopaatia kivi autor Simeonova Natalja KonstantinovnaSüsiniku tüüp Süsiniku tüüp on patsientide seas kõige tavalisem, mis pole juhuslik. Süsinik on orgaanilise elu keskne element ja kõik ained jagunevad orgaanilisteks ja anorgaanilisteks, sõltuvalt süsiniku olemasolust või puudumisest nende koostises.
2. Süsiniku elektrokeemia
Raamatust Füüsikaline keemia: loengu märkmed autor Berezovchuk AV2. Süsiniku elektrokeemia Praegu kasutatakse süsinikku tänu oma kihilisele grafiidi kujulisele struktuurile grafiidi interkalatsiooniühendi sünteesiks, mis on omakorda leidnud rakendust liitiumvooluallikas (aku), ja seda kasutatakse teaduses,
SÜSIVE KEEMILISED OMADUSED
Süsinik - passiivne, reageerib ainult fluoriga külmas; keemiline aktiivsus ilmneb kõrgel temperatuuril.
Memo! "Keemilised omadused"
|
C on redutseerija С 0 - 4 е - → С +4 või С 0 - 2 е - → С +2 |
C - oksüdeerija C 0 + 4 e - → C -4 |
|
1) hapnikuga C 0 + O 2 t ˚ C → süsinikdioksiid Kogemus hapnikuvaeguse korral põhjustab mittetäielik põlemine vingugaasi moodustumist: 2C 0 + O 2 t ˚ C → 2C + 20 2) fluoriidiga C + 2F2 → CF4 3) auruga C 0 + H 2 O t ° C → C + 2 O + H 2 vesigaas 4) metallioksiididega C +Mina x Oi = CO 2 + Mina C 0 + 2CuO t˚C → 2Cu + C +4 O2 5) hapetega - oksüdeerivad ained: C 0 + 2 H2S04 (konts.) → C + 4 O 2 + 2 SO 2 + 2 H 2 O С 0 + 4 HNO3 (konts.) → С +4 O 2 + 4 NO 2 + 2 H 2 O |
1) moodustab mõne metalliga karbiide 4 Al + 3 C 0 t ˚ C → Al 4 C 3 -4 Ca + 2 C 0 t ˚ C → CaC 2 -1 2) vesinikuga C 0 + 2H2 t˚C → CH4 |
Adsorptsioon
Vastupidine protsess on nende imendunud ainete eraldumine - desorptsioon.
Adsorptsiooni rakendus
Puhastamine lisanditest (suhkru tootmisel jms), hingamisteede organite (gaasimaskide) kaitseks, meditsiinis (Karboleni tabletid) jne.
Süsiniku pealekandmine
Teemante kasutatakse laialdaselt kivimite lõikamiseks ja eriti kõvade materjalide lihvimiseks. Ehted on lõigatud teemantidest. Grafiiti kasutatakse inertsete elektroodide ja pliiatsijuhtide valmistamiseks. Segus tehniliste õlidega määrdeainetena. Sulavad tiiglid valmistatakse grafiidi ja savi segust. Grafiiti kasutatakse tuumatööstuses neutronide absorbeerijana.
Koksi kasutatakse metallurgias redutseerijana. Puusüsi - sepaahjudes püssirohu tootmiseks (75% KNO 3 + 13% C + 12% S), gaaside imendumiseks (adsorptsioon), aga ka igapäevaelus. Tahma kasutatakse kummist täiteainena mustade trükivärvide - trükivärvi ja ripsmetuši - valmistamiseks, samuti kuivades galvaanilistes kambrites. Klaasist süsinikku kasutatakse väga agressiivses keskkonnas kasutatavate seadmete tootmiseks, samuti lennunduses ja astronautikas.
Aktiivsüsi neelab gaasidest ja vedelikest kahjulikke aineid: neid täidetakse gaasimaskide, puhastussüsteemidega, seda kasutatakse meditsiinis mürgituse jaoks.
SÜSINIK
Puusüsi
- mikropoorne kõrge süsinikusisaldusega toode, mis tuleneb puidu lagunemisest ilma õhu juurdepääsuta. Seda kasutatakse kristalse räni, süsinikdisulfiidi, mustade ja värviliste metallide, aktiivsöe jt, aga ka majapidamises kasutatava kütuse (eriline põlemissoojus 31,5-34 MJ / kg) tootmisel.

LÖÖGITÖÖD
Nr 1. Lõpetage reaktsioonivõrrandid, koostage elektrooniline kaal, näidake iga reaktsiooni oksüdeerijat ja redutseerijat:
C + O2 (log) \u003d
C + O 2 (defitsiit) \u003d
C + H2 \u003d
C + Ca \u003d
C + Al \u003d
Keemilised omadused:Tavalistel temperatuuridel on süsinik keemiliselt inertne, piisavalt kõrgel - paljude teiste elementidega - ja sellel on tugevad redutseerivad omadused. Erinevate süsinikuvormide keemiline aktiivsus väheneb järjest: amorfne süsinik, grafiit, teemant, need süttivad õhus vastavalt temperatuuridel vastavalt 300–500 ° C, 600–700 ° C ja 850–1000 ° C. Oksüdeerumisseisundid +4 (nt CO 2), −4 (näiteks CH4), harva +2 (СО, metallkarbonüülid), +3 (C2N2); elektronide afiinsus 1,27 eV; ionisatsiooni energia järjestikuse ülemineku korral C0-st C4 + -ni on vastavalt 11,2604, 24,383, 47,871 ja 64,19 eV.
Kolm kõige kuulsamat vingugaas:
1) vingugaas CO (See on värvitu gaas, millel pole maitset ega lõhna. Põlev. Nn "vingugaasi lõhn" on tegelikult orgaaniliste lisandite lõhn.)
2) süsinikdioksiid CO 2 (Mittetoksiline, kuid ei toeta hingamist. Suur kontsentratsioon õhus põhjustab lämbumist. Samuti on ohtlik süsihappegaasi puudumine. Loomade süsinikdioksiidil on ka füsioloogiline tähtsus, näiteks osaleb veresoonte toonuse reguleerimises)
3) süsinikdioksiid C 3 O 2 (mürgine värviline terava lämbumis- ja lämbumislõhnaga gaas, mis polümeriseerub normaaltingimustes kergesti, et moodustuks vees lahustumatu kollane, punane või lilla värv.)
Mittemetallühendid on oma nimed - metaan, tetrafluorometaan.
Tooted põletamine süsinik hapnikus on CO ja CO 2 (vastavalt süsinikoksiid ja süsinikdioksiid). Ebastabiilne on ka teada. underoksiid süsinik C 3 O 2 (sulamistemperatuur −111 ° C, keemistemperatuur 7 ° C) ja mõned muud oksiidid (näiteks C 12 O 9, C 5 O 2, C 12 O 12). Grafiit ja amorfne süsinik hakkavad reageerima vesinikuga temperatuuril 1200 ° C, fluoriidiga temperatuuril 900 ° C.
Süsinikdioksiid reageerib veega, moodustades nõrga süsihappe - H 2 CO 3, millest moodustuvad soolad - karbonaadid. Magneesiumis on kõige laialdasemalt levinud magneesiumi kaltsiumkarbonaadid (mineraalvormid - kriit, marmor, kaltsiit, lubjakivid jne).
43 küsimus. Räni
Räni (Si) - seisab 3. perioodil, peaalarühma IV rühm on perioodiline. süsteem.
Fiz. Püha-va: Räni on kahes versioonis: amorfne ja kristalne. Amorfne räni - sulatub metallis pruun pulber r-rr. Kristalne. räni - need on tumehallid kristallid, millel on teras läige, kõvad ja haprad. Räni koosneb kolmest isotoobist.
Chem. Püha-va: elektrooniline konfiguratsioon: 1 s 2 2 s 2 2p 6 3 s 2 3p 2 . Räni on mittemetall. Väljastpoolt energiline. U-räni räni on 4 e, mis määrab selle oksüdatsiooni oleku: +4, -4, -2. Valents - 2, 4. Amorfsel räni reaktsioonivõime on suurem kui kristalsel. Tavalistes tingimustes interakteerub see fluoriga: Si + 2F 2 \u003d SiF 4.
Räni interakteerub ainult lämmastik- ja vesinikfluoriidhapete seguga:
See käitub metallidega erinevalt: lahustub hästi sulatatud Zn, Al, Sn, Pb, kuid ei reageeri nendega; räni interakteerub teiste metallisulamitega - Mg, Cu, Fe-ga silikoidide moodustumisel: Si + 2Mg \u003d Mg2Si. Räni põleb hapnikus: Si + O2 \u003d SiO2 (liiv).
Vastuvõtmine:Tasuta räni saab peene valge liiva kaltsineerimisel magneesiumiga, mis keemilises koostises koostis on peaaegu puhas ränioksiid, SiO2 + 2Mg \u003d 2MgO + Si.
Ränidioksiid (II) SiO- vaigune amorfne, normaalsetes tingimustes hapnikukindel. Viitab mitte soola moodustavatele oksiididele. SiO looduses ei esine. Gaasilist räni monoksiidi leiti tähtedevaheliste keskkondade gaasitolmupilvedes ja päikesepistetes. Vastuvõtmine:Ränimonooksiidi saab räni kuumutamisel hapnikuvaeguse all temperatuuril 2Si + O 2 nädalat → 2SiO. Liigse hapniku kuumutamisel moodustub ränioksiid (IV) SiO2: Si + O 2 log → SiO 2.
SiO moodustub ka SiO2 redutseerimisel räni abil kõrgetel temperatuuridel: SiO 2 + Si → 2SiO.
Räni (IV) oksiid SiO2 - värvitu kristallidon kõrge kõvaduse ja tugevusega. Püha-va:See kuulub hapete rühma. oksiidid. Kuumutamisel interakteerub peamisega. oksiidid ja leelised.P-lahustub vesinikfluoriidhappes.SiO2 kuulub klaasi rühma, moodustades oksiide, s.o. See on aldis ülejahutatud sulaklaasi moodustumisele.Üks parimatest dielektrikutest (elektrivool ei juhita). Tal on aatomikristallvõre.
Nitriid on binaarne anorgaaniline aine. keemiline ühend, mis on räni ja lämmastiku Si 3 N 4 ühend. Püha-va:Räninitriidil on hea mehaaniline ja füüsikaline keemia. Teie poolt. Tänu räni nitriidi side tähendab. Ränikarbiidil, periklaasil, forsteriidil jne põhinevate tulekindlate materjalide tööomadused on paranenud.Nitriidide sidumisel põhinevatel tulekindlatel materjalidel on kõrge termiline ja kulumiskindlus, neil on suurepärane vastupidavus lõhenemisele, samuti leeliste, agressiivsete sulade ja metalli aurude mõjudele .
Räni (IV) kloriidräni - värvitu, kem. kassi valem. SiCl 4. Kasutatakse räniorgaaniliste ainete tootmisel. ühendid; Seda kasutatakse suitsukraanide loomiseks. Tehnika. ränitetrakloriid on ette nähtud etüülsilikaatide, aerosilide tootmiseks.
Ränikarbiid - binaarne anorgaaniline Chem. räni ja süsinik-SiC segu. Looduses leidub seda äärmiselt haruldase mineraali - moissaniidi - kujul.
Ränidioksiid või ränidioksiid - stabiilne ühendus Si , looduses laialt levinud. Reageerib koos sulandumisega leeliste, aluseliste oksiididega, moodustades ränihappe soolad - silikaadid. Vastuvõtmine: tööstuses saadakse puhas räni räni dioksiidi redutseerimisel koksiga elektriahjudes: SiO 2 + 2C \u003d Si + 2CO 2.
Laboris saadakse räni valge liiva magneesiumi või alumiiniumiga kaltsineerimise teel:
SiO2 + 2Mg \u003d 2MgO + Si.
3SiO2 + 4Al \u003d Al203 + 3Si.
Räni vormid teile:H2 SiO 3 - meta-räni sellele;H2 Si 2 O 5 - kaks räni selle jaoks.
Looduses olemine: Kvartsmineraal - SiO2. Kvartskristallid on värvitu ja läbipaistva kuusnurkse prisma kujul, mida nimetatakse mäekristalliks. Ametüst - mäekristall, värvitud lisanditega lillas toonis; suitsune topaas on pruunikas; ahhaat ja jaspis - kristalne. kvartsisordid. Amorfset ränidioksiidi on vähem levinud ja see eksisteerib opaalmineraalina. Diatomiit, tripool või kieselguhr (infusooriline maa) on amorfse räni mullased vormid. räni valem - n SiO2?m H2O. Looduses on see peamiselt soolade vormis, vabas vormis. vähesed, näiteks, on eraldatud HSiO (ortosilikoon) ja H2S03 (räni või metasilicon).
Ränihappe saamine:
1) silikaatide interaktsioon on aluseline. metallid komplektidega: Na2 SiO 3 + 2HCl \u003d H2 SiO 3 + 2NaCl;
2) tulekiviga - et yavl. termiliselt ebastabiilne: H2 SiO 3 \u003d H 2 O + SiO 2.
H 2 SiO 3 moodustab kassis üleküllastunud lahuseid. polümerisatsiooni tagajärjel moodustuvad kolloidid. Stabilisaatoreid kasutades saate resistentseid kolloide (soolid). Neid kasutatakse tootmises. Ilma stabilisaatoriteta moodustub kuivatatava räni lahusest geel, mille abil on võimalik saada silikageeli (kasutatakse adsorbendina).
Silikaadid - räni soolad teile. Silikaadid on oma olemuselt levinud, maapõue koosneb enamasti ränidioksiidist ja silikaatidest (maapinnad, vilgukivi, savi, talk jne). Graniit, basalt ja muud kivimid sisaldavad silikaate. Smaragd, topaas, akvamariin - silikaatide kristallid. Lahustuvad ainult naatriumi- ja kaaliumsilikaadid, ülejäänud on lahustumatud. Silikaadid on keerulised. Chem. struktuur: Kaolin Al 2 O 3 ; 2SiO 2 ; 2H 2 O või H 4 Al 2 SiO 9 .
Asbest CaO; 3MgO; 4SiO 2 või CaMgSi 4 O 12 .
Vastuvõtmine: räni oksiidi liitmine leeliste või karbonaatidega.
Lahustuv klaas - naatriumi ja kaaliumi silikaadid. Vedel klaas - aq. kaalium- ja naatriumsilikaatide lahused. Selle kasutamine happekindla tsemendi ja betooni, petrooleumikindlate krohvide, tulekindlate värvide tootmiseks. Aluminosilikaadid - alumiiniumi sisaldavad silikaadid ( päevakivi, vilgukivi). Päevakivid Lisaks räni- ja alumiiniumoksiididele koosnevad need kaaliumi, naatriumi, kaltsiumi oksiididest. Vilgukivist lisaks ränile ja alumiiniumile sisaldavad need ka vesinikku, naatriumi või kaaliumi ning harvemini kaltsiumi, magneesiumi ja rauda. Graniidid ja gneissid (kivimid) - komp. kvartsist, päevakivi ja vilgust. Sarv Maa pinnal asuvad kivimid ja mineraalid interakteeruvad vee ja õhuga, mis põhjustab nende muutumist ja hävimist. Seda protsessi nimetatakse. ilmastik.
Rakendus: silikaatkivimid (graniit), kasutades ehitusmaterjalina silikaadid - toorainena tsemendi, klaasi, keraamika, täiteainete tootmisel; vilgukivi ja asbest - nii elektri- kui ka soojusisolatsioon.