Radioaktive Transformationen von Atomic. Atomkerne drehen.
Art der Lektion
Objektive Lektion:
Studieren Sie weiterhin das Phänomen der Radioaktivität;
Untersuchen Sie radioaktive Transformationen (Verdrängungsregeln und das Gesetz der Erhaltungsgebühr und Massennummern).
Untersuchen Sie grundlegende experimentelle Daten, um die Grundprinzipien der Verwendung der Kernenergie in elementarer Form zu klären.
Aufgaben:
bildung
entwicklung
lehrreich
Herunterladen:
Vorschau:
Die Lektion zum Thema "radioaktive Transformationen von Atomkern".
Physik Lehrer I Kategorie Medvedev Galina Lvovna
Art der Lektion : Lektion, die neues Material studieren
Ziele Lektion:
Studieren Sie weiterhin das Phänomen der Radioaktivität;
Untersuchen Sie radioaktive Transformationen (Verdrängungsregeln und das Gesetz der Erhaltungsgebühr und Massennummern).
Untersuchen Sie grundlegende experimentelle Daten, um die Grundprinzipien der Verwendung der Kernenergie in elementarer Form zu klären.
Aufgaben :
bildung - Erkenntnis der Studierenden mit den Regeln der Verschiebung; Erweiterung der Ideen der Schüler über das physische Bild der Welt;
entwicklung - um die Fähigkeiten der physischen Natur der Radioaktivität, radioaktive Transformationen, Offset-Regeln herauszufinden periodensystem chemische Elemente; Setzen Sie die Entwicklung von Fähigkeiten fort, um mit Tabellen und Systemen zu arbeiten; Setzen Sie die Entwicklung von Arbeitsfähigkeiten fort: Allokation der Haupt-, Ausstellung des Materials, der Entwicklung der Aufmerksamkeit, die Fähigkeit, die Fakten zu vergleichen, zu analysieren und zusammenzufassen, zur Entwicklung des kritischen Denkens beizutragen.
lehrreich - um die Entwicklung der Neugier zu fördern, um die Fähigkeit zu fördern, ihren Standpunkt anzugeben und sein Recht zu verteidigen.
Lektion Zusammenfassung:
Text an die Lektion.
Guten Tag, alle diese auf der heutigen Lektion.
Lehrer: Also sind wir in der zweiten Bühne forschungsarbeit Auf dem Thema "Radioaktivität". Was ist es? Das heißt, heute werden wir radioaktive Transformationen und Verdrängungsregeln studieren. -----Dies ist das Thema unseres Studiums und dementsprechend das Thema der Lektion
Ausrüstung für die Forschung.: MendeleeV-Tisch, Arbeitskarte, Sammlung von Aufgaben, Kreuzworträtsel (eins für zwei).
Lehrer, Epigraph: "Wenn das Phänomen der Radioaktivität offen war, verglich sie einstein mit der Gewinnung von Feuer in der Antike, da er glaubte, dass Feuer und Radioaktivität gleichermaßen große Meilensteine \u200b\u200bin der Geschichte der Zivilisation waren."
Warum hat er das gedacht?
Studenten unserer Klasse führten theoretische Studien durch und hier ist das Ergebnis:
Studentenbotschaft:
- Pierre Curie platzierte eine Ampulle mit Radiumchlorid in einem Kalorimeter. Es wurde von α-, β-, γ-Strahlen absorbiert, und das Kalorimeter wurde aufgrund ihrer Energie erhöht. Curie hat festgestellt, dass 1 g Radium in 1 Stunde etwa 582 J Energie zuweisen. Und diese Energie wird seit einigen Jahren zugewiesen.
- Bildung 4g Gramm Helium wird von der Veröffentlichung derselben Energie wie der Verbrennung von 1,5 bis 2 Tonnen Kohle begleitet.
- Energie, die in 1 g Uran geschlossen wurde, ist gleich der Energie, die während der Verbrennung von 2,5 Tonnen Öl freigesetzt wird.
Während des Tages, Monaten und Jahre änderte sich die Strahlungsintensität nicht deutlich. Es hatte keinen Einfluss auf solche gewöhnlichen Auswirkungen als Erwärmung oder Druckanstieg. Chemische Reaktionen, in denen radioaktive Substanzen eingedrungen sind, beeinflussen auch die Intensität der Strahlung nicht.
Jeder von uns ist nicht nur "unter der Überwachung" der Strahlung nicht willkommen "Nannika", jeder von uns ist ein wenig radioaktiv und von selbst. Strahlungsquellen sind nicht nur außerhalb von uns. Wenn wir trinken, geben wir die Anzahl der Atome von radioaktiven Substanzen im Körper ein, dass das Gleiche passiert, wenn wir essen. Wenn wir außerdem atmen, kommt unser Körper wieder aus der Luft, alles, was radioaktiv fähig ist, vielleicht das radioaktive Isotop von C-14-Kohlenstoff, kann Kaliumk-40 oder ein anderes Isotop sein.
Lehrer: Wo wird diese Anzahl von Radioaktivität aufgenommen, die ständig um und in uns präsentieren?
Studenten sammeln:
Nach nuklearer Geophysik in der Natur gibt es ziemlich viele Quellen der natürlichen Radioaktivität. In Rassen erdkrusteIm Durchschnitt entfallen eine Tonne Felsen für 2,5 - 3 Gramm Uran, 10 - 13 g Thorium, 15-25 g Kalium. Richtig, radioaktiv k-40 beträgt nur bis zu 3 Milligramm pro Tonne. All diese Fülle von radioaktiven, instabilen Kernen zerfällt kontinuierlich, spontan spontan. Jede Minute in 1 kg Substanz der Erde-Rocks zerfällt durchschnittlich 60.000 K-40-Kerne, 15.000 Kerne des RB-87-Isotops, 2400 Kernen von TH-232, 2200 U-238-Kernen. Die volle Menge an natürlicher Radioaktivität beträgt etwa 200 Tausend Zerklas pro Minute. Wissen Sie, dass die natürliche Radioaktivität bei Männern und Frauen unterschiedlich ist? Erläuterung dieser Tatsache ist offensichtlich - weiche und dichte Gewebe haben eine andere Struktur, unterscheiden sich anders und sammelt radioaktive Substanzen..
PROBLEM: Welche Gleichungen, Regeln, Gesetze beschreiben die Daten der Reaktion der Dekontaminationen von Substanzen?
Lehrer: Welches Problem werden wir mit Ihnen lösen? Welche Weise, um das Problem zu lösen, bieten Sie an?
Studenten arbeiten und machen ihre Annahmen.
Pupil antwortet:
Lösung Wege:
Student 1: Erinnern Sie sich an die grundlegenden Definitionen und Eigenschaften radioaktiver Strahlung.
Student 2: Verwenden der vorgeschlagenen Reaktionsgleichungen (auf der Karte), erhalten Sie allgemeine Gleichungen. Für radioaktive Transformationsreaktionen mit einer MendeleeV-Tabelle formulieren Sie allgemeine Regeln für die Verschiebung von Alpha und Beta-Zerfällen.
Student 3. : Sichern Sie das gewonnene Wissen, um sie für weitere Forschungen anzuwenden (Probleme lösen).
Lehrer.
Okay. Wir werden zur Lösung gehen.
Bühne 1. Arbeit mit Karten. Sie erhalten Fragen, für die Sie schriftlich geben solltenantworten.
Fünf Fragen - fünf richtige Antworten. Wir bewerten auf dem Fünf-Punkt-System.
(Geben Sie Zeit, um die Antworten zu arbeiten, dann führen wir die Folien durch, ich mache eine Bewertung selbst, nach den Kriterien).
- Radioaktivität ist ...
- α-Strahlen ist ...
- β-Strahlen ist ....
- γ-Strahlung - ....
- Formulieren Sie das Gesetz der Erhaltung der Lade- und Massennummern.
Antworten und Punkte:
Stufe 2. Lehrer.
Wir arbeiten unabhängig und an der Tafel (3 Buchhaltung).
A) Schreiben Sie die Gleichungen von Reaktionen, die von der Trennung von Alphateilchen begleitet werden.
2. Schreiben Sie eine Reaktion von α-Zerfall von Uran235 92 U.
3. Isst alpha abfallkern polonium
Lehrer:
Schlussfolgerung Nummer 1:
Als Ergebnis des Alpha-Zerfalls nimmt die Massenzahl der resultierenden Substanz um 4 AH und die Ladungszahl auf 2 Elementarladungen ab.
B) Notieren Sie die Reaktionengleichungen, die von der Freigabe von Beta-Partikeln begleitet werden (3 Buchhaltung an der Tafel).
einer. . Schreiben Sie eine Reaktion β-Zerfall von Plutonium239 94 PU.
2. Schreiben Sie einen Beta-Zerfall von Thorium Isotope
3. Verteilen Sie den β-Zerfall von Curie247 96 cm.
Lehrer: Welchen allgemeinen Ausdruck können wir mit Ihnen schreiben und die entsprechende Schlussfolgerung machen?
Schlussfolgerung Nummer 2:
Infolge des Beta-Zerfalls ändert sich die Massenzahl der resultierenden Substanz nicht, und die Ladungsnummer erhöht sich um 1 Elementarladung.
Stufe 3.
Lehrer: Nach einem Zeitpunkt, nachdem diese Ausdrücke erhalten wurden, Rutinfords Student Frederick Soddy,schlug die Regeln der Verdrängung für radioaktive Abfälle vorMit der Hilfe der resultierenden Substanzen finden Sie in der Mendeleev-Tabelle. Schauen wir uns die von uns erhaltenen Gleichungen an.
FRAGE:
einer). Welches Muster wird mit Alpha-Zerfall beobachtet?
Antwort: Mit Alpha-Zerfall verschiebt sich die resultierende Substanz zwei Zellen mit dem Anfang des Mendeleev-Tischs.
2). Welches Muster wird mit Beta-Zerfall beobachtet?
Antwort: Mit Beta-Zerfall verschiebt sich die resultierende Substanz eine Zelle bis zum Ende der Mendeleev-Tabelle.
Stufe 4.
Lehrer. : Und die letzte Phase unserer Tätigkeit heute:
Unabhängige Arbeit (auf der Sammlung von Aufgaben von Lukashika):
Variante 1.
Option 2.
Prüfen: auf dem Vorstand alleine.
Kriterien für die Bewertung:
"5" - Durch Aufgaben ausgeführt
"4" - 2 Aufgaben wurden durchgeführt
"3" - 1 Task wird ausgeführt.
Selbsteinschätzung für die Lektion:
Wenn die Zeit bleibt:
Frage an den Unterricht:
Welches Thema haben Sie heute in der Lektion studiert? Wenn Sie das Kreuzworträtsel erraten, lernen Sie den Namen des radioaktiven Strahlungsausgabeprozesses.
1. Welche Wissenschaftler entdeckten Radioaktivitätsphänomen?
2. Parteisubstanz.
3. Nachname des Wissenschaftlers, der die Zusammensetzung der radioaktiven Strahlung bestimmt hat.
4. Die Kerne mit der gleichen Anzahl von Protonen, aber mit verschiedenen Neutronenzahlen - das ist ...
5. Radioaktives Element, offene Curie-Ehepartner.
6. Isotope Polonia Alpha radioaktiv. Was ist ein Element gebildet?
7. Name einer Frau - ein Wissenschaftler, der geworden ist Nobel-Laureat. zweimal.
8. Was liegt in der Mitte des Atoms?
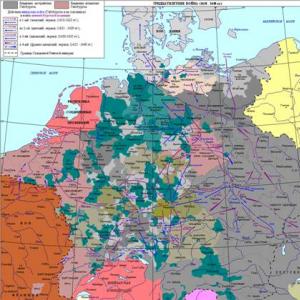
In der vorherigen Lektion diskutierten wir die Frage, die sich auf das Rutherford-Experiment bezieht, wodurch wir jetzt wissen, dass ein Atom ein Planetenmodell ist. So heißt es das Planetenmodell des Atoms. In der Mitte des Kernels gibt es einen massiven positiv aufgeladenen Kern. Und Elektronen drehen sich um ihren Umlaufbahnen um den Kernel um.
Feige. 1. Planetenmodell des Rangefordatoms
Zusammen mit dem Rangeford in den Experimenten nahm die Teilnahme von Frederick Soddy. Soddy ist ein Chemiker, also verbrachte er seine Arbeit genau in Bezug auf die Identifizierung der nach ihren chemischen Eigenschaften erhaltenen Elemente. Es war Soddy, der es geschafft hatte, herauszufinden, was A-Partikel in den Experimenten von Rangeford auf die goldene Platte fiel. Wenn Messungen gemessen wurden, stellte sich heraus, dass die Masse der A-Partikel 4 Atomeinheiten der Masse beträgt, und die Ladung A-Partikel beträgt 2 Elementarladungen. Korrigieren Sie diese Dinge, indem sie eine bestimmte Menge an Teilchen anhäufen, fanden Wissenschaftler heraus, dass diese Partikel in ein chemisches Element-Geliumgas umgewandelt wurden.
Die chemischen Eigenschaften von Helium waren aufgrund dieses Soddrucks bekannt, und argumentierten, dass die Kerne, die A-Partikel sind, die Elektronen von außen erfasst und in neutrale Heliumatome umgewandelt wurden.
In Zukunft zielten die Hauptbemühungen der Wissenschaftler darauf ab, den Kern des Atoms zu studieren. Es wurde klar, dass alle Prozesse, die während radioaktiver Strahlung auftreten, nicht mit einer Elektronenschale auftreten, keine Elektronen, die den Kernel umgeben, sondern mit den Kernen selbst. Es ist in den Kernen, dass einige Transformationen auftreten, wodurch neue chemische Elemente gebildet werden.
Die erste derartige Kette wurde erhalten, um das Radiumelement umzuwandeln, das in den Versuche in der Radioaktivität verwendet wurde, in der Inertgasradon mit emittierenden A-Partikeln; Die Reaktion wird in diesem Fall wie folgt geschrieben:
![]()
Zunächst sind A-Partikel 4 Atomeinheiten Masseneinheiten und doppelte, doppelte Elementarladung und eine positive Ladung. Radias Seriennummer 88, seine Massenzahl beträgt 226, und Radon hat bereits eine Sequenznummer 86, eine Massenzahl 222, und ein Teilchen erscheint. Dies ist der Kern des Heliumatoms. In diesem Fall schreiben wir nur Helium. Seriennummer 2, Massenzahl 4.
Reaktionen, wodurch noch neue chemische Elemente gebildet werden und gleichzeitig neue Strahlung und andere chemische Elemente gebildet werden; kernreaktionen.
Wenn klar wurde, dass radioaktive Prozesse innerhalb des Kerns fortfahren, wandten sich an andere Elemente, nicht nur auf das Radium. Wissenschaftler untersuchen, wissen Wissenschaftler, dass es nicht nur Reaktionen mit Emission, die Strahlung des A-Partikels des Kerns des Heliumatoms, aber auch andere nukleare Reaktionen gibt. Zum Beispiel Reaktionen mit Emission von B-Partikeln. Wir wissen jetzt, dass dies Elektronen sind. In diesem Fall ist das neue chemische Element jeweils ebenfalls ausgebildet neue PartikelDieses B-Partikel ist ein Elektron. Von besonderem Interesse in diesem Fall sind alle chemischen Elemente, in denen die Sequenznummer größer als 83 ist.
So können Sie die sogenannte Formulierung formulieren. Sortenregeln oder Offset-Regeln für radioaktive Transformationen:
. Mit dem Alpha-Zerfall erfolgt eine Abnahme der Sequenznummer des Elements für 2 und eine Abnahme des Atomgewichts um 4.
Feige. 2. Alpha-Zerfall.
Im Falle eines Beta-Zerfalls tritt eine Erhöhung der Ordnungszahl an 1 auf, während sich das Atomgewicht nicht ändert.

Feige. 3. Beta-Zerfall.
Liste der zusätzlichen Literatur
- Bronstein M.P. Atome und Elektronen. "Vieh" KVANT ". Vol. 1. M.: Wissenschaft, 1980
- Kikooin Ik, Kikooin A.K. Physik: Lehrbuch für Note 9 weiterführende Schule. M.: "Erleuchtung"
- Khigorodsky A.i. Physik für alle. Photonen und Kernel. Buchen Sie 4. M.: Wissenschaft
- Myakyshev g.ya., Sinyakova a.z. Physik. Optics Quantum Physik. Grad 11: Tutorial für intentierstudium Physik. M.: Tropfen
- Rutherford E. ausgewählt wissenschaftliche Arbeiten. Radioaktivität. M.: Wissenschaft.
- Rutherford E. ausgewählte wissenschaftliche Arbeiten. Die Struktur des Atoms und der künstlichen Transformation der Elemente. M.: Wissenschaft.
Geschichte Öffnung
Bereits 1903 wurden Physists Rutherford und Soddy gefunden, dass mit radioaktivem Alpha-Zerfall ein Radiumelement in ein anderes chemisches Element radoniert. Diese beiden chemischen Elemente haben völlig unterschiedliche Eigenschaften. Radium-Feststoff-, Metall- und Radon-Inertgas. Radium- und Radonatome unterscheiden sich durch Masse, die Anzahl der Elektronen in der Elektronenschale, der Ladung des Kernels. Weitere Studien haben gezeigt, dass in Beta-Zerfall eine Umwandlung einiger chemischer Elemente an andere ist. Im Jahr 1911 schlug Rutherford ein Atommodellatom vor. Die Essenz des Modells war wie folgt: Ein Atom besteht aus einem positiv aufgeladenen Kern und negativ aufgeladener Elektronen, die sich um den Kernel bewegen. Es war logisch, anzunehmen, dass in einem solchen Modell eines Atoms mit radioaktivem Alpha oder Beta-Zerfall eine Änderung des Kerns eines Atoms war, da sich nur die Anzahl der Elektronen ändern könnte, da ein neues chemisches Element erhalten würde, und Das Ion würde das gleiche chemische Element erhalten.
Formular-Zerfall-Bild.
Radium-Alpha-Zerfall wird wie folgt geschrieben:
(226.88) RA -\u003e (222.86) RN + (4.2) Er.
Bild
In der obigen Formel bezeichnet (226,88) RA den Kernel des Radiumatoms (222.86) RN der Kernel des Radonatoms und (4.2) He-Alpha-Partikel oder des Kernels des Heliumatoms.
Bitte beachten Sie, dass die Bezeichnung auch verwendet wird, um den Atomkernel wie für das Atom selbst zu bezeichnen. Wir werden mit Indizes umgehen. Die Nummer, die oben steht, wird als Massenzahl bezeichnet. Die Massenzahl des Atomkerns zeigt, wie viele atomare Einheiten der Masse in der Masse des Kerns dieses Atoms enthalten sind. Die Anzahl wird nachstehend aufgezeichnet, wird als geladene Gebühr bezeichnet. Die Ladungszahl des Atomkerns zeigt, wie viele elementare elektrische Ladungen in der Ladung des Kerns dieses Atoms enthalten sind. Massen- und Ladungsnummer sind immer ganze Zahlen und positive Werte. Sie haben keine separate Bezeichnungeinheit, da sie ausdrücken, wie oft die Masse und die Ladung des Kerns dieses Atoms mehr als einzelne Indikatoren ist.
Die Essenz des Phänomens
Wir werden die Reaktionsgleichung analysieren, die wir für den Alpha-Zerfall des Kerns des Radiumatoms aufgenommen haben.
(226.88) RA -\u003e (222.86) RN + (4.2) Er.
Wir haben, dass der Kernel des Radiumatoms während der Strahlung des Alpha-Partikels 4 Masseneinheiten und zwei Elementarladungen verloren hat und gleichzeitig in den Kernel des Radonatoms umgewandelt wurde. Sie können verfolgen, dass die Gesetze der Aufrechterhaltung einer Massenzahl und der Ladung durchgeführt werden. Mischen Sie separat Massenzahlen und Ladungszahlen der resultierenden zwei Elemente:
Wie Sie sehen, geben sie in Summe die gleichen Indikatoren, die sie einen Radiumatom-Kern hatten. Von all dem oben genannten folgt, dass der Atomkern auch aus einigen Partikeln besteht, dh also aufweist, dh eine komplexe Zusammensetzung aufweist. Und wir können nun die Definition der Radioaktivität klarstellen. Radioaktivität - Die Fähigkeit der Kerne einiger Atome, sich spontan in andere Kerne zu verwandeln, während die Emit-Partikel entsteht.
S.g.kadmensky.
Voronezh State University.
Radioaktivität der Atomkerne: Geschichte, Ergebnisse, neueste Errungenschaften
1996 feierte die körperliche Gemeinschaft das Jahrhundert, seit der Eröffnung der Radioaktivität atomarer Kerne. Diese Entdeckung führte zur Geburt neuer Physik, die die Struktur des Atoms und des Atomkerns verstehen ließ und als Tor zur seltsamen und harmonischen Quantenwelt der elementaren Partikel diente. Wie bei vielen herausragenden Entdeckungen trat die Radioaktivitätserkennung zufällig auf. Anfang 1896 unmittelbar nach der Entdeckung von V.K. Röntgenrahmen-Röntgenrahmen-französischer Physiker Henri Becquer, um die Hypothese über die fluoreszierende Natur der Röntgenstrahlung zu überprüfen, die herausfand, dass das Uran-Kaliumsalz spontan, spontan, ohne äußere Einflüsse, harte Strahlung frisst. Später stellte Becquille heraus, dass dieses Phänomen mit Radioaktivität rief, dh radialer Aktivität ist vollständig mit der Anwesenheit von Uran verbunden, die das erste radioaktive chemische Element wurde. Nach einigen Jahren wurden solche Immobilien in Thoria gefunden, dann Polonium und Radium, Open Marie und Pierre Curie, und in Zukunft alle chemischen Elemente, deren Zahlen mehr als 82 sind. Mit dem Aufkommen von Beschleunigern und Kernreaktoren waren radioaktive Isotope In allen chemischen Elementen erkannt, von denen die meisten praktisch nicht in vivo gefunden werden.
Arten von radioaktiven Transformationen von atomaren Kernen
Analyse der durchdringenden Fähigkeit der radioaktiven Uran-Radiation E. Rutherford entdeckte zwei Komponenten dieser Strahlung: weniger durchdringende, α-Strahlung und durchdringender, eindringender, genauer-Emission. Der dritte Bestandteil der Uranstrahlung, das durchdringendste von allen, wurde später in 1900 dem Villard-Feld entdeckt und wurde von Analogie mit der Rutherford in der Nähe von γ-Strahlung benannt. Rutherford und sein Personal zeigten, dass Radioaktivität mit dem Zusammenbruch von Atomen verbunden ist (viel später klar, dass wir über den Zerfall von Atomkern sprechen), begleitet von der Emission einer bestimmten Art von Strahlung. Diese Schlussfolgerung verursachte einen zerquetschenden Schlag auf das konkrissive, was für Atome, die in der Physik und der Chemie dominierten, unverzichtbar ist.
In nachfolgenden Untersuchungen von Rutinford wurde gezeigt, dass α-Strahlung ein Fluss von α-Partikeln ist, der nicht mehr als ein healner Kern nein ist, und β-Strahlung besteht aus Elektronen. Schließlich erscheint γ-Strahlung als Relativ von Licht- und Röntgenstrahlung und ist ein Fluss der hochfrequenten elektromagnetischen Quanten, der von atomaren Kernen emittiert wird, wenn er sich von angeregten zu niedrigeren Faltzuständen bewegt.
Die Art des β-Zerfalls der Kerne war sehr neugierig. Die Theorie dieses Phänomens wurde erst 1933 ENRICO FERMI erstellt, der die Hypothese von Wolfgang Pauli über die Geburt im β-Zerfall des neutralen Partikels mit einer entspannten Friedensmasse und als Neutrino genannt hatte. Fermi stellte fest, dass β-Zerfall auf eine neue Art der Wechselwirkung von Partikeln in der Natur - "schwaches" Wechselwirkung zurückzuführen ist, und ist mit den Prozessen der Umwandlung im übergeordneten Neutronenkern in ein Proton mit der Emission eines Elektron E - und Antineutrino ( β - -Respad), Proton im Neutron mit der Emission des Positen E + und Neutrinos ν (β + -Respad) sowie mit einer Protonenaufnahme des Atomelektronens und emittierenden Neutrinos ν (elektronischer Griff).
Die vierte Art der Radioaktivität, in Russland 1940 von jungen Physiker G.N. eröffnet. FLEROV und K.A. Petrzhak ist mit der spontanen Aufteilung von Kernen verbunden, in der einige ausreichend schwere Kerne mit ungefähr gleichen Massen in zwei Fragmente zerfallen.
Die Division hat jedoch nicht alle Arten von radioaktiven Transformationen von Atomkernen erschöpft. Ab den 50er Jahren näherte sich die Physik methodisch mit der Entdeckung der Proton-Radioaktivität der Kerne. Damit der Kern, der sich im Hauptstaat befindet, ist notwendig, um Protonen spontan auszusetzen, es ist notwendig, dass die Energie der Protonentrennung aus dem Kernel positiv ist. Es gibt jedoch keine solchen Kerne zu irdischen Bedingungen, und sie mussten künstlich erstellen. Russische Physiker in Dubna waren sehr nahe bei der Erlangung solcher Kerne, aber Protonradioaktivität wurde 1982 von deutschen Physikern in Darmstadt entdeckt, der den leistungsstärksten Beschleuniger von mehrseitigen Ionen verwendete.
1984 eröffneten 1984 unabhängige Gruppen von Wissenschaftlern in England und Russland die Radioaktivität von Cluster von einigen schweren Kernen, die spontan mit Clustern - atomare Atomkerne von 14 bis 34 emittiert wurden.
Auf der Registerkarte. 1 präsentiert die Geschichte der Öffnung verschiedener Arten von Radioaktivität. Ob alle möglichen Arten von radioaktiven Transformationen der Kerne erschöpft sind, Time wird erkennen. In der Zwischenzeit sind die Suchen nach Kernen intensiv weiter, was aus den Hauptzuständen des Neutron-Radioaktivitäts (Neutronenradioaktivität) oder zwei Protonen (zwei terminaler Radioaktivität) emittiert würden.
Tabelle 1. Geschichte der Öffnung verschiedener Arten von Radioaktivität
| Art der Radioaktivität von Kernel | Art der erfassten Strahlung | Entdeckungsjahr. | Autoren öffnen sich |
| Radioaktivität von Atomkern | Strahlung | 1896 | A. Becquer. |
| Alpha-Zerfall. | 4 ne. | 1898 | E. RUTFORD. |
| Beta-Zerfall. | e - | 1898 | E. RUTFORD. |
| Gamma-Zerfall | γ -Quantum. | 1900 | P. Villard. |
| Spontane Division von Kernel | Zwei Fragmente | 1940 | G.N. Fleroov, K.a. Petrzhak. |
| Proton-Zerfall | p. | 1982 | 3. Hofman usw. |
| Cluster-Zerfall. | 14 C. | 1984 | X. Rose, Jones; D.v. Alexandrov et al. |
Moderne Ideen über Alpha-Zerfall
Alle Arten von radioaktiven Transformationen der Kerne erfüllen das exponentielle Gesetz:
N (t) \u003d n (0) exp (-λt)
wobei n (t) die Anzahl radioaktiver Kerne ist, überlebt von der Zeit t > 0, falls zu der Zeit t \u003d 0 ihre Anzahl n (0) war. Der Wert von λ fällt mit der Wahrscheinlichkeit des Zerfalls des radioaktiven Kerns pro Zeiteinheit zusammen. Dann ist die Zeit t 1/2, als Halbwertszeit genannt, für die die Anzahl der radioaktiven Kerne um zweimal reduziert wird, definiert als
T 1/2 \u003d (ln2) / λ ,.
Die Werte von T 1/2 für α-Emitter variieren in einem weiten Bereich von 10 bis 10 Sekunden bis 10 bis 20 Jahren, abhängig vom Wert der relativen Bewegung des α-Partikels und des Kinderkerns, der, Bei der Verwendung der Gesetze der Erhaltung von Energie und Impuls wird der α-Zerfall als bestimmt
Q \u003d b (A-4, Z-2) + in (4.2) - in (a, z),
wo in (A, z) die Bindungsenergie des Elternkerns ist. Für alle untersuchten α-Übergänge studiert der Wert von q\u003e 0 und überschreitet nicht 10 MEV. Im Jahr 1910 entdeckten Hans Heiger und George Nattol experimentell das Gesetz, das eine Halbwertszeit t 1/2 mit einer Energie verband:
| lGT 1/2 \u003d B + C -1/2 | (1) |
wenn sich die Werte in und Ó nicht von Q abhängen, veranschaulicht Abbildung 1 das spezifizierte Gesetz für gleichmäßige Polonium, Radon und Radium gleichmäßig isotopes. Aber dann erscheint ein sehr ernstes Problem. Das Potential der Wechselwirkung V (R) des α-Partikels und des Kinderkerns, in Abhängigkeit von dem Abstand R zwischen ihren Zentren, ist es möglich, qualitativ wie folgt dargestellt zu werden (Abb. 2). Bei langen Entfernungen sind sie mit Coulomb und Potenzial interagieren
![]()
Bei den kleinen Entfernungen R im Spiel ziehen die Kernkräfte und das Potential V (R) an. Daher erscheint in dem Potential V (R) die Schranke, wobei die Position RB des Maximums v B \u003d V (R b) für schwere Kerne mit Z ≈ 82 im Bereich von 10 bis 12 cm liegt, und der Wert von vb \u003d 25 mev. Aber dann entsteht die Frage wie A-Partikel mit der Energie q < V b kann den radioaktiven Kernel verlassen, wenn sein Wert in der Subventionsregion kinetische Energie K \u003d Q - V (R) wird negativ und aus der Sicht der klassischen Mechanik ist die Bewegung des Partikels in diesem Bereich unmöglich. Die Lösung dieses Problems wurde 1928 vom russischen Physiker G.a gefunden. Gamov. Basierend auf kurzem, vor dieser Zeit, der erstellten Quantenmechanik, zeigten die Gams, dass die Welleneigenschaften der α-Partikel es ermöglichen, es mit einer gewissen Verlustwahrscheinlichkeit durch eine potentielle Barriere gegeben zu werden. Wenn wir dann annehmen, dass das α-Teilchen in einer vollständig ausgebildeten Form innerhalb des Kerns existiert, ist die Wahrscheinlichkeit ihres α-Zerfalls pro Zeiteinheit A, die Formel auftritt.
wo 2 ν - die Anzahl der Schläge der α-Partikel an der Innenwand der Barriere, die durch die Frequenz bestimmt wird ν Schwingungen von α-Partikeln im Mutterkern. Dann wurde die quantenmechanische Größe von P und Schätzen V in den einfachsten Annäherungen in den einfachsten Annäherungen berechnet, der für LGT 1/2 von GEIGER-NATTOL (1) erhielt. Das Ergebnis von Gamova hatte eine große Resonanz bei Physikern, da er demonstrierte, dass der Atomkern durch die Gesetze der Quantenmechanik beschrieben wird. Das Hauptproblem des α-Zerfalls blieb jedoch ungelöst: wobei in schweren Kernen, bestehend aus Neutronen und Protonen, α-Partikel sind?
Multipoint-Alpha-Zerfall-Theorie
Die Vielpartikeltheorie des α-Zerfalls, bei dem das Problem der Bildung eines α-Partikels aus Neutronen und Protonen des Mutterkerns konsequent gelöst ist, stammt in den frühen 50er Jahren und letzten Jahren Er erhielt einen konzeptionellen Fertigstellung in den Werken einiger Physiker, einschließlich des Autors und seiner Mitarbeiter. Diese Theorie beruht auf dem Muschelmodell des Kerns, das im Rahmen der Fermi-Fluid-Theorie LD gerichtet ist. Landau und A.B. Migdal, in dem das Proton und Neutron in einem selbstkonsistenten Feld in dem Kernel in einem selbstkonsistenten Feld angenommen wird, das von den restlichen Nukleonen erzeugt wird. Mit den Hüllewellenfunktionen von zwei Protonen und zwei Neutronen kann man die Wahrscheinlichkeit finden, mit der diese Nukleonen in einem sortikulären Zustand liegen. Dann kann die Formel Gamova (2) als verallgemeinert werden
wENN W IF ist die Wahrscheinlichkeit, dass die Bildung eines Alpha-Partikels aus den Nukleonen des übergeordneten Kernels I einen bestimmten Zustand des Kinderkerns bildet. Berechnungen der Werte von W, wären die wichtigste Bedeutung der Bilanzierung von superfluiden Eigenschaften von Atomkern, um die Natur des Alpha-Zerfalls zu verstehen.
Eine kleine Geschichte. 1911 fand Heika Chalimling-onane das Phänomen der Supraleitung einiger Metalle, für die bei Temperaturen unter einem bestimmten kritischen Widerstand der Sprung auf Null sinkt. 1938, p.l. Kapitsa öffnete das Phänomen der Superfluidität von flüssigem Helium 4 nicht, was darin bestand, dass bei Temperaturen unterhalb eines kritischen flüssigen Heliums durch dünne Kapillarrohre ohne Reibung strömt. Beide Phänomene wurden lange Zeit als unabhängig in Betracht gezogen, obwohl viele Physiker intuitiv ihre Angehörigen fühlten. Die Superfluidität von flüssigem Helium wurde in den Werken von N.n. Bogolyubova und S.T. Belyaeva dadurch, dass bei niedrigen Temperaturen eine Bose-Kondensation durchgeführt wird, bei der sich die meisten Heliumatome in einem Zustand von Nullimpuls ansammeln. Dies ist möglich, weil Heliumatome eine Spin gleich Null haben, und daher sind ein Bose-Partikel, die in beliebigen Mengen in einem bestimmten Quantenzustand sein können, beispielsweise in einem Pulszustand, der Null gleich ist. Im Gegensatz zu den Heliumatomen haben Elektronen, Protonen und Neutronen einen halbfreien Spin und sind Fermi-Partikel, für die das Powli-Prinzip gültig ist, wodurch nur ein Partikel in einem bestimmten Quantenzustand ermöglicht wird. Die Erläuterung der Supraleitfähigkeit von Metallen basiert auf dem von L. Cooper vorhergesagten Phänomen, wenn zwei Elektronen in der Supraleiter ein verknüpftes System bilden, das das Cooper-Paar namens Cooper-Paare bezeichnet. Der volle Spin dieses Paares ist Null, und es kann als Bose-Partikel betrachtet werden. Dann tritt im Supraleiter eine Bose-Kondensation von Cooper-Paaren mit Pulsen gleich Null auf, und sie erscheinen das Phänomen der Superflüssigkeit dieser Paare, das Flüchtlingsphänomen von flüssigem Helium. Superfluidität von Cooper-Paaren und bildet supraleitende Eigenschaften von Metallen. So waren zwei Phänomene formal mit verschiedenen Abschnitten der Physik - supralkuktusivität und der Superfluidität - körperlich bezogen. Die Natur mag es nicht, ihre wundervollen Funde zu verlieren. Es verwendet sie in verschiedenen physischen Objekten. Dies bildet die Einheit der Physik.
Im Jahr 1958 drückte Oge Bor die Hypothese zum Vorhandensein von superfluiden Eigenschaften in Atomkernen aus. In fast einem Jahr wurde diese Hypothese vollständig bestätigt und in der Erzeugung des superfluid-Modells des Atomkerns implementiert, in dem angenommen wird, dass die Paare von Protonen oder Neutronen mit einer Spin von Null gleich und der Bose Kondensation dieser Dampf bildet superfluidische Kerneigenschaften.
Da das α-Teilchen aus zwei Protonen besteht, und zwei Neutronen mit den insgesamt gleichen Spins gleich Null, fällt seine interne Symmetrie mit der Symmetrie von Cooper-Paaren von Protonen und Neutronen in Atomkern zusammen. Daher ist die Wahrscheinlichkeit, ein α-Partikel W erforderlich, wenn es maximal ist, wenn er aus zwei zusammenwirkenden Paarpaaren von Protonen und Neutronen gebildet wird. Die α-Übergänge dieses Typs werden als leichter Bezeichnet und treten zwischen den wichtigsten Zuständen selbster Nuklei auf, in denen alle Nukleons gepaart sind. Für solche Übergänge bei schweren Kernen mit Z\u003e 82 der Wert W falls \u003d 10 -2. Wenn nur ein Cooper-Pair (Proton oder Neutron) in der Zusammensetzung des α-Partikels enthalten ist, werden ähnliche α-Übergänge, die von ungeraden Kernen charakteristisch sind, semi-einfach und für sie w if \u003d 5 * 10 -4 genannt. Wenn schließlich die Person aus ungepaarten Protonen und Neutronen gebildet wird, wird der α-Übergang nicht einfach und für ihn der Wert W if \u003d 10 -5 bezeichnet. Wenn Sie sich auf das superfluid-Modell des Kernels verlassen, gelang es dem Autor und seine Mitarbeiter bis 1985, auf der Grundlage von Typ (3) auf der Grundlage von Typ (3), nicht nur der relativen, sondern auch absoluten Wahrscheinlichkeiten des α-Zerfalls atomarer Kerne zu beschreiben.
Multipurpical Proton Radioaktivitätstheorie
Um den Proton-Zerfall der Atomkerne zuverlässig zu beobachten, ist es notwendig, dass die Energie der relativen Bewegung des Protons und des Kinderkerns Q positiv war und gleichzeitig spürbar weniger als die Höhe war von der Protonpotential VB Barriere, so dass die Lebensdauer des Protonwellenkerns für seine experimentelle Forschung nicht zu klein war. Solche Bedingungen werden in der Regel nur für Hoch-Neutronodefizienzkerne durchgeführt, deren Erhalt nur in den letzten Jahren möglich geworden ist. Derzeit befinden sich mehr als 25 Protonenverteiler aus den wichtigsten und isomeren (ausreichend langlebigen) angeregten Zuständen der Kerne. Aus theoretischer Sicht sieht der Proton-Zerfall wesentlich einfacher aus als α-Zerfall, da das Proton im Kernel enthalten ist, und daher schien es, dass die Formeln wie Formeln (2) verwendet werden könnten. Es wurde jedoch sehr bald, dass fast alle Protonenübergänge für die Struktur der Eltern- und Tochterkerne empfindlich sind, und es ist notwendig, die Formel (3) zu verwenden und die Wahrscheinlichkeiten W zu berechnen, wenn der Autor mit den Mitarbeitern ein Multipurpical entwickeln musste Theorie der Protonradioaktivität unter Berücksichtigung von superfluiden Effekten. Basierend auf dieser Theorie war es möglich, alle beobachteten Fälle von Proton-Zerfall erfolgreich zu beschreiben, einschließlich eines besonders unverständlichen Falls des Zerfalls des langlebigen isomeren Bundesstaates des Kerns von 53 ° C und Vorhersagen in Bezug auf das Neueste Wahrscheinlich Kandidaten zur Beobachtung der Protonenradioaktivität. Gleichzeitig wurde gezeigt, dass die Mehrheit der Protonenwellenkerne im Gegensatz zu den ersten Repräsentationen nicht-Fleece ist.
Clusterverfall von Atomkern
Gegenwärtig wurden 25 Kerne von 221 FRs experimentell nachgewiesen, die aus den Hauptzuständen der Typen 14 C-Cluster, 20 O, 24 NE, 26 NE, 28 mg, 30 mg, 32 Si und 34 Si emittieren. Die Energie der relativen Bewegung des abreibenden Clusters und des Kinderkerns q wandelt sich von 28 bis 94 MEV, und in allen Fällen erweisen sich in allen Fällen, um spürbar kleiner als die Höhe der potentiellen Barriere V B. Gleichzeitig sind alle untersuchten Cluster radioaktiven Kernel α-Zerfall, wobei das Verhältnis der Wahrscheinlichkeit des Cluster-Zerfalls pro Zeiteinheit zu einer ähnlichen Wahrscheinlichkeit λ α für α-Zerkleinerung mit zunehmender Masse des Carving-Clusters abnimmt und in der der Bereich von 10 -9 bis 10 -16. Solche geringen Werte solcher Beziehungen wurden noch nie auf andere Arten von Radioaktivität analysiert und zeigen Rekordleistungen von Experimentierer, wenn der Clusterverfall beobachtet wird.
Derzeit zwei theoretische Ansätze zur Beschreibung der Dynamik des Cluster-Zerfalls atomarer Kerne, die tatsächlich zwei mögliche Grenzwerke sind. Der erste Ansatz betrachtet den Cluster-Zerfall als tiefe, stark asymmetrische spontane Spontane auf den Massen der Fragmente von Fragmenten. In diesem Fall ist der Elternkern in einem Zustand aber Bis zum Zeitpunkt des Brechens in den reibungslosen Wiederaufbau, der Änderung ihrer Form merklich und durch eine Zwischenkonfiguration. b.Was zeigt FIG? 3. Beschreibung einer solchen Umstrukturierung erfolgt auf der Grundlage kollektiver Modelle des Kernels, die eine Verallgemeinerung des hydrodynamischen Modells sind. Dieser Ansatz steht derzeit an erheblichen Schwierigkeiten bei der Beschreibung der subtilen Merkmale des Cluster-Zerfalls.
Der zweite Ansatz wird von Analogie mit der Theorie von α-Zerfall errichtet. In diesem Fall wird der Übergang zum Endkonfigurationsübergang ohne die Einführung einer Zwischenkonfiguration durchgeführt. b. Sofort aus der Konfiguration A in der Sprache der Typ (3) Formel mit dem Konzept der Wahrscheinlichkeit der Wahrscheinlichkeit der Bildung des Clusters W, wenn. Ein gutes Argument zugunsten des zweiten Ansatzes ist die Tatsache, dass für den Clusterverfall, wie bei α-Zerfall, durch das Gesetz von Heigera Nattol (1) durchgeführt wird, das die Clusterperiode der Halbwertszeit t 1 verbindet / 2 und die Energie Q. Diese Tatsache zeigt FIG. 4. Im Rahmen des zweiten Ansatzes, der von der Analogie mit α-Zerfall verwaltet wird, um Clusterübergänge nach dem dankbaren Grad von dankbar zu klassifizieren, verwenden die Ideologie des Superfluid-Kernel-Modells und prognostizieren Sie eine dünne Struktur in den Spektren von abreibenden Clustern. Später wurde die angegebene Struktur in den Experimenten der französischen Gruppe in Sakle entdeckt. Dieser Ansatz ermöglichte es auch, den Maßstab der relativen und absoluten Wahrscheinlichkeiten des bekannten Clusters angemessen zu beschreiben, und ergibt Vorhersagen, um Clusterradioaktivität in neuen Cluster-Zerkleinerungskernen zu überwachen.
Fazit
Untersuchungen verschiedener Arten von Radioaktivität der atomaren Kerne setzt sich derzeit fort. Von besonderem Interesse manifestiert sich für die Untersuchung des Proton-Zerfalls der Kerne, da in diesem Fall einzigartige Informationen über die Struktur der Kerne ermöglicht, die den Grenzen der Nukleonstabilität der Kerne zugrunde liegen. Zuletzt synthetisierte das Team von Physiker unter der Anleitung von Professor K. Davids im Argonne National Laboratory (USA) einen starken Neutronode-Kern 131 EU und fand nicht nur den Proton-Zerfall, sondern erstmals die subtile Struktur seines Protonenspektrums . Die Analyse dieser vom Autor entwickelten Theorie der Theorie der Theorie ermöglichte es, die Idee der starken Nicht-Verboichtigkeit dieses Kerns überzeugend zu bestätigen.
Ein Illustration von Interesse an solchen Forschungen ist der Artikel des Journalisten M. Brauni namens "Ein Blick auf die ungewöhnlichen Kerne ändert den Standpunkt der Atomstruktur", der 1998 in der März-Ausgabe der New York Time-Zeitung erschien, in dem die Ergebnisse in populärer Form erzählt werden, das von der Argonne-Gruppe und der Wege ihrer Interpretation erhalten wird.
Die oben genannte Überprüfung, die die Entwicklung von Ideen zur Natur der Radioaktivität der atomaren Kerne für ein gesamtes Jahrhundert darstellt, zeigt eine explizite Beschleunigung des Tempos, in diesem Bereich neues Wissen in diesem Bereich in den letzten 25 Jahren ein neues Wissen zu erhalten. Und obwohl die Kernphysik recht in der experimentellen und theoretischen Sinne von der Wissenschaft entwickelt ist, ist es zweifellos, dass die Forschung darauf, und auch an der Kreuzung mit anderen Wissenschaften, die Forschung in der Nähe von neuem und erstaunlichen Ergebnissen in der Nähe ist.
Radioaktive Transformationen von Kernel
Struktur der Materie
Alles in der Natur besteht aus einfachen und komplexen Substanzen. Einfache Substanzen umfassen chemische Elemente, komplexe chemische Komponenten. Es ist bekannt, dass Substanzen in der Welt um uns herum aus Atomen bestehen, die der kleinste Teil des chemischen Elements sind. Atom ist das kleinste Teilchen einer Substanz, die es definiert. chemische Eigenschaftener hat schwierig interne Struktur. In der Natur sind nur inerte Gase in Form von Atomen gefunden, da ihre äußeren Schalen geschlossen sind, gibt es in Form von Molekülen alle anderen Substanzen.
1911 schlug E. Rutherford ein Planetenmodell eines Atoms vor, das von Born (1913) entwickelt wurde. Gemäß dem allgemein akzeptierten Modell der Struktur des Atoms darin werden zwei Bereiche unterschieden: ein starker, positiv aufgeladener Kernel, der sich in der Mitte befindet, in der fast alle Masse des Atoms konzentriert ist, und eine Lichtelektronenhülle besteht aus von negativ geladenen Teilchen - Elektronen, mit einer riesigen Drehzahl um den Kernel.
Elektron (e -)- stabile Elementarteilchen mit einer Rufmasse gleich 9,1 · 10 -31 kg oder 0,000548 ae.m. (Atomische Masseneinheit ist eine gleichgültige Menge an Atommasse, die zeigt, wie oft das Atom dieses Elements oder Teilchen schwerer als 1/12 Teile des Kohlenstoff-Isotop-Atoms-12 ist; Energieäquivalent 1 A.M ist 931 MEV). Das Elektron trägt eine elementare negative Ladung von Elektrizität (Q \u003d 1,6 · 10 -19 cl), d. H. Die kleinste Menge an Strom, die in der Natur auftritt. Basierend auf dieser Ladung des für einen angenommenen Elektronen grundeinheit Elektrische Ladung.
Je nach Energie, die Elektronen beim Drehen des Kernels hält, werden sie in verschiedenen Umlaufbahnen (Level oder Ebenen) gruppiert. Die Anzahl der Schichten in verschiedenen Atomen ist ungleich. In Atomen mit großer Masse erreicht die Anzahl der Umlaufbahnen sieben. Sie sind mit Zahlen oder Buchstaben des lateinischen Alphabets gekennzeichnet, das das Symbol aus dem Kern beginnt: K, L, M, N, O, P, Q. Die Anzahl der Elektronen in jeder Schicht ist streng definiert. So weist die K-Schicht nicht mehr als 2 Elektronen, die L-Schicht bis 8, M-Schicht bis 18, n-Schicht-32-Elektronen usw. auf.
Die Abmessungen des Atoms werden durch die Größen seiner elektronischen Hülle bestimmt, was keine streng definierten Grenzen hat. Annähernd lineare Abmessungen des Atoms betragen 10 -10 m.
Ader - der zentrale massive Teil des Atoms, bestehend aus Protonen und Neutronen, das positiv aufgeladen ist. Fast alle Atommasse konzentrieren sich im Kern (mehr als 99,95%). Die Gesamtzahl der Elektronen in Umlaufbahnen entspricht immer der Menge an Protonen im Kernel. Beispielsweise enthält ein Sauerstoffatom 8 Protonen im Kern und weist 8 Elektronen in Umlaufbahnen, ein Blei-Atom-82-Proton in den Kernel- und 82-Elektronen in Umlaufbahnen auf. Aufgrund der Gleichheit der Menge an positiven und negativen Ladungen ist ein Atom ein elektrisch neutrales System. Für jedes der Elektronen, der sich um den Kernel bewegt, gibt es zwei gleiche, entgegengesetzt gerichtete Kräfte: Die Coulomb-Kraft zieht Elektronen an den Kernel an, und die Zentrifugalkraft der Trägheit strebt an, "ein Elektron aus dem Atom herausziehen. Außerdem haben Elektronen, Bewegung (rotierend) um den Orbit-Kernel, gleichzeitig ihren eigenen Bewegungsmoment, der als Spin genannt wird, einfach als Drehung wie eine Spitze um die eigene Achse dargestellt. Die Spins einzelner Elektronen können parallel ausgerichtet sein (drehung in derselben Richtung) und der Anteile der Anteile (Rotation in verschiedenen Richtungen). In vereinfachter Form gewährleistet all dies die stetige Bewegung von Elektronen im Atom.
Es ist bekannt, dass nicht nur die Coulomb-Kraft der Anziehungskraft und der Zentrifugalkraftenträger, sondern auch die Festigkeit der Abstoßung anderer Elektronen, für den Anschluss des Elektrons mit dem Kern gültig ist. Dieser Effekt wird als Abschirmung bezeichnet. Die weitere elektronische Umlaufbahn aus dem Kern, desto stärker ist das Screening von Elektronen auf ihn und der schwächer die Energiebindung das Elektron. In externen Umlaufbahnen überschreitet die Elektronenbindungsenergie nicht mehr als 1-2 eV, während die Elektronen der K-Schicht oft mehrmals stärker sind und mit einer Erhöhung der Atomzahl des Elements zunimmt. Beispielsweise ist in Kohlenstoff die elektronenbindende Energie der K-Schicht 0,28 KEV, das Strontium - 16 KEV, am Cäsium - 36 KEV, in Uran - 280 KEV. Daher sind die Elektronen der externen Umlaufbahn externen Faktoren, insbesondere niedrige Energieemissionen, ausgesetzt. Bei der Kommunikation von Elektronen von außen zusätzlicher Energie können sie sich von einem Energieriveau zur anderen bewegen oder sogar die Grenzen dieses Atoms verlassen. Wenn die externe Belichtungsenergie mit dem Kernel schwächer ist als die Elektronenbindung mit dem Kernel, kann das Elektron nur von einem Energiepegel zur anderen ziehen. Ein solcher Anom bleibt jedoch neutral, unterscheidet sich jedoch von den verbleibenden Atomen dieses chemischen Elements mit einem Überschuss an Energie. Atome mit einem Überschuss an Energie werden angerufen und der Übergang von Elektronen von einem Energiepegel zur anderen, der Remote aus dem Kernel, dem Erregungsprozess. Da in der Natur jedes System dazu neigt, in einen stabilen Zustand zu wechseln, in dem seine Energie der kleinste sein wird, dann bewegt es sich zu einem Zeitpunkt, wenn er sich vom angeregten Zustand in die Hauptstärke (Initial) bewegt. Die Rückkehr des Atoms in den Bodenzustand wird von der Freisetzung von überschüssiger Energie begleitet. Der Übergang von Elektronen aus äußeren Umlaufbahnen an das Inn wird von Strahlung mit einem Wellenlängencharakteristik nur für diesen Übergang von einem Energieniveau zur anderen begleitet. Elektronenübergänge Innerhalb der aus dem Kernel, die aus dem Kernel abgelegensten Orbits bestehen, bestreiten Strahlung, bestehend aus ultravioletten, leichten und Infrarotstrahlen. Bei starken externen Effekten, wenn die Energie die Elektronenbindungsenergie mit dem Kern übersteigt, werden die Elektronen aus dem Atom herausgezogen und werden über seine Grenzen hinaus entfernt. Ein Atom, das einen oder mehrere Elektronen verliert, verwandelt sich in ein positives Ion, und "angebracht" zu sich selbst ein oder mehrere Elektronen in einem negativen Ion. Folglich ist ein negatives Ion für jedes positive Ion ausgebildet, dh ein Paar von Ionen entsteht. Der Prozess der Bildung von Ionen aus neutralen Atomen wird genannt ionisation. Atom im Zustand des Ionen besteht in normalen Bedingungen eine extrem kurze Zeit. Der freie Ort in der Umlaufbahn des positiven Ions ist mit einem freien Elektron gefüllt (ein Elektron, das nicht mit einem Atom verbunden ist) und das Atom wird wieder ein neutrales System. Dieser Prozess wird als Rekombination von Ionen (Entionisierung) bezeichnet und wird durch Ausscheidung von überschüssiger Energie als Strahlung begleitet. Die während der Ionenrekombination freigesetzte Energie ist numerisch ungefähr gleich der Energie, die für die Ionisierung aufgewendet wird.
Proton(r.) - ein stabiles Elementarteilchen mit einer Masse von 1,6725 · 10 -27 kg oder 1,00758 AE.M., das etwa 1840 mal mehr Elektronenmasse ist. Die Protonenladung ist positiv und in der Größe entspricht der Elektronenladung. Das Wasserstoffatom ist ein Kernel, der ein Proton enthält, um das ein Elektron dreht. Wenn Sie dieses Elektron "stören", dann ist der verbleibende Teil des Atoms ein Proton, daher wird das Proton häufig als Wasserstoffkern definiert.
Jedes Atom eines beliebigen Elements enthält eine bestimmte Anzahl von Protonen in dem Kernel, das ständig die physikalischen und chemischen Eigenschaften des Elements bestimmt. Zum Beispiel in dem Kernel des Silberatoms von ihnen 47 im Urankern - 92. Die Anzahl der Protonen im Kernel (Z) wird als Atomzahl oder Ladungsnummer bezeichnet, entspricht der Reihenfolge des Elements in der Periodensystem di MendeleeV.
Neutron(n.) - Elektrisch neutrales Elementarteilchen mit einer Masse von etwas übertriebenen Masse des Protons und gleich 1,6749 10 -27 kg oder 1.00898 AE.M. Neutron ist nur in der Zusammensetzung stabiler atomarer Kerne stabil. Kostenlose Neutronen zerfallen auf Protonen und Elektronen.
Neutron, aufgrund seiner elektrischen Neutralität, weicht nicht unter der Wirkung eines Magnetfelds ab, wird nicht vom Atomkern abgestoßen, und hat daher eine große Durchdringungsfähigkeit, die eine schwere Gefahr als biologischer Effektfaktor der Strahlung erzeugt. Die Anzahl der Neutronen im Nukleus ergibt nur grundsätzlich die physikalischen Eigenschaften des Elements, da in verschiedenen Kernen des gleichen chemischen Elements eine andere Anzahl von Neutronen (von 1 bis 10) sein kann. In den Kernen der Lunge stabiler Elemente bezieht sich die Anzahl der Protonen auf die Anzahl der Neutronen als 1: 1. Mit einer Erhöhung der Atomzahl des Elements (ab dem 21. Element - Scandium) in seinen Atomen übersteigt die Anzahl der Neutronen die Anzahl der Protonen. In den schwersten Kernen ist die Anzahl der Neutronen 1,6-fachen die Anzahl der Protonen.
Protonen und Neutronen sind zusammengesetzte Teile des Kerns, sodass sie Nukleonen genannt werden, um die Bequemlichkeit zu nennen. Nuklon(von Lat. Nucleus - Kernel) - Allgemeiner Name für Protonen und Neutronenkern. Wenn sie über einen bestimmten atomaren Kern sprechen, wird der Begriff Nuklid verwendet. Nuklid - jeder Atomkern mit einer vorbestimmten Anzahl von Protonen und Neutronen.
Die Entwicklung von Nukliden oder Atomen, verwenden das Symbol des Elements, an dem der Kernel gehört, und angeben die Massenzahl - A, an der Unterseite der atomaren (Reihenfolge)-Nummer - Z in Form von Indizes, wobei E ein Symbol der Chemisches Element. Und zeigt die Anzahl der Nukleonen, von denen der Kern des Atoms (a \u003d z + n) ist. Z zeigt nicht nur die Ladung des Kerns und der Sequenznummer, sondern auch die Anzahl der Protonen im Kernel und dementsprechend die Anzahl der Elektronen im Atom, weil Atom im Allgemeinen neutral. N ist die Anzahl der Neutronen im Kernel, das am häufigsten angegeben ist. Beispielsweise, - radioaktives Isotop von Cäsium, A \u003d 137, daher besteht der Kern aus 137 Nukleonen; Z \u003d 55, was im Kern von 55 Protonen bzw. 55 Elektronen im Atom bedeutet; N \u003d 137 - 55 \u003d 82 ist die Anzahl der Neutronen im Kernel. Die Sequenznummer wird manchmal abgesenkt, da der Zeichen des Elements seinen Platz in dem periodischen System vollständig definiert (z. B. CS-137, nicht-4). Die lineare Größe des Kerns des Atoms beträgt 10 -15 -10 -14 m, was 0,0001 Durchmesser des Gesamtatoms beträgt.
Protonen und Neutronen werden durch die angerufenen Kräfte im Kern gehalten nuklearer. In seiner Intensität sind sie viel stärkere elektrische, Gravitations- und Magnetkräfte. Kernkräfte sind mit einem Radius von 10 -14 bis 10 -15 m kurz. Sie manifestieren sich gleichermaßen zwischen dem Proton und dem Neutron, einem Protonen- und Protonen, Neutronen und Neutron. Mit zunehmendem Abstand zwischen Nukleonen werden Kernkräfte sehr schnell reduziert und werden nahezu gleich Null. Kernkräfte haben die Eigenschaft der Sättigung, d. H. Jeder Nukleon interagiert nur mit einer begrenzten Anzahl benachbarter Nucleons. Daher wird mit einer Erhöhung der Anzahl der Nukleonen im Kern die Kernkräfte erheblich geschwächt. Dies erklärt die geringere Stabilität der Hauptelemente, die eine beträchtliche Anzahl von Protonen und Neutronen enthalten.
Um den Kernel an die Komponenten seiner Protonen und Neutronen zu teilen und aus dem Wirkungsbereich der Atomkräfte zu entfernen, ist es notwendig, zu arbeiten, d. H. Kostensenergie. Diese Energie wird aufgerufen die bindende Energie des Kerns. Wenn der Kern gebildet wird, zeichnet sich die Energie des Bobs im Gegenteil aus.
m i \u003d m p n p + m n n n
wo M i - die Masse des Kerns; m p - Protonmasse; N p - die Anzahl der Protonen; M n - Neutronenmasse; N n ist die Anzahl der Neutronen, es ist gleich 1,0076 · 2 + 1.0089 · 2 \u003d 4.033 A.e.M.
Gleichzeitig beträgt die tatsächliche Masse des Heliumkerns 4.003 Uhr. Somit ertönt die tatsächliche Masse des Heliumkerns als geringer als der berechnete Wert von 0,03 AE.M. In diesem Fall sagen sie, dass der Kernel einen Massenfehler hat (Mangel an Masse). Der Unterschied zwischen der berechneten und tatsächlichen Masse des Kerns des Kerns wird als Massenfehler (DM) bezeichnet. Der Massenfehler zeigt, wie fest die Partikel im Kernel verbunden sind, sowie wie viel Energie getrennt wurde, wenn der Kern aus einzelnen Nukleonen gebildet wird. Sie können eine Masse mit Energie unter Verwendung einer von A. Einstein abgeleiteten Gleichung binden:
wärter ist die Änderung der Energie; DM - Massenfehler; C ist die Lichtgeschwindigkeit.
Gegeben, dass 1 a.e.m. \u003d 1,661 10 -27 kg, und in der Kernphysik pro Energieeinheit wurde ein Elektronenvolt (EV) empfangen, und 1 bis cm. Entspricht 931 MEV, dann wird die Energie, die während der Bildung des Heliumkerns verlängert wird, gleich 28 MEV. Wenn es einen Weg gab, den Kernel des Heliumatoms in zwei Protonen und zwei Neutronen zu trennen, wäre es notwendig, mindestens 28 Mio. Energie zu verbringen.
Die verbindliche Energie der Kerne erhöht sich mit einer Erhöhung der Anzahl der Nukleonen, jedoch nicht streng im Verhältnis zu ihrer Zahl. Zum Beispiel Stickstoffkern-Kommunikationsenergie - 104.56 MeV und Uran - 1800 MeV.
Die durchschnittliche bindende Energie, die auf einem Nukleon kommt, wird genannt spezifische Kommunikation. Für Helium wird es 28: 4 \u003d 7 Mev sein. Wenn Sie nicht die einfachsten Kernel (Deuterium, Tritium) zählen, ist die Kommunikationsenergie für einen Nukleon für alle Kerne von ungefähr 8 MeV.
Die meisten chemischen Elemente in der Natur sind bestimmte Mischungen von Atomen mit Kernen verschiedener Massen. Die Unterschiede in den Massen sind auf die Anwesenheit in Kernen zurückzuführen von verschiedenen Zahlen Neutronen.
Isotope (aus dem Griechisch. ISOS ist derselbe und topos - Sorten des Atoms des gleichen chemischen Elements, das die gleiche Anzahl von Protonen (Z) und eine andere Anzahl von Neutronen (N) aufweisen. Sie haben fast die gleichen physikalischen und chemischen Eigenschaften, die sie in der natürlichen Mischung teilen, ist sehr schwierig. Die Anzahl der Isotope von Elementen variiert von 3 - bei Wasserstoff bis 27 - im Polonium. Isotope sind stabil und instabil. Stabile Isotope im Laufe der Zeit werden keine Änderungen unterzogen, wenn sich nicht von außen auswirkt. Instabile oder radioaktive Isotope auf Kosten von Prozessen, die im Kern auftreten, werden im Laufe der Zeit in Isotope anderer chemischer Elemente. Stabile Isotope befinden sich nur an Elementen mit der Sequenznummer Z ≤ 83. Derzeit sind etwa 300 stabile und mehr als 2000 radioaktive Isotope bekannt. Für alle Elemente des periodischen Systems werden D. I. Mendeleev, radioaktive Isotope synthetisiert, als künstlich genannt.
Phänomen der Radioaktivität.
Alle chemischen Elemente sind nur in einem engen Intervall des Verhältnisses der Anzahl der Protonen auf die Anzahl der Neutronen im Kernel stabil. In der Lunge von Kernen sollte es annähernd robuste Protonen und Neutronen geben, d. H. Der Wert des Verhältnisses n: p ist nahe an 1, für schwere Kerne wird dieses Verhältnis auf 0,7 reduziert. Wenn es zu viele Neutronen oder Protonen im Kernel gibt, werden solche Kerne instabil (instabil) und werden spontane radioaktive Transformationen unterzogen, wodurch die Zusammensetzung des Kerns ändert und die geladenen oder neutralen Partikel emittiert werden. Das Phänomen der spontanen Strahlung wurde als Radioaktivität genannt, und Substanzen emittieren Strahlung - radioaktiv.
Radioaktivität (von lat. Radio-Radius, Radiusstrahl, Aktivus - effektiv) - diese sind spontane Transformationen (Zerklasz) von atomaren Kernen von einigen chemischen Elementen in Atomkern von anderen Elementen mit der Emission einer besonderen Art von Strahlung. Die Radioaktivität führt zu einer Änderung der atomaren Zahl und der Massenzahl des selektischen chemischen Elements.
Die Eröffnung des Phänomens der Radioaktivität trugen zu den zwei größten Öffnungen des 19. Jahrhunderts bei. Im Jahr 1895 fanden V-Röntgenstrahlen Strahlen, die beim Überlassen des Hochspannungsstroms zwischen den in einem versiegelten Glasrohr angeordneten Elektroden auftrat, von dem Luft abgeladen wurde. Strahlen wurden Röntgenn genannt. Und 1896 entdeckte A. Becquer, dass Uransalze spontan unsichtbarer Strahlen mit einer großen Durchdringungsfähigkeit emittieren, wodurch die Schwärzung des Photofastischen und der Glühen einiger Substanzen verursacht wurden. Diese Strahlung nannte er radioaktiv. Im Jahr 1898 eröffnete Pierre Curie und Maria Sklodovskaya-Curie zwei neue radioaktive Elemente - Polonium und Radium, die eine solche Strahlung emittierten, aber die Intensität von ihnen übertraf die Intensität der Uranstrahlung. Darüber hinaus wurde festgestellt, dass radioaktive Substanzen kontinuierlich Energie in Form von Wärme ausscheiden.
Die radioaktive Strahlung wird auch ionisierend bezeichnet, da sie das Medium oder das Nuklear ionisieren können, was die Tatsache betont, dass Strahlung vom Kern und kein Atom emittiert wird.
Der radioaktive Zerfall ist mit Änderungen der Atomkerne und der Freigabe von Energie verbunden, deren Wert in der Regel mehrere Größenordnungen höher als die Energie chemischer Reaktionen ist. So wird mit einem vollen radioaktiven Zerfall von 1 G-Atom 14, 3 zugeordnet. 10 9 Kalorien, während die Verbrennung derselben Menge 14c zu Kohlendioxid nur 9.4 zugeordnet ist. 10 4 Kalorien.
Als Energieeinheit der radioaktiven Zersetzung wird 1 elektronenvolt (eV) genommen und 1 kev -derivate \u003d 10 3 eV und 1 mev \u003d 10 6 eV. 1 eV \u003d 1.6. 10 -19 J. 1 EV entspricht der von dem Elektron im elektrischen Feld erfassten Energie, wenn der Weg passiert ist, auf dem die Potentialdifferenz 1 Volt beträgt. Wenn der Zusammenbruch der meisten radioaktiven Kerne, ist die freigesetzte Energie von mehreren KeV auf mehrere MeV.
Radioaktive Phänomene, die in der Natur auftreten, werden als natürliche Radioaktivität genannt; Ähnliche Verfahren, die in künstlich erhaltenen Substanzen (durch geeignete Kernreaktionen) - künstliche Radioaktivität auftreten. Beide Arten von Radioaktivität gehorchen jedoch die gleichen Gesetze.
Arten von radioaktivem Zerfall
Die Kerne von Atomen sind stabil, ändern jedoch seinen Zustand in der Unterbrechung eines bestimmten Verhältnisses von Protonen und Neutronen. In der Lunge von Kernen sollten ungefähr gleichermaßen aufgelistete Protonen und Neutronen sein. Wenn es zu viele Protonen oder Neutronen im Kernel gibt, sind solche Kerne instabil und unterzogen sich spontane radioaktive Transformationen, wodurch die Zusammensetzung des Kerns geändert wird und daher der Kern des Atoms eines Elements in die Kern des Atoms eines anderen Elements. In diesem Prozess wird die Atomstrahlung emittiert.
Es gibt folgende Haupttypen von Kerntransformationen oder Arten von radioaktivem Zerfall: Alpha-Zerfall und Beta-Zerfall (Electronic, Positron und K-Capture), interne Konvertierung.
Alpha-Zerfall -dies ist die Emission des Kerns des radioaktiven Isotops von Alphateilchen. Aufgrund des Verlusts mit einem Alpha-Teilchen von zwei Protonen und zwei Neutronen dreht sich der zerfallende Kern in einen anderen Kern, in dem die Anzahl der Protonen (Kernladung) um 2 abnimmt, und die Anzahl der Partikel (Massenzahl) um 4. Mit diesem radioaktiven Zerfall gemäß den von Fayen und Soddy (1913) formulierten (1913) formulierten (1913) formulierten (Kind) -Element wird in zwei Zellen nach links in zwei Zellen in zwei Zellen versetzt Periodensystem di MendeleeV. Der Prozess des Alpha-Zerfalls in allgemeines wie folgt geschrieben:
![]() ,
,
wobei x das Symbol des Quellkerns ist; Y - Symbol des Kerns des Zerfallsprodukts; 4 2 He-Alpha-Partikel, Q - Befragte überschüssige Energie.
Zum Beispiel wird der Zerfall der Radie-226-Kerne mit der Emission von Alpha-Partikeln mit Radium-226-Kern in Radon-222-Kernel begleitet:
![]()
Die während des Alpha-Zerfalls freigesetzte Energie ist zwischen dem Alpha-Partikel unterteilt, und der Kern ist umgekehrt proportional zu ihren Massen. Die Energie von Alpha-Partikeln ist streng mit einer Halbwertszeit dieses Radionuklids (Geiger-Nettols Gesetz) verbunden. . Dies deutet darauf hin, dass, dass Sie die Energie von Alpha-Partikeln kennen, die Halbwertszeit und in der Halbwertszeit einstellen können, das Radionuklid identifizieren. Zum Beispiel ist der Kern von Polonium-214 durch die Energiewerte der Alpha-Partikel E \u003d 7,687 MEV und T 1/2 \u003d 4,5 × 10 -4c gekennzeichnet, während für den Uran-238 E \u003d 4,196 MeV und T 1/2 \u003d 4, 5 × 10 9 Jahre. Darüber hinaus wurde festgestellt, dass die Energie des Alpha-Zerfalls größer ist, desto schneller strömt es.
Alpha-Zerfall ist eine ziemlich häufige nukleare Umwandlung von schweren Kernen (Uran, Thorium, Polonium, Plutonium usw. mit Z\u003e 82); Derzeit sind mehr als 160 alpha strahlende Kerne bekannt.
Beta-Zerfall -spontane Transformationen des Neutrons in Protonen oder Protonen in das Neutronen im Nukleus, begleitet von der Emission der Elektronik und des Antineutrino oder des Neutrino N E.
Wenn der Kernel überschüssige Neutronen hat ("Neutronenüberlastung" des Kernels), tritt ein elektronischer Beta-Zerfall auf, in dem sich eines der Neutronen in ein Proton verwandelt, das das Elektronen- und Antineutrino emittiert:
Gleichzeitig wird der Zerfall des Kerns und dementsprechend die atomare Zahl des Kernkerns um 1 erhöht, und die Massenzahl ändert sich nicht, dh das untergeordnete Element wird in dem periodischen System von di Mendeleev auf einer Zelle verschoben rechts vom Original aus. Der Prozess des Beta-Zerfalls im Allgemeinen ist wie folgt geschrieben:
![]() .
.
Auf diese Weise zerfällt die Kerne mit einem überschüssigen Neutron. Zum Beispiel wird der Zerfall von Strontium-90-Kernel mit der Emission von Elektronen begleitet und in Yttrium-90 verwandelt:
Oft haben der Kern der während des Beta-Zerfalls gebildeten Elemente übermäßige Energie, die durch die Emission eines oder mehrerer Gamma-Quanten freigegeben wird. Beispielsweise:
![]()
Der elektronische Beta-Zerfall ist charakteristisch für viele natürliche und künstlich erhaltene radioaktive Elemente.
Wenn das ungünstige Verhältnis von Neutronen und Protonen im Kernel auf überschüssigen Protonen zurückzuführen ist, gibt es einen Positron-Beta-Zerfall, in dem der Kernel auf Positrone und Neutrinos als Ergebnis der Umwandlung des Protons in Neutron in den Kernel isst:
Die Ladung des Kerns und deshalb nimmt die Kernzahl des untergeordneten Elements um 1 ab, die Massenzahl ändert sich nicht. Das untergeordnete Element wird einen Platz im Periodensystem D. I. Mendeleev auf einer Zelle links von dem Mütternal besetzen:
![]()
Positron-Zerfall wird in einigen künstlich erhaltenen Isotopen beobachtet. Zum Beispiel der Zerfall des Phosphor-30-Isotops mit Siliziumformation-30:
Das Positron, das vom Kernel abfällt, bricht mit einem "extra" -Eronenatom (schwach mit dem Kernel verbunden) oder interagiert mit einem freien Elektron, der ein Paar "Positron-Elektron" bildet. Aufgrund der Tatsache, dass das Partikel und das Antipartikel mit der Freisetzung von Energie sofort gegenseitig verfällt, dreht sich der geformte Dampf in zwei Gamma-Quanten mit einer Energie, die der Masse von Partikeln (E + und E -) äquivalent ist. Der Prozess der Umdrehung des Paares "Positron-Elektron" in zwei Gamma-Quantum wird als Vernichtung (Zerstörung) und das aufkommende elektromagnetische Strahlung Anniehung genannt. In diesem Fall wird eine Form der Materie (Partikel des Stoffs) in eine andere (Strahlung) umgewandelt. Dies wird durch das Vorhandensein der umgekehrten Reaktion bestätigt - die Umsetzung der Bildung eines Paares, in dem die elektromagnetische Strahlung einer ausreichend hohen Energie, die in der Nähe des Kerns unter der Wirkung eines starken elektrischen Feldes des Atoms führt, in ein Paar "Electron-Positron".
Somit fliegen mit einem Positron-Beta-Zerfall keine Partikel, sondern zwei Gamma-Quanten, die in 0,511 MEV Energie auftreten, aus dem Elternkern, der ein Energieäquivalent der Masse der Pause der Partikel - Positrone und Elektron E \u003d aufweist. 2m EC 2 \u003d 1.022 MEV.
Die Umwandlung des Kerns kann durch elektronischem Griff durchgeführt werden, wenn eine der Protonen des Kernels spontan ein Elektron mit einem der Innenschalen eines Atoms (k, l usw.) erfasst, der meistens mit k-shell, und verwandelt sich in ein Neutron. Ein solcher Prozess wird auch aufgenommen, um zu erfassen. Das Proton verwandelt sich nach der folgenden Reaktion in ein Neutron:
In diesem Fall nimmt die Ladung des Nukleus um 1 ab, und die Massenzahl ändert sich nicht:
Beispielsweise,
Gleichzeitig nimmt der von der Elektron freigesetzte Ort ein Elektron von den Außenschalen des Atoms ein. Infolge der Umstrukturierung von elektronischen Muscheln wird Röntgenquantum emittiert. Das Atom behält immer noch elektrische Neutralität, da die Anzahl der Protonen im Kern während des elektronischen Griffs pro Abnahme pro Einheit abnimmt. Somit führt diese Art von Zerfall zu den gleichen Ergebnissen wie der Positron-Beta-Zerfall. In der Regel ist es typisch für künstliche Radionuklide.
Die vom Kernel freigesetzte Energie mit einem Beta-Zerfall eines bestimmten Radionuklids ist immer konstant, aber aufgrund der Tatsache, dass die Art des Zerfalls nicht zwei und drei Partikel ausgebildet ist, und drei Partikel: der Dummy-Kern (Kind), Elektron (oder Positron) und Neutrinos, dann unterscheidet sich die Energie in jedem Zerfall, der Zerfall wird zwischen dem Elektron (Positron) und Neutrino umverteilt, da die Tochtergesellschaft des Kernels immer den gleichen Teil der Energie nimmt. Je nach Winkel der Spule kann Neutrino größere oder weniger Energie durchgeführt werden, wodurch das Elektron Energie von Null auf einen bestimmten Maximalwert erhalten kann. Daher, mit Beta-Zerfall von Beta-Partikeln desselben Radionuklids haben unterschiedliche Energie, Von Null bis zu einem maximalen Wert, der für den Zerfall dieses Radionuklids charakteristisch ist. Bei der Energie der Beta-Strahlung ist es fast unmöglich, Radionuklid zu identifizieren.
Einige Radionuklide können auf zwei oder drei Arten gleichzeitig abfallen: durch Alpha- und Beta-Zerfälle und durch K-Capture eine Kombination von drei Arten von Zerfall. In diesem Fall wird die Umwandlung in einem streng definierten Verhältnis durchgeführt. Beispielsweise ist das natürliche langlebige Radioisotop von Kalium-40 (t 1/2 \u003d 1,49 × 10 9 Jahre), deren Inhalt in natürlichem Kalium 0,0119% beträgt, einem elektronischen Beta-Zerfall und zum Erfassen unterzogen:
![]() (88% - elektronischer Zerfall),
(88% - elektronischer Zerfall),
![]() (12% - k-Capture).
(12% - k-Capture).
Von den oben beschriebenen Arten von Zerkennungen kann geschlossen werden, dass der Gamma-Zerfall in "reiner Form" nicht existiert. Gamma-Strahlung kann nur von verschiedenen Arten von Zerfällen begleitet werden. Bei der Emission von Gammastrahlung im Kernel werden weder Massenzahl oder seine Ladung nicht geändert. Folglich ändert sich die Art des Radionuklids nicht, sondern nur die in den Kernel enthaltene Energie. Die Gamma-Strahlung wird ausgesetzt, wenn sich Kerne mit aufgeregten Niveaus zu mehr bewegen niedrige Level, auch auf der Hauptseite. Wenn zum Beispiel der Cäsium-137 verfallen ist, wird der angeregte Barium-137-Kernel gebildet. Der Übergang von angeregter bis zu einem stabilen Zustand wird von der Emission von Gamma Quanta begleitet:
![]()
![]()
Da die Lebensdauer von Kernen in aufgeregten Zuständen sehr klein ist (normalerweise t<10 -19 с), то при альфа- и бета-распадах гамма-квант вылетает практически одновременно с заряженной частицей. Исходя из этого, процесс гамма-излучения не выделяют в самостоятельный вид распада. Entsprechend der Energie der Gamma-Strahlung, wie bei der Energie der Alpha-Strahlung, können Sie Radionuklid identifizieren.
Interne Umwandlung.Angeregt (infolge einer Kerntransformation) zeigt der Zustand des Atomkerns das Vorhandensein eines Energieüberguts darin. Zu einem Zustand mit einem niedrigeren Energie (normaler Zustand) kann der angeregte Kernel nicht nur durch Strahlung von Gamma-Quantum oder Emissionen von Partikeln, sondern auch durch interne Umwandlung oder Umwandlung auf die Bildung von Elektronenpositionenpaaren übersetzen.
Das Phänomen der internen Umwandlung besteht darin, dass der Kernel die Anregungsenergie an einen der Elektronen der inneren Schichten (k-, l-oder M-Schicht) überträgt, was zu den Grenzen des Atoms führt. Solche Elektronen wurden Umwandlungselektronen bezeichnet. Folglich ist das Emittieren der Elektronen der Umwandlung auf die direkte elektromagnetische Wechselwirkung des Kerns mit den Elektronen der Schale zurückzuführen. Umwandlungselektronen haben im Gegensatz zu Elektronen-Beta-Zerfall ein Spaziergüter-Energiespektrum, wodurch ein festes Spektrum ergibt.
Wenn die Anregungsenergie 1,022 MEV übersteigt, kann der Kernelübergang zum Normalzustand von der Emission des Elektron-Positron-Paars begleitet werden, gefolgt von ihrer Annihilation. Nach der inneren Umwandlung erscheint die "freie" Szene der konturierten Elektronenkonvertierung in der elektronischen Hülle des Atoms. Eine der Elektronen von mehr entfernten Schichten (mit höheren Energienebenen) führt einen Quantenübergang zum "vakanten" Ort mit der Emission der charakteristischen Röntgenstrahlung durch.
Eigenschaften der Atomstrahlung
Kernlichtstrahlung (radioaktive) Strahlung ist Strahlung, die als Folge eines radioaktiven Zerfalls ausgebildet sind. Die Strahlung aller natürlichen und künstlichen Radionuklide ist in zwei Arten unterteilt - korpuskulärer und elektromagnetisch. Die korpuskuläre Strahlung ist ein Fluss von Partikeln (Korpuskel), das durch eine bestimmte Masse, Ladung und Geschwindigkeit gekennzeichnet ist. Dies sind Elektronen, Positronen, der Kernel von Heliumatomen, Deuterons (Wasserstoff-Isotop-Kernel von Deuterium), Neutronen, Protonen und anderen Partikeln. In der Regel ionize die korpuskuläre Strahlung die Umwelt direkt ionisieren.
Elektromagnetische Strahlung ist ein Fluss von Quanten oder Photonen. Diese Strahlung hat weder Masse oder Ladung und erzeugt eine indirekte Ionisierung des Mediums.
Bei der Bildung von 1 Paar Ionen in der Luft ist im Durchschnitt 34 eV erforderlich. Daher umfassen ionisierende Strahlungen Strahlung mit Energie von 100 und über eV (nicht sichtbares Licht und UV-Strahlung umfassen).
Für die Eigenschaften von ionisierender Strahlung werden Kilometer und spezifische Ionisierung verwendet. Kilometerleistung ist die minimale Dicke des Absorbers (einiger Substanz), die für die vollständige Absorption von ionisierender Strahlung erforderlich ist. Eine spezifische Ionisierung ist die Anzahl der Paare von Ionen, die von einer Einheit der Länge des Weges in der Substanz unter dem Einfluss der ionisierenden Strahlung gebildet werden. Beachten Sie, dass das Konzept eines Laufs und der Länge der zurückgelegten Entfernung nicht identische Konzepte ist. Wenn sich die Partikel gerade bewegen, übereinstimmen diese Werte, wenn die Flugbahn der Teilchenbewegung eine gebrochene Wickellinie ist, dann ist die Kilometerleistung immer weniger als die Länge der zurückgelegten Entfernung.
Alpha-Strahlung. Es ist ein Fluss von A-Partikeln, die die Kerne von Heliumatomen sind, manchmal als zweimal ionisierte Heliumatome genannt werden). Das Alpha-Partikel besteht aus 2 Protonen und 2 Neutronen, die positiv aufgeladen sind und mit Ihnen zwei elementare positive Ladungen mit sich bringt. Masse von Partikeln M a \u003d 4.003 A.e.M. - Es ist der größte der Partikel. Die Geschwindigkeit der Bewegung beträgt (14,1-24,9) × 10 6 m / s. In der Alpha-Teilchensubstanz bewegen Sie sich gerade, was mit einer relativ großen Masse und erheblichen Energie verbunden ist. Die Abweichung erfolgt nur mit einer Frontalkollision mit Kernen.
Die Kilometerleistung von Alphateilchen in der Substanz hängt von der Energie des Alpha-Partikels ab und der Art der Substanz, in der sie sich bewegt. Im Durchschnitt beträgt die Alpha-Partikelkilometer 2,5-9 cm, maximal - bis 11 cm, in biologischen Geweben - 5-100 μm, in Glas - 4. 10 -3 cm. Die Energie des Alpha-Partikels liegt innerhalb von 4-9 MEV. Es ist möglich, die Alpha-Strahlung mit einem Blatt Papier vollständig zu verzögern. Die gesamte Länge der Alpha-Partikelmeile kann von 116.000 bis 254.000 Paaren von Ionen erstellen.
Die spezifische Ionisation beträgt ungefähr 40.000 Paare von Ionen / cm in der Luft, die gleiche spezifische Ionisierung im Körper auf der Basis von 1-2 Mikrometer.
Nachdem der Energieverbrauch des Alpha-Partikels verlangsamt wird, stoppt der Ionisierungsprozess. Die Gesetze, die die Bildung von Atomen regulieren, treten in Kraft. Der Kernel von Heliumatomen befestigt 2 Elektronen und bildet ein vollflächiges Heliumatom. Dies erklärt die Tatsache der obligatorischen Anwesenheit von Helium in Felsen, die radioaktive Substanzen enthalten.
Von allen Arten von radioaktiven Strahlung ist Alpha-Strahlung am stärksten fluoreszierenden (Glühen).
Beta-Strahlung. - Dies ist ein Strom von Beta-Partikeln, die Elektronen oder Positionen sind. Eine elementare elektrische Ladung wird getragen, M B \u003d 0,000548 AE.M. Bewegen Sie sich mit Geschwindigkeiten in der Nähe der Lichtgeschwindigkeit, d. H. (0.87-2.994) × 10 8 m / s.
Im Gegensatz zu A-Particellen B-Partikel des gleichen radioaktiven Elements haben sie eine andere Energiereserve (von Null bis zu einem maximalen Wert). Dies ist darauf zurückzuführen, dass bei jedem Beta-Zerfall zwei Partikel vom Atomkern abgewogen werden: B-Partikel und Neutrino (N e). Energie, die an jedem Zerfallsakt freigesetzt wird, ist in unterschiedlichen Verhältnissen zwischen B-Partikel und Neutrino verteilt. So reicht die Iteration von Beta-Partikeln von den Zehntel und Hundertstel MEV (weiche B-Strahlung) bis 2-3 MEV (harte Strahlung).
Aufgrund der Tatsache, dass Beta-Partikel, die von demselben Beta-Emitter emittiert, eine andere Energiereserve (von minimal bis maximal), dann die Länge des Laufs und die Anzahl der Ionenpaare für Beta-Partikel dieses Radionukliums nicht gleich . Typischerweise ist die Kilometerleistung in der Luft Dutzende von cm, manchmal mehrere Meter (bis zu 34 m) in Biotatinen - bis zu 1 cm (bis 4 cm für Beta-Partikel energie 8 mev).
Beta-Strahlung hat einen wesentlich geringeren Ionisationswirkung als Alpha-Strahlung. In der Luft sind die Betapartikel in der Luft also aus 1000 bis 25.500 Paaren von Ionen gebildet. Im Durchschnitt auf der ganzen Wege in der Luft oder 50-100-Ionenpaare pro 1 cm-Pfad. Der Ionisierungsgrad hängt von der Geschwindigkeit des Partikels ab, desto geringer, desto größer ist die Ionisierung. Der Grund dafür liegt in der Tatsache, dass Beta-Partikel mit hoher Energien zu schnell an Atomen fliegen und keine Zeit haben, um gleiche starke Wirkung wie langsame Betapartikel zu verursachen.
Da Beta-Partikel eine sehr geringe Masse haben, dann in einer Kollision mit Atomen und Molekülen, sind sie leicht von ihrer Anfangsrichtung abgewichen. Ein solches Störungsphänomen wird als Streuung genannt. Daher ist es sehr schwierig, genau die Länge des Pfads von Beta-Partikeln und nicht einer Kilometerbahn zu bestimmen, da es zu dumm ist.
Mit dem Energieverlust wird das Elektron entweder durch ein positives Ion aufgenommen, um ein neutrales Atom oder ein Atom mit der Bildung eines negativen Ions zu bilden.
Gammastrahlung - Dies ist der Fluss von Photonen (Quanta) von elektromagnetischer Strahlung. Die Ausbreitungsgeschwindigkeit im Vakuum ist gleich der Lichtgeschwindigkeit - 3 × 10 8 m / s. Da die Gammastrahlung Welle ist, zeichnet sie sich durch eine Wellenlänge, Häufigkeit von Schwingungen und Energie aus. Die G-Quanta-Energie ist proportional zur Schwingungsfrequenz, und die Schwingungsfrequenz ist mit der Länge ihrer Welle verbunden. Je größer die Wellenlänge ist, desto weniger die Häufigkeit von Schwingungen und umgekehrt, d. H. Die Frequenz von Schwingungen ist umgekehrt proportional zur Wellenlänge. Je kleiner die Wellenlänge und eine höhere Häufigkeit von Strahlungsschwingungen, desto größer ist ihre Energie und deshalb durchdringende Fähigkeit. Die Energie der Gammastrahlung von natürlichen radioaktiven Elementen reicht von mehreren KeV bis 2-3 MEV und erreicht selten 5-6 MeV.
Gamma Quanta, ohne die Ladung und Masse des Friedens zu haben, verursachen einen schwachen ionisierenden Effekt, sondern haben eine große Durchdringungsfähigkeit. In der Luft können sie den Weg auf 100-150 m erledigen. Durch den menschlichen Körper geht diese Strahlung ohne Schwächung durch.
Messungen
Konzept der Dosis.
Das Ergebnis der Auswirkungen von ionisierender Strahlung auf die bestrahlten Objekte sind die physikalisch-ärztlichen oder biologischen Änderungen dieser Objekte. Beispiele für solche Änderungen können die Erwärmung des Körpers, der photochemischen Reaktion des Röntgenfilms, der Änderung der biologischen Indikatoren eines lebenden Organismus und dergleichen sein. Der Strahlungseffekt hängt von physikalischen Mengen ab X I.Charakterisierung des Strahlungsfelds oder der Wechselwirkung von Strahlung mit einem Stoff:
Werte X I.Funktionsweise verwandter Strahlungseffekt η , werden als dosimetric genannt. Der Zweck der Dosimetry ist das Messen, studierende und theoretische Berechnungen von Dosimetriewerten für die Vorhersage oder Bewertung des Strahlungseffekts, insbesondere der radiobiologischen Wirkung.
Das System der Dosimetry-Werte wird als Ergebnis der Entwicklung von Radiobiologie, Dosimetrie und Strahlungssicherheit gebildet. Sicherheitskriterien werden weitgehend von der Gesellschaft bestimmt, daher wurden verschiedene Systeme von Dosimetriewerten in verschiedenen Ländern gegründet. Eine wichtige Rolle bei der Vereinigung dieser Systeme wird von der internationalen Kommission zum radiologischen Schutz (MCRZ) gespielt - eine unabhängige Organisation, die Experten im Bereich der biologischen Wirkung von Strahlung, Dosimetrie und