Методы получения наноматериалов. Способ получения наноматериалов
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
Нанотехнология -- область фундаментальной и прикладной науки и техники, имеющая дело с совокупностью теоретического обоснования, практических методов исследования, анализа и синтеза, а также методов производства и применения продуктов с заданной атомной структурой путём контролируемого манипулирования отдельными атомами и молекулами.
Основой всех нано технологий является способность четырехвалентных элементов (чаще всего углерода) образовывать многоатомные, а затем и многомолекулярные структуры. Такие структуры чаще всего обладают специфическими (в зависимости от состава, формы полученной молекулы и других ее параметров) свойствами, не присущими никаким другим известным соединениям, что делает их такими интересными для науки и открывает огромные области для применения наномолекул и в целом нанотехнологий. нанотехнология техника материал
Так, например, оказалось, что наночастицы некоторых материалов имеют очень хорошие каталитические и адсорбционные свойства. Другие материалы показывают удивительные оптические свойства, например, сверхтонкие пленки органических материалов применяют для производства солнечных батарей.
В свою очередь способность четырехвалентных элементов, например, углерода, образовывать четыре связи с другими атомами объясняется с точки зрения физики наличием четырех валентных электронов на внешнем энергетическом уровне.
Конечно, следует сказать, что такое объяснение не совсем раскрывает вопрос и является скорее химическим, а не физическим. Но если капнуть дальше можно увидеть что в основе всего лежит физическое явление, которое объясняет образование связей между атомами.
Так же заметим, современное описание химической связи проводится на основе именно квантовой механики которая является разделом физики. Химическая связь определяется взаимодействием между заряженными частицами (ядрами и электронами). Такое взаимодействие называется электромагнитным.
Методы получения наноматериалов делятся на механические, физические, химические и биологические. Т.е. в основе данной классификации лежит природа процесса синтеза наноматериалов. В основе механических методов получения лежит воздействие больших деформирующих нагрузок: трения, давления, прессования, вибрации, кавитационные процессы и т.п. Физические методы получения основываются на физических превращениях: испарении, конденсации, возгонке, резком охлаждении или нагреве, распылении расплава и т.п. (Для полноты классификации и для справки) К химическим относятся методы, основным диспергирующим этапом которых являются: электролиз, восстановление, термическое разложение. Биологические методы получения основаны на использовании биохимических процессов, происходящих в белковых телах.
Механические методы Механическое воздействие при измельчении материалов является импульсным, т.е. возникновение поля напряжений и его последующая релаксация происходят не в течение всего времени пребывания частиц в реакторе, а только в момент соударения частиц и в короткое время после него. Механическое воздействие является также и локальным, так как происходит не во всей массе твёрдого вещества, а там, где возникает и затем релаксирует поле напряжений. Благодаря импульсности и локальности в небольших областях материала в течение короткого времени сосредотачиваются большие нагрузки. Это приводит к возникновению в материале дефектов, напряжений, полос сдвига, деформаций, трещин. В результате происходит измельчение вещества, ускоряется массоперенос и перемешивание компонентов, активируется химическое взаимодействие твёрдых реагентов. В результате механического истирания и механического сплавления может быть достигнута более высокая взаимная растворимость некоторых элементов в твёрдом состоянии, чем возможна в равновесных условиях. Размол проводится в шаровых, планетарных, вибрационных, вихревых, гироскопических, струйных мельницах, аттриторах. Измельчение в этих устройствах происходит в результате ударов и истирания.Разновидностью метода механического измельчения является механохимический способ. При тонком измельчении смеси различных компонентов между ними ускоряется взаимодействие. Кроме того, возможно протекание химических реакций, которые при контакте, не сопровождающемся измельчением, вообще не происходят при таких температурах. Эти реакции называются механохимическими. С целью формирования наноструктуры в объемных материалахиспользуют специальные механические схемы деформирования, которые позволяют достичь больших искажений структуры образцов при относительно низких температурах.Соответственно, к интенсивной пластической деформации относятся следующие методы:
Кручение под высоким давлением;
Равноканальное угловое прессование (РКУ-прессование);
Метод всесторонней ковки;
Равноканальная угловая вытяжка (РКУ-вытяжка);
Метод «песочных часов»;
Метод интенсивного трения скольжением.
В настоящее время большинство результатов получено первыми двумя методами. В последнее время разрабатываются методы получения наноматериалов с использованием механического воздействия различных сред. К этим способам относятся кавитационно-гидродинамический, вибрационный способы, способ ударной волны, измельчение ультразвуком и детонационный синтез.
Кавитационно-гидродинамический метод служит для получения суспензий нанопорошков в различных дисперсионных средах. Кавитация - от лат. слова «пустота» - образование в жидкости полостей (кавитационных пузырьков или каверн), заполненных газом, паром или их смесью. В ходе процесса кавитационные эффекты, вызванные образованием и разрушением парогазовых микропузырьков в жидкости в течение 10-3 - 10-5 с при давлениях порядка 100 - 1000 МПа, приводят к разогреву не только жидкостей, но и твёрдых тел. Это воздействие вызывает измельчение частиц твёрдого вещества.
Измельчение ультразвуком также основано на расклинивающем действии кавитационных ударов. В основе вибрационного метода получения наноматериалов лежит резонансная природа эффектов и явлений, которые обеспечивают минимальные энергозатраты при проведении процессов и высокую степень гомогенизации многофазных сред. Принцип действия заключается в том, что какой-либо сосуд подвергается вибрационному воздействию с определённой частотой и амплитудой.
Наночастицы алмаза можно получать детонационным синтезом. В способе используется энергия взрыва, при этом достигается давление в сотни тысяч атмосфер и температуры до нескольких тысяч градусов. Эти условия соответствуют области термодинамической устойчивости фазы алмаза. К физическим методам получения УД материалов относятся методы распыления, процессы испарения-конденсации, вакуум-сублимационная технология, методы превращений в твёрдом состоянии.
Метод распыления струи расплава жидкостью или газом заключается в том, что тонкая струя жидкого материала подается в камеру, где разбивается в мелкие капли потоком сжатого инертного газа или струей жидкости. В качестве газов в этом методе используют аргон или азот; в качестве жидкостей - воду, спирты, ацетон, ацетальдегид. Формирование наноструктур возможно способом закалки из жидкого состояния или спиннингованием. Способ состоит в получении тонких лент с помощью быстрого (не менее 106 К/с) охлаждения расплава на поверхности вращающегося диска или барабана.
Физические методы. Методы испарения-конденсации основаны на получении порошков в результате фазового перехода пар - твёрдое тело или пар - жидкость - твёрдое тело в газовом объёме либо на охлаждаемой поверхности.
Сущность метода состоит в том, что исходное вещество испаряется путём интенсивного нагрева, а затем резко охлаждается. Нагрев испаряемого материала может осуществляться различными способами: резистивным, лазерным, плазменным, электрической дугой, индукционным, ионным. Процесс испарения-конденсации можно проводить в вакууме или среде нейтрального газа. Электрический взрыв проводников проводят в аргоне или гелии при давлении 0,1 - 60 МПа. В этом методе тонкие проволочки металла диаметром 0,1 - 1 мм помещают в камеру и импульсно подают к ним ток большой силы.
Продолжительность импульса 10-5 - 10-7 с, плотность тока 104 - 106 А/мм2. При этом проволочки мгновенно разогреваются и взрываются. Образование частиц происходит в свободном полёте. Вакуум-сублимационная технология получения наноматериалов включает три основные стадии. На первой стадии готовится исходный раствор обрабатываемого вещества или нескольких веществ. Вторая стадия - замораживания раствора - имеет целью зафиксировать равномерное пространственное распределение компонентов, присущее жидкости для получения минимально возможного размера кристаллитов в твёрдой фазе. Третья стадия - удаление из замороженного раствора кристаллитов растворителя путём его возгонки.
Существует ряд методов получения наноматериалов, в которых диспергирование осуществляется в твёрдом веществе без изменения агрегатного состояния. дним из способов получения массивных наноматериалов является способ контролируемой кристаллизации из аморфного состояния. Метод предполагает получение аморфного материала закалкой из жидкого состояния, а затем в условиях контролируемого нагрева проводится кристаллизация вещества. В настоящее время наиболее распространенным методом получения углеродных нанотрубок является метод термического распыления графитовых электродов в плазме дугового разряда.
Процесс синтеза осуществляется в камере, заполненной гелием под высоким давлением. При горении плазмы происходит интенсивное термическое испарение анода, при этом на торцевой поверхности катода образуется осадок, в котором формируются нанотрубки углерода. Образующиеся многочисленные нанотрубки имеют длину порядка 40 мкм. Они нарастают на катоде перпендикулярно плоской поверхности его торца и собраны в илиндрические пучки диаметром около 50 мкм.
Пучки нанотрубок регулярно покрывают поверхность катода, образуя сотовую структуру. Ее можно обнаружить, рассматривая осадок на катоде евооруженным глазом. Пространство между пучками нанотрубок заполнено смесью неупорядоченных наночастиц и одиночных нанотрубок. Содержание нанотрубок в углеродном осадке (депозите) может приближаться к 60%.
Согласно небольшому исследованию, проведенному мной по современным технлогиям которые вводятся в производстве одежды, могу сказать, что некоторые технологии уже активно используются при создании материалов для одежды и обуви, но что касается био- и нанотехнологий, пока информации о подобных эксперементах, таких как Olivia Ong, очень мало и она достаточно редко встречается в сети. Я нашел около 10 примеров упоменания использования наноматериалов в создании одежды.
…Необычная одежда разработана японской исследовательской группой Life BEANS…
…или Кричевский Герман Евсеевич, профессор, доктор технических наук, заслуженный деятель РФ, эксперт ЮНЕСКО, академик РИА и МИА, Лауреат Госпремии МСР рассказывает в статье для сайта nanonewsnet.ru о своем опыте внедрения нанотехнологий на текстильных производствах…
…Китайские ученые создали наноткань, которая сама очищается под воздействием солнечного излучения...
…Португалии разрабатывают новые материалы и устройства, которые являются последним словом в инновациях в рамках Европейского научно-исследовательского проекта DEPHOTEX…
И несколько других упоминаний других проектов.
К сожалению, не смотря на некоторые успехи в области био- и нанотехнологий и даже конкретно области одежды, получаемая продукция остается непомерно дорогой как для производителя так и для покупателя поэтому нанотехнологичная одежда пока не готова производиться в более крупных количествах. Сегодня эта область активно развивается и остается перспективным направлением в области нанотехнологий.
По прогнозам некоторых ученых важность доступность высоких технологий в будущем будет достигаться за счет поиска рациональных методов и технологий получения различных наноматериалов и в конечном счете приведет к повсеместной замене обычных материалов на те которые были получены с применением высоких технологий.
Лидером в исследовании методов получения наноматериалов является НГТУ и ТПУ в частности кафедра Биотехнологии на базе Института Физики Высоких Технологий.
Размещено на Allbest.ru
...Подобные документы
Общие сведения о методах получения наночастиц. Основные процессы криохимической нанотехнологии. Приготовление и диспергирование растворов. Биохимические методы получения наноматериалов. Замораживание жидких капель. Сверхзвуковое истечение газов из сопла.
курсовая работа , добавлен 21.11.2010
Исследование особенностей объемных наноструктурных материалов. История развития нанотехнологий. Причины широкого интереса к нанотехнологиям и наноматериалам. Методы получения нанопорошков. Плазмохимический и криохимический синтез. Продукты криотехнологии.
презентация , добавлен 25.12.2015
Фуллерит как кристалл из больших молекул углерода Сn-фуллеренов. Знакомство с основными особенностями нанокристаллических материалов, анализ преимуществ: высокая вязкость, повышенная износостойкость. Характеристика механических свойств наноматериалов.
реферат , добавлен 20.05.2014
Группа методов количественного химического анализа, основанных на использовании электролиза (электрохимические методы анализа). Особенности электрогравиметрического метода, его сущность и применение. Основная аппаратура, метод внутреннего электролиза.
реферат , добавлен 15.11.2014
Нанокатализ как быстро развивающейся область науки, которая включает использование наноматериалов в качестве катализаторов для различных процессов катализа. Особенности производства наноразмерных катализаторов со 100% селективностью и высокой активностью.
реферат , добавлен 06.01.2014
Влияние механоактивации на геометрические параметры дисперсных материалов. Основное оборудование, используемое для седиментационного анализа материалов. Разработка установки для исследования материалов, технико-экономическое обоснование данного процесса.
дипломная работа , добавлен 16.04.2014
Понятие и назначение химических методов анализа проб, порядок их проведения и оценка эффективности. Классификация и разновидности данных методов, типы проводимых химических реакций. Прогнозирование и расчет физико-химических свойств разных материалов.
лекция , добавлен 08.05.2010
Теоретические аспекты методов. Сущность испытаний материалов на стойкость к микроскопическим грибам и к бактериям. Особенности измерения интенсивности биолюминесценции и индекса токсичности. Главные параметры оценки биостойкости строительных материалов.
реферат , добавлен 13.01.2015
Одним из наиболее перспективных и многообещающих направлений развития современной науки является нанотехнология. Исследование нанокомпозитов из керамики и полимеров, нанокомпозитов, содержащих металлы или полупроводники. Возможности нанотехнологий.
реферат , добавлен 26.01.2011
Изучение химических методов получения порошков: восстановление оксидов и солей металлов твердыми или газообразными восстановителями, диссоциация карбонилов и неустойчивых соединений, металлотермия. Извлечение железа из использованных автомобильных шин.
К настоящему времени разработано большое количество методов и способов получения наноматериалов. Это обусловлено разнообразием состава и свойств наноматериалов, с одной стороны, а с другой – позволяет расширить ассортимент данного класса веществ, создавать новые и, уникальные образцы. Формирование наноразмерных структур может происходить в ходе таких процессов, как фазовые превращения, химическое взаимодействие, рекристаллизация, аморфизация, высокие механические нагрузки, биологический синтез. Как правило, формирование наноматериалов возможно при наличии существенных отклонений от равновесных условий существования вещества, что требует создания специальных условий и, зачастую, сложного и прецизионного оборудования. Совершенствование ранее известных и разработка новых методов получения наноматериалов определило основные требования, которым они должны соответствовать, а именно:
· метод должен обеспечивать получение материала контролируемого состава с воспроизводимыми свойствами;
· метод должен обеспечивать временную стабильность наноматериалов, т.е. в первую очередь защиту поверхности частиц от самопроизвольного окисления и спекания в процессе изготовления;
· метод должен иметь высокую производительность и экономичность;
· метод должен обеспечивать получение наноматериалов с определенным размером частиц или зерен, причем их распределение по размерам должно быть, при необходимости, достаточно узким.
Следует отметить, что в настоящее время не существует метода, отвечающего в полной мере всей совокупности требований. В зависимости от способа получения такие характеристики наноматериалов, как средний размер и форма частиц, их гранулометрический состав, величина удельной поверхности, содержание в них примесей и др., могут колебаться в весьма широких пределах. Например, нанопорошки в зависимости от метода и условий изготовления могут иметь сферическую, хлопьевидную, игольчатую или губчатую форму; аморфную или мелкокристаллическую структуру. Методы получения наноматериалов делятся на механические, физические, химические и биологические. Т.е. в основе данной классификации лежит природа процесса синтеза наноматериалов. В основе механических методов получения лежит воздействие больших деформирующих нагрузок: трения, давления, прессования, вибрации, кавитационные процессы и т.п. Физические методы получения основываются на физических превращениях: испарении, конденсации, возгонке, резком охлаждении или нагреве, распылении расплава и т.п. К химическим относятся методы, основным диспергирующим этапом которых являются: электролиз, восстановление, термическое разложение. Биологические методы получения основаны на использовании биохимических процессов, происходящих в белковых телах. Методы механического измельчения применительно к наноматериалам часто называют механосинтезом. Основой механосинтеза является механическая обработка твёрдых веществ. Механическое воздействие при измельчении материалов является импульсным, т.е. возникновение поля напряжений и его последующая релаксация происходят не в течение всего времени пребывания частиц в реакторе, а только в момент соударения частиц и в короткое время после него. Механическое воздействие является также и локальным, так как происходит не во всей массе твёрдого вещества, а там, где возникает и затем релаксирует поле напряжений. Благодаря импульсности и локальности в небольших областях материала в течение короткого времени сосредотачиваются большие нагрузки. Это приводит к возникновению в материале дефектов, напряжений, полос сдвига, деформаций, трещин. В результате происходит измельчение вещества, ускоряется массоперенос и перемешивание компонентов, активируется химическое взаимодействие твёрдых реагентов. В результате механического истирания и механического сплавления может быть достигнута более высокая взаимная растворимость некоторых элементов в твёрдом состоянии, чем возможна в равновесных условиях. Размол проводится в шаровых, планетарных, вибрационных, вихревых, гироскопических, струйных мельницах, аттриторах. Измельчение в этих устройствах происходит в результате ударов и истирания. Разновидностью метода механического измельчения является механохимический способ. При тонком измельчении смеси различных компонентов между ними ускоряется взаимодействие. Кроме того, возможно протекание химических реакций, которые при контакте, не сопровождающемся измельчением, вообще не происходят при таких температурах. Эти реакции называются механохимическими. С целью формирования наноструктуры в объемных материалах используют специальные механические схемы деформирования, которые позволяют достичь больших искажений структуры образцов при относительно низких температурах. Соответственно, к интенсивной пластической деформации относятся следующие методы: – кручение под высоким давлением; – равноканальное угловое прессование (РКУ–прессование); – метод всесторонней ковки; – равноканальная угловая вытяжка (РКУ–вытяжка); – метод «песочных часов»; – метод интенсивного трения скольжением. В настоящее время большинство результатов получено первыми двумя методами. В последнее время разрабатываются методы получения наноматериалов с использованием механического воздействия различных сред. К этим способам относятся кавитационно–гидродинамический, вибрационный способы, способ ударной волны, измельчение ультразвуком и детонационный синтез. Кавитационно–гидродинамический метод служит для получения суспензий нанопорошков в различных дисперсионных средах. Кавитация – от лат. слова «пустота» – образование в жидкости полостей (кавитационных пузырьков или каверн), заполненных газом, паром или их смесью. В ходе процесса кавитационные эффекты, вызванные образованием и разрушением парогазовых микропузырьков в жидкости в течение 10–3 – 10–5 с при давлениях порядка 100 – 1000 МПа, приводят к разогреву не только жидкостей, но и твёрдых тел. Это воздействие вызывает измельчение частиц твёрдого вещества. Измельчение ультразвуком также основано на расклинивающем действии кавитационных ударов. В основе вибрационного метода получения наноматериалов лежит резонансная природа эффектов и явлений, которые обеспечивают минимальные энергозатраты при проведении процессов и высокую степень гомогенизации многофазных сред. Принцип действия заключается в том, что какой–либо сосуд подвергается вибрационному воздействию с определённой частотой и амплитудой. Наночастицы алмаза можно получать детонационным синтезом. В способе используется энергия взрыва, при этом достигается давление в сотни тысяч атмосфер и температуры до нескольких тысяч градусов. Эти условия соответствуют области термодинамической устойчивости фазы алмаза. К физическим методам получения УД материалов относятся методы распыления, процессы испарения–конденсации, вакуум–сублимационная технология, методы превращений в твёрдом состоянии. Метод распыления струи расплава жидкостью или газом заключается в том, что тонкая струя жидкого материала подается в камеру, где разбивается в мелкие капли потоком сжатого инертного газа или струей жидкости. В качестве газов в этом методе используют аргон или азот; в качестве жидкостей – воду, спирты, ацетон, ацетальдегид. Формирование наноструктур возможно способом закалки из жидкого состояния или спиннингованием. Способ состоит в получении тонких лент с помощью быстрого (не менее 106 К/с) охлаждения расплава на поверхности вращающегося диска или барабана. Физические методы. Методы испарения–конденсации основаны на получении порошков в результате фазового перехода пар – твёрдое тело или пар – жидкость – твёрдое тело в газовом объёме либо на охлаждаемой поверхности. Сущность метода состоит в том, что исходное вещество испаряется путём интенсивного нагрева, а затем резко охлаждается. Нагрев испаряемого материала может осуществляться различными способами: резистивным, лазерным, плазменным, электрической дугой, индукционным, ионным. Процесс испарения–конденсации можно проводить в вакууме или среде нейтрального газа. Электрический взрыв проводников проводят в аргоне или гелии при давлении 0,1 – 60 МПа. В этом методе тонкие проволочки металла диаметром 0,1 – 1 мм помещают в камеру и импульсно подают к ним ток большой силы. Продолжительность импульса 10–5 – 10–7 с, плотность тока 104 – 106 А/мм 2 . При этом проволочки мгновенно разогреваются и взрываются. Образование частиц происходит в свободном полёте. Вакуум–сублимационная технология получения наноматериалов включает три основные стадии. На первой стадии готовится исходный раствор обрабатываемого вещества или нескольких веществ. Вторая стадия – замораживания раствора – имеет целью зафиксировать равномерное пространственное распределение компонентов, присущее жидкости для получения минимально возможного размера кристаллитов в твёрдой фазе. Третья стадия – удаление из замороженного раствора кристаллитов растворителя путём его возгонки. Существует ряд методов получения наноматериалов, в которых диспергирование осуществляется в твёрдом веществе без изменения агрегатного состояния. Одним из способов получения массивных наноматериалов является способ контролируемой кристаллизации из аморфного состояния. Метод предполагает получение аморфного материала закалкой из жидкого состояния, а затем в условиях контролируемого нагрева проводится кристаллизация вещества. В настоящее время наиболее распространенным методом получения углеродных нанотрубок является метод термического распыления графитовых электродов в плазме дугового разряда. Процесс синтеза осуществляется в камере, заполненной гелием под высоким давлением. При горении плазмы происходит интенсивное термическое испарение анода, при этом на торцевой поверхности катода образуется осадок, в котором формируются нанотрубки углерода. Образующиеся многочисленные нанотрубки имеют длину порядка 40 мкм. Они нарастают на катоде перпендикулярно плоской поверхности его торца и собраны в цилиндрические пучки диаметром около 50 мкм. Пучки нанотрубок регулярно покрывают поверхность катода, образуя сотовую структуру. Ее можно обнаружить, рассматривая осадок на катоде невооруженным глазом. Пространство между пучками нанотрубок заполнено смесью неупорядоченных наночастиц и одиночных нанотрубок. Содержание нанотрубок в углеродном осадке (депозите) может приближаться к 60%. Химические методы получения наноразмерных материалов можно разделить на группы, в одну из которых можно отнести методы, где наноматериал получают по той или иной химической реакции, в которых участвуют определённые классы веществ. В другую можно отнести различные варианты электрохимических реакций. Метод осаждения заключается в осаждении различных соединений металлов из растворов их солей с помощью осадителей. Продуктом осаждения являются гидроксиды металлов. Регулированием рН и температуры раствора возможно создание оптимальных для получения наноматериалов условий осаждения, при которых повышаются скорости кристаллизации и образуется высокодисперсный гидроксид. Затем продукт прокаливают и, при необходимости, восстанавливают. Получаемые нанопорошки металлов имеют размер частиц от 10 до 150 нм. Форма отдельных частиц обычно близка к сферической. Однако, этим методом, варьируя параметры процесса осаждения, можно получать порошки игольчатой, чешуйчатой, неправильной формы. Золь–гельный метод первоначально был разработан для получения порошка железа. Он сочетает процесс химической очистки с процессом восстановления и основан на осаждении из водных растворов нерастворимых металлических соединений в виде геля, получаемого с помощью модификаторов (полисахаридов), с последующим их восстановлением. В частности, содержание Fe в порошке составляет 98,5 – 99,5 %. В качестве сырья можно использовать соли железа, а также отходы металлургического производства: лом металлов или отработанный травильный раствор. Благодаря использованию вторичного сырья, метод обеспечивает возможность производства чистого и дешёвого железа. Этим методом можно получать и другие классы материалов в наносостоянии: оксидную керамику, сплавы, соли металлов и др. Восстановление оксидов и других твердых соединений металлов является одним из наиболее распространенных и экономичных способов. В качестве восстановителей используются газы – водород, монооксид углерода, конвертированный природный газ, твёрдые восстановители – углерод (кокс, сажа), металлы (натрий, калий), гидриды металлов. Исходным сырьем могут быть оксиды, различные химические соединения металлов, руды и концентраты после соответствующей подготовки (обогащение, удаление примесей и т.п.), отходы и побочные продукты металлургического производства. На размер и форму получаемого порошка оказывают влияние состав и свойства исходного материала, восстановителя, а также температура и время восстановления. Сущность способа химического восстановления металлов из растворов заключается в восстановлении ионов металла из водных растворов их солей различными восстановителями: Н2, СО, гидразин, гипофосфит, формальдегид и др. В методе газофазных химических реакций синтез наноматериалов осуществляется за счёт химического взаимодействия, протекающего в атмосфере паров легколетучих соединений. Нанопорошки изготавливают также с помощью процессов термической диссоциации или пиролиза. Разложению подвергаются соли низкомолекулярных органических кислот: формиаты, оксалаты, ацетаты металлов, а также карбонаты и карбонилы металлов. Температурный интервал диссоциации составляет 200 – 400 о С. Метод электроосаждения заключаются в осаждении металлического порошка из водных растворов солей при пропускании постоянного тока. Методом электролиза получают примерно 30 металлов. Они имеют высокую чистоту, поскольку в ходе электролиза происходит рафинирование. Осаждающиеся на катоде металлы в зависимости от условий электролиза могут получаться в виде порошка или губки, дендритов, которые легко поддаются механическому измельчению. Такие порошки хорошо прессуются, что важно при производстве изделий. Наноматериалы могут производиться и в биологических системах. Как оказалось, природа использует материалы наноразмеров миллионы лет. Например, во многих случаях живые системы (некоторые бактерии, простейшие организмы и млекопитающие) производят минеральные вещества с частицами и микроскопическими структурами в нанометровом диапазоне размеров. Было установлено, что биологические наноматериалы отличаются от других, поскольку их свойства вырабатывались эволюционным путём в течение длительного времени. В процессе биоминерализации действуют механизмы тонкого биологического контроля, в результате чего производятся материалы с чётко определёнными характеристиками. Это обеспечило высокий уровень оптимизации их свойств по сравнению со многими синтетическими наноразмерными материалами. Живые организмы могут быть использованы как прямой источник наноматериалов, свойства которых могут быть изменены путём варьирования биологических условий синтеза или при переработке после извлечения. Наноматериалы, полученные биологическими методами, могут быть исходным материалом для некоторых стандартных методов синтеза и обработки наноматериалов, а также в ряде технологичеких процессов. Пока ещё работ в этой области немного, но уже есть ряд примеров, которые показывают, что в этом направлении существует значительный потенциал для будущих достижений. В настоящее время наноматериалы могут быть получены из ряда биологических объектов, а именно:
1) ферритинов и связанных с ними белков, содержащих железо;
2) магнетотактических бактерий;
3) псевдозубов некоторых моллюсков;
4) с помощью микроорганизмов путём извлечения некоторых металлов из природных соединений.
Ферритины – это класс белков, обеспечивающих для живых организмов возможность синтезировать частицы гидроксидов и оксифосфатов железа нанометрового размера. Возможно также получение нанометаллов с помощью микроорганизмов. Процессы использования микроорганизмов можно условно разделить на три группы. К первой группе относятся процессы, нашедшие применение в промышленности. Сюда входят: бактериальное выщелачивание меди из сульфидных материалов, бактериальное выщелачивание урана из руд, отделение примесей мышьяка от концентратов олова и золота. В некоторых странах в настоящее время до 5 % меди, большое количество урана и цинка получают микробиологическими методами. Ко второй группе относятся микробиологические процессы, достаточно хорошо изученные в лабораторных условиях, но не доведённые до промышленного использования. Сюда относятся процессы извлечения марганца, висмута, свинца, германия из бедных карбонатных руд. Как оказалось, с помощью микроорганизмов можно вскрывать тонко вкраплённое золото в арсенопиритных концентратах. Золото, которое относится к трудно окисляемым металлам, под воздействием некоторых бактерий образует соединения, и за счёт этого может быть извлечено из руд. К третьей группе относятся теоретически возможные процессы, требующие дополнительного изучения. Это процессы получения никеля, молибдена, титана, таллия. Считается, что в определённых условиях применение микроорганизмов может быть использовано при переработке бедных руд, отвалов, «хвостов» обогатительных фабрик, шлаков.
К настоящему времени разработано большое количество методов и способов получения наноматериалов. Это обусловлено разнообразием состава и свойств наноматериалов, с одной стороны, а с другой - позволяет расширить ассортимент данного класса веществ, создавать новые и, уникальные образцы. Формирование наноразмерных структур может происходить в ходе таких процессов, как фазовые превращения, химическое взаимодействие, рекристаллизация, аморфизация, высокие механические нагрузки, биологический синтез. Как правило, формирование наноматериалов возможно при наличии существенных отклонений от равновесных условий существования вещества, что требует создания специальных условий и, зачастую, сложного и прецизионного оборудования. Совершенствование ранее известных и разработка новых методов получения наноматериалов определило основные требования, которым они должны соответствовать, а именно:
метод должен обеспечивать получение материала контролируемого состава с воспроизводимыми свойствами;
метод должен обеспечивать временную стабильность наноматериалов, т.е. в первую очередь защиту поверхности частиц от самопроизвольного окисления и спекания в процессе изготовления;
метод должен иметь высокую производительность и экономичность;
метод должен обеспечивать получение наноматериалов с определенным размером частиц или зерен, причем их распределение по размерам должно быть, при необходимости, достаточно узким.
Следует отметить, что в настоящее время не существует метода, отвечающего в полной мере всей совокупности требований. В зависимости от способа получения такие характеристики наноматериалов, как средний размер и форма частиц, их гранулометрический состав, величина удельной поверхности, содержание в них примесей и др., могут колебаться в весьма широких пределах. Например, нанопорошки в зависимости от метода и условий изготовления могут иметь сферическую, хлопьевидную, игольчатую или губчатую форму; аморфную или мелкокристаллическую структуру. Методы получения наноматериалов делятся на механические, физические, химические и биологические. Т.е. в основе данной классификации лежит природа процесса синтеза наноматериалов. В основе механических методов получения лежит воздействие больших деформирующих нагрузок: трения, давления, прессования, вибрации, кавитационные процессы и т.п. Физические методы получения основываются на физических превращениях: испарении, конденсации, возгонке, резком охлаждении или нагреве, распылении расплава и т.п. К химическим относятся методы, основным диспергирующим этапом которых являются: электролиз, восстановление, термическое разложение. Биологические методы получения основаны на использовании биохимических процессов, происходящих в белковых телах. Методы механического измельчения применительно к наноматериалам часто называют механосинтезом. Основой механосинтеза является механическая обработка твёрдых веществ. Механическое воздействие при измельчении материалов является импульсным, т.е. возникновение поля напряжений и его последующая релаксация происходят не в течение всего времени пребывания частиц в реакторе, а только в момент соударения частиц и в короткое время после него. Механическое воздействие является также и локальным, так как происходит не во всей массе твёрдого вещества, а там, где возникает и затем релаксирует поле напряжений. Благодаря импульсности и локальности в небольших областях материала в течение короткого времени сосредотачиваются большие нагрузки. Это приводит к возникновению в материале дефектов, напряжений, полос сдвига, деформаций, трещин. В результате происходит измельчение вещества, ускоряется массоперенос и перемешивание компонентов, активируется химическое взаимодействие твёрдых реагентов. В результате механического истирания и механического сплавления может быть достигнута более высокая взаимная растворимость некоторых элементов в твёрдом состоянии, чем возможна в равновесных условиях. Размол проводится в шаровых, планетарных, вибрационных, вихревых, гироскопических, струйных мельницах, аттриторах. Измельчение в этих устройствах происходит в результате ударов и истирания. Разновидностью метода механического измельчения является механохимический способ. При тонком измельчении смеси различных компонентов между ними ускоряется взаимодействие. Кроме того, возможно протекание химических реакций, которые при контакте, не сопровождающемся измельчением, вообще не происходят при таких температурах. Эти реакции называются механохимическими. С целью формирования наноструктуры в объемных материалах используют специальные механические схемы деформирования, которые позволяют достичь больших искажений структуры образцов при относительно низких температурах. Соответственно, к интенсивной пластической деформации относятся следующие методы: - кручение под высоким давлением; - равноканальное угловое прессование (РКУ-прессование); - метод всесторонней ковки; - равноканальная угловая вытяжка (РКУ-вытяжка); - метод «песочных часов»; - метод интенсивного трения скольжением. В настоящее время большинство результатов получено первыми двумя методами. В последнее время разрабатываются методы получения наноматериалов с использованием механического воздействия различных сред. К этим способам относятся кавитационно-гидродинамический, вибрационный способы, способ ударной волны, измельчение ультразвуком и детонационный синтез. Кавитационно-гидродинамический метод служит для получения суспензий нанопорошков в различных дисперсионных средах. Кавитация - от лат. слова «пустота» - образование в жидкости полостей (кавитационных пузырьков или каверн), заполненных газом, паром или их смесью. В ходе процесса кавитационные эффекты, вызванные образованием и разрушением парогазовых микропузырьков в жидкости в течение 10-3 - 10-5 с при давлениях порядка 100 - 1000 МПа, приводят к разогреву не только жидкостей, но и твёрдых тел. Это воздействие вызывает измельчение частиц твёрдого вещества. Измельчение ультразвуком также основано на расклинивающем действии кавитационных ударов. В основе вибрационного метода получения наноматериалов лежит резонансная природа эффектов и явлений, которые обеспечивают минимальные энергозатраты при проведении процессов и высокую степень гомогенизации многофазных сред. Принцип действия заключается в том, что какой-либо сосуд подвергается вибрационному воздействию с определённой частотой и амплитудой. Наночастицы алмаза можно получать детонационным синтезом. В способе используется энергия взрыва, при этом достигается давление в сотни тысяч атмосфер и температуры до нескольких тысяч градусов. Эти условия соответствуют области термодинамической устойчивости фазы алмаза. К физическим методам получения УД материалов относятся методы распыления, процессы испарения-конденсации, вакуум-сублимационная технология, методы превращений в твёрдом состоянии. Метод распыления струи расплава жидкостью или газом заключается в том, что тонкая струя жидкого материала подается в камеру, где разбивается в мелкие капли потоком сжатого инертного газа или струей жидкости. В качестве газов в этом методе используют аргон или азот; в качестве жидкостей - воду, спирты, ацетон, ацетальдегид. Формирование наноструктур возможно способом закалки из жидкого состояния или спиннингованием. Способ состоит в получении тонких лент с помощью быстрого (не менее 106 К/с) охлаждения расплава на поверхности вращающегося диска или барабана. Физические методы. Методы испарения-конденсации основаны на получении порошков в результате фазового перехода пар - твёрдое тело или пар - жидкость - твёрдое тело в газовом объёме либо на охлаждаемой поверхности. Сущность метода состоит в том, что исходное вещество испаряется путём интенсивного нагрева, а затем резко охлаждается. Нагрев испаряемого материала может осуществляться различными способами: резистивным, лазерным, плазменным, электрической дугой, индукционным, ионным. Процесс испарения-конденсации можно проводить в вакууме или среде нейтрального газа. Электрический взрыв проводников проводят в аргоне или гелии при давлении 0,1 - 60 МПа. В этом методе тонкие проволочки металла диаметром 0,1 - 1 мм помещают в камеру и импульсно подают к ним ток большой силы. Продолжительность импульса 10-5 - 10-7 с, плотность тока 104 - 106 А/мм 2 . При этом проволочки мгновенно разогреваются и взрываются. Образование частиц происходит в свободном полёте. Вакуум-сублимационная технология получения наноматериалов включает три основные стадии. На первой стадии готовится исходный раствор обрабатываемого вещества или нескольких веществ. Вторая стадия - замораживания раствора - имеет целью зафиксировать равномерное пространственное распределение компонентов, присущее жидкости для получения минимально возможного размера кристаллитов в твёрдой фазе. Третья стадия - удаление из замороженного раствора кристаллитов растворителя путём его возгонки. Существует ряд методов получения наноматериалов, в которых диспергирование осуществляется в твёрдом веществе без изменения агрегатного состояния. Одним из способов получения массивных наноматериалов является способ контролируемой кристаллизации из аморфного состояния. Метод предполагает получение аморфного материала закалкой из жидкого состояния, а затем в условиях контролируемого нагрева проводится кристаллизация вещества. В настоящее время наиболее распространенным методом получения углеродных нанотрубок является метод термического распыления графитовых электродов в плазме дугового разряда. Процесс синтеза осуществляется в камере, заполненной гелием под высоким давлением. При горении плазмы происходит интенсивное термическое испарение анода, при этом на торцевой поверхности катода образуется осадок, в котором формируются нанотрубки углерода. Образующиеся многочисленные нанотрубки имеют длину порядка 40 мкм. Они нарастают на катоде перпендикулярно плоской поверхности его торца и собраны в цилиндрические пучки диаметром около 50 мкм. Пучки нанотрубок регулярно покрывают поверхность катода, образуя сотовую структуру. Ее можно обнаружить, рассматривая осадок на катоде невооруженным глазом. Пространство между пучками нанотрубок заполнено смесью неупорядоченных наночастиц и одиночных нанотрубок. Содержание нанотрубок в углеродном осадке (депозите) может приближаться к 60%. Химические методы получения наноразмерных материалов можно разделить на группы, в одну из которых можно отнести методы, где наноматериал получают по той или иной химической реакции, в которых участвуют определённые классы веществ. В другую можно отнести различные варианты электрохимических реакций. Метод осаждения заключается в осаждении различных соединений металлов из растворов их солей с помощью осадителей. Продуктом осаждения являются гидроксиды металлов. Регулированием рН и температуры раствора возможно создание оптимальных для получения наноматериалов условий осаждения, при которых повышаются скорости кристаллизации и образуется высокодисперсный гидроксид. Затем продукт прокаливают и, при необходимости, восстанавливают. Получаемые нанопорошки металлов имеют размер частиц от 10 до 150 нм. Форма отдельных частиц обычно близка к сферической. Однако, этим методом, варьируя параметры процесса осаждения, можно получать порошки игольчатой, чешуйчатой, неправильной формы. Золь-гельный метод первоначально был разработан для получения порошка железа. Он сочетает процесс химической очистки с процессом восстановления и основан на осаждении из водных растворов нерастворимых металлических соединений в виде геля, получаемого с помощью модификаторов (полисахаридов), с последующим их восстановлением. В частности, содержание Fe в порошке составляет 98,5 - 99,5 %. В качестве сырья можно использовать соли железа, а также отходы металлургического производства: лом металлов или отработанный травильный раствор. Благодаря использованию вторичного сырья, метод обеспечивает возможность производства чистого и дешёвого железа. Этим методом можно получать и другие классы материалов в наносостоянии: оксидную керамику, сплавы, соли металлов и др. Восстановление оксидов и других твердых соединений металлов является одним из наиболее распространенных и экономичных способов. В качестве восстановителей используются газы - водород, монооксид углерода, конвертированный природный газ, твёрдые восстановители - углерод (кокс, сажа), металлы (натрий, калий), гидриды металлов. Исходным сырьем могут быть оксиды, различные химические соединения металлов, руды и концентраты после соответствующей подготовки (обогащение, удаление примесей и т.п.), отходы и побочные продукты металлургического производства. На размер и форму получаемого порошка оказывают влияние состав и свойства исходного материала, восстановителя, а также температура и время восстановления. Сущность способа химического восстановления металлов из растворов заключается в восстановлении ионов металла из водных растворов их солей различными восстановителями: Н2, СО, гидразин, гипофосфит, формальдегид и др. В методе газофазных химических реакций синтез наноматериалов осуществляется за счёт химического взаимодействия, протекающего в атмосфере паров легколетучих соединений. Нанопорошки изготавливают также с помощью процессов термической диссоциации или пиролиза. Разложению подвергаются соли низкомолекулярных органических кислот: формиаты, оксалаты, ацетаты металлов, а также карбонаты и карбонилы металлов. Температурный интервал диссоциации составляет 200 - 400 о С. Метод электроосаждения заключаются в осаждении металлического порошка из водных растворов солей при пропускании постоянного тока. Методом электролиза получают примерно 30 металлов. Они имеют высокую чистоту, поскольку в ходе электролиза происходит рафинирование. Осаждающиеся на катоде металлы в зависимости от условий электролиза могут получаться в виде порошка или губки, дендритов, которые легко поддаются механическому измельчению. Такие порошки хорошо прессуются, что важно при производстве изделий. Наноматериалы могут производиться и в биологических системах. Как оказалось, природа использует материалы наноразмеров миллионы лет. Например, во многих случаях живые системы (некоторые бактерии, простейшие организмы и млекопитающие) производят минеральные вещества с частицами и микроскопическими структурами в нанометровом диапазоне размеров. Было установлено, что биологические наноматериалы отличаются от других, поскольку их свойства вырабатывались эволюционным путём в течение длительного времени. В процессе биоминерализации действуют механизмы тонкого биологического контроля, в результате чего производятся материалы с чётко определёнными характеристиками. Это обеспечило высокий уровень оптимизации их свойств по сравнению со многими синтетическими наноразмерными материалами. Живые организмы могут быть использованы как прямой источник наноматериалов, свойства которых могут быть изменены путём варьирования биологических условий синтеза или при переработке после извлечения. Наноматериалы, полученные биологическими методами, могут быть исходным материалом для некоторых стандартных методов синтеза и обработки наноматериалов, а также в ряде технологичеких процессов. Пока ещё работ в этой области немного, но уже есть ряд примеров, которые показывают, что в этом направлении существует значительный потенциал для будущих достижений. В настоящее время наноматериалы могут быть получены из ряда биологических объектов, а именно:
- 1) ферритинов и связанных с ними белков, содержащих железо;
- 2) магнетотактических бактерий;
- 3) псевдозубов некоторых моллюсков;
- 4) с помощью микроорганизмов путём извлечения некоторых металлов из природных соединений.
Ферритины - это класс белков, обеспечивающих для живых организмов возможность синтезировать частицы гидроксидов и оксифосфатов железа нанометрового размера. Возможно также получение нанометаллов с помощью микроорганизмов. Процессы использования микроорганизмов можно условно разделить на три группы. К первой группе относятся процессы, нашедшие применение в промышленности. Сюда входят: бактериальное выщелачивание меди из сульфидных материалов, бактериальное выщелачивание урана из руд, отделение примесей мышьяка от концентратов олова и золота. В некоторых странах в настоящее время до 5 % меди, большое количество урана и цинка получают микробиологическими методами. Ко второй группе относятся микробиологические процессы, достаточно хорошо изученные в лабораторных условиях, но не доведённые до промышленного использования. Сюда относятся процессы извлечения марганца, висмута, свинца, германия из бедных карбонатных руд. Как оказалось, с помощью микроорганизмов можно вскрывать тонко вкраплённое золото в арсенопиритных концентратах. Золото, которое относится к трудно окисляемым металлам, под воздействием некоторых бактерий образует соединения, и за счёт этого может быть извлечено из руд. К третьей группе относятся теоретически возможные процессы, требующие дополнительного изучения. Это процессы получения никеля, молибдена, титана, таллия. Считается, что в определённых условиях применение микроорганизмов может быть использовано при переработке бедных руд, отвалов, «хвостов» обогатительных фабрик, шлаков.
К настоящему моменту известны десятки методов создания наноструктурированных материалов. Принципиально все методы получения наноструктур возможно условно разделить на два больших класса – физические и химические методы . При этом нужно подчеркнуть, что подход «снизу-вверх» характерен в большей степени для химических методов получения. Процессы получения наноматериалов включают как этап их синтеза, так и этап их стабилизации. Учитывая так же, что наноструктуры проявляют свои уникальные свойства в большинстве случаев именно в неравновесном метастабильном состоянии. Использование различных стабилизаторов позволяет не только синтезировать наноструктуры, но и использовать наноматериалы на их основе в нанотехнологии.
1 группа методов получения и изучения наночастиц (конденсация при сверхнизких температурах, варианты химического, фотохимического и радиационного восстановления, лазерное испарение) не позволяет создавать новые материалы.
П группа методов позволяет получать на основе наночастиц наноматериалы и нанокомпозиты (варианты механохимического дробления, конденсация из газовой фазы, плазмохимические методы и др.)
Структура наночастиц одних и тех же размеров, получаемых диспергированием и путем построения из атомов, может различаться. В первом случае в структуре частиц сохраняется структура исходного образца. Наночастицы, полученные путем агрегации атомов, могут иметь другое пространственное расположение атомов. Например, при размере 2-4 нм наблюдается уменьшение параметра решетки
Физические методы.
1. Плазменное напыление: плазменное, анодное, магнетронное и т.д. в зависимости от способа создания газовой среды, осаждаемой на подложку или уносимую из зоны реакции, например газовым потоком.
2. Ионно-лучевая эпитаксия.
3. Газофазное компактирование.
4. Методы лазерного испарения.
5. Контролируемая кристаллизация.
6. Диспергирование и измельчение.
7. Пластическая деформация.
Одним из основных методов получения наночастиц металлов является процесс, основанный на сочетании испарения металла в поток инертного газа с последующей конденсацией в камере, находящейся при определенной температуре.
Испарение происходит путем низкотемпературной плазмы, молекулярных пучков и газового испарения, катодного распыления, ударной волны, электровзрыва, лазерной электродисперсии, сверхзвуковой струи, различных методов механического диспергирования.
На начальном этапе исходное вещество испаряют, применяя подходящие методы нагрева. Пары вещества разбавляют большим избытком потока инертного газа. Обычно используют аргон или ксенон. Полученную паро-газовую смесь направляют на поверхность образца (подложку), охлажденную до низких температур (обычно 4-77 К). Формирование наночастиц на поверхности подложки является неравновесным процессом зависит от ряда факторов, например: температуры охлаждаемой подложки, степени разбавления инертным газом, скорости достижения поверхности подложки, скорости конденсации и т.д. Получение наночастиц методом соконденсации нескольких веществ на охлаждаемой поверхности позволяет легко вводить в их состав различные добавки, а в процессе контролируемого нагрева, увеличивая подвижность наночастиц, осуществлять ряд новых и необычных химических синтезов.
Для синтеза наноструктурированных материалов методом химической соконденсации разработан ряд специальных криореакторов. На криореакторах, созданных в РФ, США и Японии получают наноматериалы, используемые в качестве катализаторов, ферромагнетиков, пленочных материалов, антикоррозионных покрытий. Например, на одной из установок два металла испаряют в вакууме и конденсируют на подложку, охлаждаемую жидким азотом. Образовавшийся конденсат спрессовывают при высоком давлении и превращают в биметаллический нанокомпозит.
В установке плазменного осаждения в зону плазмы вместе с инертным газом – носителем вводятся соединения металла. В зоне плазмы образуются наночастицы, которые при выходе из зоны плазмы контактируют с органическим мономером и образуют стабилизированные полимером наночастицы оксидов, нитридов, карбидов металлов.
Методами ионно-лучевой имплантации получают упорядоченные наноструктуры из квантовых точек, называемых гетероструктурами. Подобные гетероструктуры могут быть использованы в качестве сенсоров, логических устройств, лазерных источников нового поколения.
В установках ионно-лучевой имплантации систему из квантовых точек покрывают слоем инертного материала, а затем снова наносят основной активный материал второго слоя. В этом втором слое происходит самосборка квантовых точек, связанных с положением в первом слое активного материала. Многократное напыление приводит к получению требуемой гетероструктуры.
При газофазном получении наноматериалов частицы металлов из тигля – испарителя направляются на фильтр, с которого они удаляются потоком газа. В результате компактирования – укрупнения наночастиц возможно серийное получение нанопористых материалов.
В случае использования метода лазерного испарения для нанесения покрытия на различные частицы используются различные лазеры, работающие в импульсном или непрерывном режимах.
Наноматериалы можно получать и модернизированным методом Вернеля, когда сверхлегкий порошок («пудра») обрабатываемого материала пропускается через факел из горючего газа (водородно-кислородное), или плазму безэлектродного высокочастотного или электродного разрядов. В пламени образуются наночастицы оксидов металлов, которые в виде порошка (~50 нм) осаждаются на охлаждаемой подложке. На базе такой технологии уже получены покрытия, не уступающие по твердости алмазу, резко увеличивающие износостойкость режущих поверхностей, их жаростойкость и коррозионную устойчивость.
Химические методы. К основным химическим методам получения наноматериалов относятся следующие:
· химическая конденсация паров;
· получение золей путем жидкофазного восстановления (в том числе электрохимическое осаждение и синтез в нанореакторах);
· радиолиз;
· матричный синтез.
Получение золей.
Фарадей получил агрегативно устойчивые золи золота (с частицами 2 – 50 нм) восстановлением разбавленной соли золота жёлтым фосфором.
AuCl 3 + 3H 2 O + P ® Au + P(OH) 3 + 3HCl.
Позже Зигмонди разработал методы (ставшие классическими) синтеза монодисперсных золей золота с заданной степенью дисперсности восстановлением золота пероксидом водорода и формальдегидом.
2 HАuCl 4 + 3H 2 O 2 ® 2 Au + 8HCl + 3O 2 ,
2 HАuCl 4 + 3HCHO + 11KOH ® 2Au + 3HCOOK + 8KCl + 8H 2 O
Процесс протекает в две стадии. Сначала формируются зародыши новой фазы, а затем в золе создаётся слабое пересыщение, при котором уже не происходит образования новых зародышей, а идёт только их рост. Таким способом можно получить жёлтые (d ~ 20 нм), красные (d ~ 40 нм) и синие (d ~ 100 нм) золи золота.
В настоящее время для получения наночастиц золота – используются три раствора:
1. золотохлористо-водородная кислота в воде
2. карбонат натрия в воде
3. гипофосфит в диэтиловом эфире.
Смесь растворов час выдерживают при 70 0 С
Размер частиц золота – 2-5 нм
Недостаток: большое количество примесей, уменьшить которые можно восстановлением системы водородом.
Химическое восстановление осуществляется в термодинамически и кинетически нестабильных системах. На процесс влияют подбор пары восстановитель-окислитель, их концентрации, температура, рН среды, диффузные и сорбционные характеристики.
Сейчас выбирают процессы, в которых восстановитель одновременно выполняет и функции стабилизатора (N-S- содержащие ПАВ, тиолы, соли нитратов и др.).
В качестве восстановителя наиболее распространены тетрабораты щелочных металлов(МВН 4), которые восстанавливают в водных средах в широком диапазоне рН почти все катионы (высокий редокс-потенциал – 1,24 В в щелочной среде). Восстановление ионов металла идет с участием комплексов с мостиковыми связями М…Н….В. Это способствует последующему переносу атомов водорода и разрыву мостиковой связи, окислительно-восстановительному процессу и разрыву связи В-Н с образованием ВН 3 . Последний гидролизуется или каталитически разлагается на поверхности частиц металлов.
Широкое распространение метода жидкофазного восстановления вызвано его относительной простотой. Химическое восстановление зависит как от природы пары восстановитель-окислитель, итак и от их концентрации, pH среды, температуры, свойств растворителя. В качестве восстановителей ионов металлов чаще всего используют – борогидриды (например, NaBH 4), алюмогидриды, соли щавелевой и винной кислот, формальдегид в водных и неводных средах.
Например, наночастицы серебра (Ag) размером менее 5 нм получены восстановлением азотнокислого серебра (AgNO 3) борогидридом натрия (NaBH 4) .
Сферические наночастицы серебра размером 3-5 нм синтезированы восстановлением AgNO 3 боргидридом натрия в присутствии четвертичных солей дисульфида аммония при смешивании соответствующих растворов при определенном температурном режиме:
Полученные частицы характеризуются интенсивным оптическим поглощением в области 400 нм, что свидетельствует о металлической природе частиц. При рН=5-9 в водной среде частицы стабильны в течение недели. Увеличение или уменьшение рН приводит к быстрой агрегации и осаждению частиц серебра.
Соли платины при восстановлении боргидридом натрия дают частицы радиусом 2-3 нм, при восстановлении гидразином – 40 нм. В качестве наноструктурированных сред использовались полиэлектролитные гели с противоположно заряженными ПАВ.
Наночастицы 1-2 нм получены при нагревании гидроокиси в этиленгликоле
Перспективной разновидностью является электрохимическое восстановление. Электрохимическое восстановление металлов позволяет, изменяя параметры электродных процессов, в широких пределах варьировать свойства получаемых нанокластеров. Например, при катодном восстановлении металлов:
На платиновых катодах могут образовываться сферические наночастицы металлов, а на катодах из алюминия – формируются пленки наноразмеров.
Наночастицы серебра 2-7 нм получены при электрохимическом растворении анода(пластины серебра в апротонном растворе тетрабутиламмонийбромида в ацетонитриле). При высоких плотностях тока образуются частицы неправильной формы. При плотности тока от -1,35 до – 6,90 мА. см -2 диаметр сфер меняется от 6 до 1,7 нм. Это при платиновом катоде. На катоде из А1 формируются и осаждаются только пленки
К настоящему времени разработано большое количество методов синтеза наночастиц.. Например, золь гидроксида железа может быть получен по реакции:
FeCl 3 + 3H 2 O T (90 – 100º C ) « Fe (OH) 3 + 3HCl
При таком получении золей важно тщательно соблюдать условия проведения реакции, в частности, необходимы строгий контроль рН и присутствие ряда органических соединений в системе. Так, размер частиц Fe 2 O 3 , получаемых в результате гидролиза FeCl 3 , зависит от концентрации триэтаноламина, изопропиламина и пиперазина.
Для контроля процессов формирования и стабилизации наночастиц используют эмульсии и мицеллы и молекулы органических веществ больших размеров – макромолекулы (дендримеры),. Дендримеры, эмульсии, мицеллы можно рассматривать как нанореакторы, позволяющие синтезировать наночастицы требуемых размеров и формы.
Наличие в ультрадисперсных системах большого избытка энергии, связанного с высокоразвитой межфазной поверхностью раздела, способствует протеканию процессов агрегирования коллоидных частиц. Для получения частиц заданной дисперсности необходимо вовремя остановить рост частиц. С этой целью поверхность частиц дисперсной фазы ингибируют за счёт образования на ней защитного слоя из ПАВ или за счёт образования на ней комплексных соединений.
Уникальным объектом химии являются ПАВ – органические вещества (синтетические и природные), обладающие ограниченной растворимостью в воде и способные адсорбироваться на поверхности раздела фаз, снижая межфазное натяжение. Эти вещества имеют дифильное строение: молекула или ион ПАВ содержит гидрофобную часть и полярную группу той или иной природы. Гидрофобная часть представляет углеводородный радикал (C n H 2 n+1 , С n H 2 n–1 , С n H 2 n+1 , C 6 H 4 и другие), содержащий от 8 до 18 углеродных атомов. В зависимости от природы гидрофильной группы ПАВ делят на катионные (к ним относятся первичные, вторичные, третичные амины и четвертичные аммониевые основания), анионные (молекулы этих соединений содержат карбоксильные, сульфоэфирные, сульфогруппы и другие). Специфика поведения ПАВ в водных растворах связана с особенностями взаимодействия между молекулами воды и ПАВ. Согласно многочисленным исследованиям, вода при комнатной температуре является структурированной жидкостью, структура которой подобна структуре льда, но в отличие от льда вода имеет только ближний порядок (r< 0,8 нм). При растворении ПАВ происходит дальнейшее структурирование молекул воды вокруг неполярных углеводородных радикалов ПАВ, что приводит к уменьшению энтропии системы. Поскольку система стремится к максимуму энтропии, то при достижении определённой концентрации, называемой критической концентрацией мицеллообразования (ККМ), молекулы или ионы ПАВ начинают самопроизвольно образовывать ассоциаты, которые называются мицеллами (по предложению открывшего их учёного Мак-Бэна, 1913 г.). Образование мицелл сопровождается высвобождением части структурированной воды, что является термодинамически выгодным процессом, поскольку он приводит к увеличению энтропии системы.
Образование мицелл фиксируется обычно по изменению какого-либо физического свойства раствора ПАВ (например, поверхностного натяжения, электропроводности, плотности, вязкости, светорассеяния и т. д.) в зависимости от концентрации ПАВ. Величина ККМ зависит от целого ряда факторов: природы ПАВ, длины и степени разветвления углеводородного радикала, присутствия электролитов или других органических соединений, рН раствора. Однако основным фактором является соотношение между гидрофильными и гидрофобными свойствами ПАВ. Так, чем длиннее углеводородный радикал и слабее полярная группа, тем меньше величина ККМ
При концентрациях, близких к ККМ, мицеллы представляют собой примерно сферические образования, в которых полярные группы контактируют с водой, а гидрофобные радикалы находятся внутри, образуя неполярное ядро. Молекулы или ионы, входящие в состав мицеллы, находятся в динамическом равновесии с объёмом раствора. Это является одной из причин «шероховатости» внешней поверхности мицелл. Степень гидратации полярных групп, структура гидратного слоя, а также структура внутреннего ядра зависят от природы ПАВ.
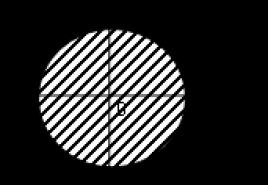
При концентрациях ПАВ, больших ККМ, возможно образование нескольких типов мицелл (рис. 4.1), различающихся по форме: сферические, цилиндрические, гексагонально упакованные, ламеллярные. Таким образом, мицеллы можно рассматривать как одномерные, двумерные и объёмные нанообъекты. В зависимости от природы ПАВ числа агрегации (n ) могут изменяться от десятков до нескольких сотен, при этом будут меняться и размеры мицелл.
Нерастворимые в воде молекулы ПАВ с длинным углеводородным радикалом и слабой полярной группой могут растворяться в неполярных жидких фазах. В этом случае при определённой концентрации ПАВ также наблюдается образование мицелл, которое обусловлено специфическими взаимодействиями между полярными группами ПАВ. Такие мицеллы называют обратными. Форма обратных мицелл зависит от концентрации ПАВ и может быть различной.
Существует два подхода к описанию процесса мицеллобразования. Согласно первому подходу (квазихимическая модель), образование мицелл рассматривается с позиций закона действующих масс. Другой подход трактует появление мицелл как возникновение новой фазы
Одним из важных свойств мицеллярных систем является их способность солюбилизировать – значительно увеличивать растворимость углеводородов в водных мицеллярных растворах или, соответственно, полярных жидкостей в обратных мицеллярных системах.
Рис. 4.1 - Структуры, возникающие в растворах ПАВ .
1 – мономеры, 2 – мицелла, 3 – цилиндрическая мицелла, 4 – гексагонально упакованные цилиндрические мицеллы, 5 – ламинарная мицелла, 6 – гексагонально упакованные капли воды в обратной мицеллярной системе.
В результате солюбилизации образуются термодинамически устойчивые равновесные изотропные системы, называемые микроэмульсионными . Многообразие факторов, влияющих на солюбилизацию (природа контактирующих фаз и ПАВ, присутствие электролитов, температура), приводит к тому, что максимальная растворимость веществ в мицеллах ПАВ может изменяться в очень широких пределах. Следует отметить, что свойства вещества при солюбилизации сильно изменяются, в результате чего скорость химических реакций, протекающих в этих системах, также может меняться. Это явление, известное как мицеллярный катализ, находит широкое применение в химии, биологии, медицине, различных технологических процессах. Например, увеличение реакционной способности веществ широко используется в процессах эмульсионной полимеризации и ферментативного катализа.
Микроэмульсии – это термодинамически стабильные изотропные дисперсии двух несмешивающихся жидкостей. При смешивании таких жидкостей капли одной из них, стабилизированные межфазной плёнкой ПАВ и со-ПАВ, в качестве которой используются низкомолекулярные спирты, распределяются в другой. Микроэмульсии относятся к лиофильным дисперсным системам и могут быть получены либо путём самопроизвольного диспергирования двух несмешивающихся жидкостей в результате сильного снижения межфазного натяжения, либо в процессе солюбилизации. Термодинамическая стабильность микроэмульсионных систем обусловлена низким межфазным натяжением, которое может составлять 10 – 5 мДж. м – 2 для ионных ПАВ и 10 – 4 мДж. м – 2 для неионогенных ПАВ. В зависимости от того, какая фаза является дисперсной, а какая непрерывной, микроэмульсии могут быть прямыми – масло в воде (м/в) – или обратными – вода в масле (в/м). Термин «масло» означает неполярную органическую жидкость. В обоих случаях дисперсная фаза состоит из капель, размер которых не превышает 100 нм.
Как правило, микроэмульсии являются многокомпонентными системами, состоящими из различных структур (бислойных, цилиндрических, сферических мицелл). В процессе мицеллообразования помимо жидких изотропных мицеллярных фаз образуются оптически анизотропные мицеллярные фазы, например, слоистые смектические и гексагональные фазы, состоящие из палочкообразных агрегатов бесконечной длины, то есть микроэмульсии обладают внутренней микроструктурой. В том случае, когда содержание воды и масла в системе сопоставимо, возможно образование биконтинуальных систем.
Свойства микроэмульсий во многом определяются размером и формой частиц дисперсной фазы, а также реологическими свойствами межфазных адсорбционных слоёв, образованных ПАВ. Поскольку микроэмульсии обладают большой подвижностью и большой поверхностью раздела между фазами, они могут служить универсальной средой, в том числе и для получения твёрдых наночастиц.
В микроэмульсионной системе частицы дисперсной фазы постоянно сталкиваются, коалесцируют и разрушаются вновь, что приводит к непрерывному обмену их содержимым. Процесс столкновения капель зависит от диффузии капель в масляной фазе (для обратной микроэмульсионной системы), тогда как процесс обмена определяется взаимодействием адсорбционных слоёв ПАВ и гибкостью межфазной поверхности (последнее обстоятельство является чрезвычайно важным при проведении химических реакций в таких системах) .

Рис. 4.2 - Схема реакции, протекающей в обратной микроэмульсионной системе.
Обратные микроэмульсионные системы часто используются для получения твёрдых наночастиц. С этой целью смешиваются две идентичные микроэмульсионные системы в/м, водные фазы которых содержат вещества А и В, образующие в ходе химической реакции труднорастворимое соединение С. При коалесценции капель в них в результате обмена веществом образуется новое соединение С (рис. 4.2). Размеры частиц новой фазы будут ограничены размером капель полярной фазы.
Наночастицы металлов могут быть получены также при введении в микроэмульсию, содержащую соль металла, восстановителя (например, водорода или гидразина) или при пропускании газа (например, СО или H 2 S) через эмульсию. Именно таким способом (восстановлением соли соответствующего металла или гидразином) впервые были получены получены монодисперсные металлические частицы Pt, Pd, Rh и Ir (с размером частиц 3 – 5 нм). Аналогичный метод был использован для синтеза биметаллических наночастиц платины и палладия.
В настоящее время реакции осаждения в микроэмульсионных системах широко применяются для синтеза металлических наночастиц, полупроводников, монодисперсных частиц SiO 2 , высокотемпературной керамики.
Несмотря на то, что механизм образования наночастиц окончательно не установлен, можно выделить ряд факторов, влияющих на протекание реакции. Это прежде всего соотношение водной фазы и ПАВ в системе (W = /[ПАВ]), структура и свойства солюбилизированной водной фазы, динамическое поведение микроэмульсий, средняя концентрация реагирующих веществ в водной фазе. На размер капель дисперсной фазы оказывает также влияние природа ПАВ, являющихся стабилизаторами микроэмульсионной системы. Однако во всех случаях размер наночастиц, образующихся в процессах реакции, контролируется размером капель исходной эмульсии. Так, размер наночастиц CdS практически линейно возрастает с увеличением соотношения W. Вместе с тем размер частиц, полученных в обратной микроэмульсионной системе, стабилизированной ди(этилгексил)сульфосукцинатом натрия (Aerosol OT), оказывается меньше, чем в системе, стабилизированной неионогенным ПАВ Triton X-100 (n -(трет -октил)фениловый эфир полиэтиленгликоля с n = 10).
Микроэмульсионные системы используются и для проведения реакций гидролиза. Примером служит реакция гидролиза тетраэтоксисилана в обратной мицеллярной системе, стабилизированной Aerosol OT
Si (Oet) 4 + 2H 2 O ® SiO 2 + 4EtOH.
Большинство исследований в этой области относится к синтезу наночастиц сферической формы. Вместе с тем большой научный и практический интерес представляет получение ассиметричных частиц (нити, диски, эллипсоиды) и точный контроль за их формой.
Большой интерес представляет синтез нанокомпозитов, состоящих из частиц одного материала (размер частиц 50 – 100 нм), покрытых тонким слоем другого материала.
Фото- и радиационно-химическое восстановление.
Метод основан на генерации высокоактивных сильных восстановителей типа электронов, радикалов, возбужденных частиц.
Для фотохимического восстановления (фотолиз) типичны энергии менее 60эВ, для радиолиза (радиационно-химического) – 103-104 эВ.
Особенности фотолиза и радиолиза:
Неравновесность в распределении частиц по энергиям,
Перекрывание характерных времен физических и химических процессов,
Определяющее значение для химических превращений активных частиц,
Многоканальность и нестационарность процессов в реагирующих системах.
Преимущества фотолиза и радиолиза перед химическим восстановлением:
Большая чистота образующихся наночастиц,
Возможен синтез наночастиц в твердых средах при низких температурах.
Фотолиз в растворах часто применяют для синтеза частиц благородных металлов.
Среда – растворы солей в воде, спиртах, органических растворителях. В них под действием света образуются активные частицы
Н 2 0 → hν е - (aq) + H + OH
Реагируя со спиртами, атом водорода и радикал гидроксил дают спиртовые радикалы:
H(OH) + (CH 3) 2 CHOH → hν H 2 O(H 2) + (CH 3) 2 COH
Сольватированный электрон взаимодействует с ионом серебра и восстанавливает его до металла
Ag + + (дендример)-СОО - → hν Ag 0
Вначале фотолиза в УФ-спектре поглощения появляются полосы при 277 и 430 нм, относимые к кластерам Ag 4 + и наночастицам серебра с размером 2-3 нм. При увеличении времени облучения максимумы полос поглощения раздвигаются, что указывает на уменьшение среднего размера частиц и протекание процесса агрегации(длинноволновый).
Фотовосстановление нитрата серебра в присутствии поликарбоновых кислот позволило разработать способы управления формой и размером частиц. Получены сферические и стержнеобразные частицы серебра.
Синтез наночастиц при радиолизе заключается в воздействии на систему высоких энергий, примерно 100 эВ. При радиолизе в системе генерируются свободные электроны и радикалы. Так, в водных растворах при облучении из молекулы воды получаются гидратированные частицы – электроны и радикалы водорода и гидроксила:
H 2 O hv →H 0 +HO 0 +e
Электроны и радикалы при взаимодействии с исходным веществом образуют наночастицы.С использованием радиолиза получены нанокомпозиты, состоящие из нескольких металлов. Например, наносистемы никель-серебро с диаметром 2-4 нм; биметаллические частицы Au-Ni размером 2.5 нм, нанесенные на аморфный углерод; триметаллические наночастицы Pd-Au-Ag, состоящие из ядер палладия и двух оболочек золота и серебра. Образующиеся многослойные нанокластерные материалы предполагается использовать для фемтосекундных электронных устройств нового поколения.
Радиолиз для синтеза частиц металлов, проходящий в жидкой фазе, способствует синтезу более узкодисперсных по размеру частиц. При радиолизе вначале образуются атомы и малые кластеры металлов, которые затем превращаются в наночастицы. Начальные стадии их образования представляют собой заряженные кластеры Ag 2 + , Ag 4 + .
Получены наночастицы, включающие по два и более металлов. Так, при восстановлении водородом соли Na 2 PdCl 4 в присутствии цитрата натрия как стабилизатора были получены частицы палладия диаметром 4 нм. Добавление K 2 Au(CN) 4 к золю частиц палладия в метаноле и последующее γ- облучение приводит к восстановлению ионов золота. Всё золото осаждается на частицах палладия, образуя внешний слой. На полученные частицы был осажден и слой серебра. Эти многослойные кластеры интересны для изучения фемтосекундных электронных процессов.
Криохимический синтез
Высокая активность малых кластеров металлов в отсутствии стабилизаторов приводит к агрегации без энергии активации. Стабилизацию активных атомов удалось осуществить при низких(77К) и сверхнизких(4-10К) температурах методом матричной изоляции: пары атомов конденсируют с тысячекратным избытком аргона и ксенона на поверхность, охлажденную до 4-12К.
При исследовании образцов, полученных методом матричной изоляции, в процессе нагревания осуществляются реакции со специально вводимыми химическими соединениями(схема). М- металл, Х – химическое соединение(лиганд). Это схема последовательно-параллельных конкурирующих реакций. Направление 1 отражает процесс агрегации и образование ди-,тримеров и наночастиц; направление 2 – взаимодействие атомов с лигандами и последующее получение комплексов или металлоорганических соединений.
На формирование наночастиц в процессе криоконденсации влияют: скорость достижения атомами охлаждаемой поверхности, соотношение металл-лиганд, скорость конденсации, скорость потери атомами избыточной энергии, давление паров и др.
М → М М 2 → М М 3 → М М 4 → М направление 1
↓ х ↓ х ↓ х ↓х
МХ → М М 2 Х → М М 3 Х → М М 4 Х → М
↓ х ↓х ↓х ↓ х
МХ 2 → М М 2 Х 2 → М
Направление 2 Атомы металлов можно получать, применяя различные методы их нагрева:
Прямым нагревом испаряются атомы щелочных и щелочноземельных элементов (с помощью низковольтного(5В) трансформатора с 300А.
Высокопроводящие металлы(Cu, Ag, Au) испаряются из ячейки Кнудсена при прямом или косвенном нагреве.
Наночастицы обладают повышенной реакционной способностью. Одним из способов получения и стабилизации наночастиц является использование матриц с нанопорами и каналами, размеры и геометрия которых могут изменяться в широких пределах нанотехнологическими средствами. Такие мезопористые матрицы препятствуют агрегации наночастиц, служат как наноконтейнеры. Часто в качестве матриц используются пористые неорганические материалы – цеолиты (алюмосиликаты), силикагель, гидроксилапатиты. Наноструктуры формируются или адсорбцией паров исходного вещества в порах матрицы, или химическим превращением адсорбированных в порах веществ. Например, при использовании полиэтилена в качестве матрицы получены наночастицы металлов в пустотах матрицы. Наноструктуры металлов образовались при термическом разложении металлорганических соединений, адсорбированных в мезопористом полиэтилене.
Размер и форма наночастиц металлов зависят от способа получения, соотношения скоростей нуклеации и роста частиц (температура, природа и концентрация металла или лиганда, характер стабилизатора и восстановителя)
Наночастицы серебра в виде сфер и цилиндров получены при фотохимическом восстановлении солей серебра в присутствии полиакриловой кислоты, дающей с Ag + комплекс, при облучении которого и получаются наночастицы размером 1-2 нм.
В присутствии декарбоксилированной кислоты кроме сфер образуются и наностержни длиной до 80 нм. Эта кислота уменьшает эффективность стабилизации сферических наночастиц и облегчает рост наностержней.
Размер формирующихся в присутствии макромолекул частиц металлов зависит от условий образования полимером защитной оболочки. Если полимер не достаточно эффективный стабилизатор, рост частицы может продолжаться и после ее связывания с макромолекулой. Меняя природу мономера и отвечающего ему полимера и концентрацию полимера в растворе – меняется размер и форма наночастиц.При использовании ультразвука при электролизе нитрата серебра в присутствии N(CH 2 COOH) 3 получены частицы в виде сфер, стержней и дендритов. Форма зависит от длительности импульса ультразвука и концентрации реагентов. Сферы имели диаметр 20 нм, диаметр стержней 10-20 нм. Наночастицы железа в виде сфер и стержней получены при термическом разложении пентакарбонила железа в присутствии стабилизаторов. Сферы имели диаметр 2 нм и были аморфными, при диспергировании в растворе превращались в стержни диаметром 2 нм и длиной в 11 нм и имели кубическую ОЦК структуру.
Наносеребро. ВМС обеспечивают высокую стабильность получающейся дисперсной системы и непосредственно участвуют в процессе ее формирования, контролируя размер и форму растущих наночастиц.
Поликарбоновые кислоты акрилового ряда имеют ионизированные карбоксилатные группы и взаимодействуют с ионами серебра, связывая их в прочный комплекс(1),
Восстанавливают их под действием света прямо в комплексе(2),
Стабилизируют последовательно образующиеся в ходе синтеза малые заряженные кластеры и наночастицы металла (3):
(1) R-COO - + Ag + → R-COO -● Ag +
(2) R-COO -● Ag + → hν R-COO -● + Ag +
(3) R-COO -● Ag + + Ag 0 → R-COO -● Ag + 2 → R-COO -● Ag 2+ 4 → hν R-COOAg + n
Весь процесс формирования наночастиц протекает в контакте с полимерной матрицей.
Связывание Ag+ полиакрилат анионами(ПА) с М=450000 и 1250000 при степени ионизации α = 1,0 происходит кооперативно(с увеличением содержания серебра в растворе растет концентрация цепей в предельной степени заполненных ионами Ag+ .
Облучение ртутной лампой водного раствора Ag+●ПА вызывает фотовосстановление катионов Ag+. При этом вначале образуются кластеры Ag 2 +8 (в отсутствии УФ-света они стабильны несколько недель). Дальнейшее облучение приводит к образованию Ag2+14 и наночастиц серебра. Этот раствор тоже стабилен несколько недель. Эти частицы имеют сферическую форму и размер 1-2 нм при М=450000 и размер 4-5 нм при М=1250000.
Т.о. восстановление катионов, рост частиц протекает внутри макромолекулярного клубка, выступающего в качестве нанореактора фотохимического синтеза сферических наночастиц.
При связывании Ag+ полиакрилат-анионом с М=2000 кооперативности нет: при увеличении содержания Ag равномерное заполнение макромолекул сопровождается ростом концентрации ионов Ag+ в растворе. Фотолиз также приводит к образованию и золей и наночастиц.
Форма наночастиц серебра определяется содержанием в полимере ионизированных карбоксилатных групп. При γ< 0,7 происходит формирование стержневидных частиц.
При γ=0,5 сразу образуются агрегаты частиц в виде наностержней толщиной 20-30 нм и длиной до нескольких микрометров.
Восстановление AgNO 3 (6.10-4М) борогидридом натрия(1,2.10-3М) в присутствии фотодекарбоксилированного ПА γ=0,5 (1,2.10-3М) приводит к стабильному золю со сферами 6 нм. Для превращения их в удлиненные достаточно облучение с 363 <λ <555нм, т.е. в полосе их поглощения. Усиление диполь-дипольного взаимодействия между частицами и вызывает их фотоиндуцированную агрегацию.
Размером, формой и степенью полидисперсности наночастиц серебра, образующихся при фотовосстановлении ионов можно управлять, меняя М, степень ионизации и декарбоксилирования поликарбоновых кислот.
Нанореакторы. Высокая активность кластеров и частиц металлов связана с некомпенсированностью поверхностных связей. Многофакторный процесс M+L конкурирующих последовательно – параллельных реакций, идущих с энергией активации Е=0 происходит в образованиях, которые можно рассматривать как нанореактор. Это неравновесные системы. Поэтому чем активнее частица, тем ниже температура её стабилизации. Атомы большинства металлов стабилизируются при температуре 4-10К в инертных матрицах при разбавлении, например, аргоном в 1000 раз. Это метод матричной изоляции. Суть его – в накоплении веществ в условиях, которые мешают реакциям. Так, в твердом инертном веществе при низких температурах матрица препятствует диффузии и активные частицы практически заморожены(стабильны) в среде, которая не способная с ними реагировать.
Температуры плавления(в К) для инертных газов – матриц
Атомы Ne Ar Kr Xe
Р=1 атм 25 83 116 161
Р=10-3 мм рт. ст. 11 39 54 74
Элементы УШ группы: Fe, Co, Ni, Ru, Rh, Pd, Os, Ir, Pt. Формирование кластера палладия с лигандной оболочкой L-1,10-фенантролин и группы OАc происходит в 2 стадии:
Pd(OAc) 2 + L + H 2 → (1/n) n + AcOH,
N + O 2 +AcOH →Pd 561 L 60 (OAc) 180 + Pd(OAc) 2 + L + H 2 O
Полученные частицы палладия относятся к «магическим» 13, 55, 147, 309, 561,…..
Эти числа соответствуют полностью заполненным оболочкам кубооктаэдрических кластеров. Механизм синтеза частиц с фиксированным числом атомов до конца не выяснен.
К настоящему времени разработаны многочисленные методы получения наноматериалов как в виде нанопорошков, так и в виде включений в пористые или монолитные матрицы. При этом в качестве нанофазы могут выступать ферро- и ферримагнетики, металлы, полупроводники, диэлектрики и др.
Согласно Фендлеру, важнейшими условиями получения наноматериалов являются:
1. Неравновесность систем. Практически все наносистемы термодинамически неустойчивы, и их получают в условиях, далеких от равновесных, что позволяет добиться спонтанного зародышеобразования и избежать роста и агрегации сформировавшихся наночастиц.
2. Однородность наночастиц. Высокая химическая однородность наноматериала обеспечивается, если в процессе синтеза не происходит разделения компонентов как в пределах одной наночастицы, так и между частицами.
3. Монодисперсность наночастиц. Свойства наночастиц чрезвычайно сильно зависят от их размера, поэтому для получения материалов с хорошими функциональными характеристиками необходимо использовать частицы с достаточно узким распределением по размерам.
В дальнейшем было показано, что эти условия не всегда обязательны для выполнения. Например, растворы поверхностно-активных веществ (мицеллярные структуры, пленки Ленгмюра - Блоджетт, жидкокристаллические фазы) являются термодинамически стабильными, тем не менее они служат основой для формирования разнообразных наноструктур.
Все методы получения наноматериалов можно условно разделить на несколько больших групп. К первой группе относят так называемые высокоэнергетические методы, основанные на быстрой конденсации паров в условиях, исключающих агрегацию и рост образующихся частиц. Основные различия между отдельными методами этой группы состоят в способе испарения и стабилизации образующихся наночастиц. Испарение можно проводить с использованием плазменного возбуждения (plasma-ark), лазерного излучения (laser ablation), вольтовой дуги (carbon ark) или термического воздействия. Конденсацию осуществляют либо в присутствии ПАВ, адсорбция которого на поверхности частиц замедляет рост (vapor trapping); либо на холодной подложке, когда рост частиц ограничен скоростью диффузии; либо в присутствии инертного компонента, что позволяет направленно получать нано композитные материалы с различной микроструктурой . Если компоненты взаимно нерастворимы, то размер наночастиц можно варьировать с помощью термической обработки.
Ко второй группе относятся механохимические методы (ball-milling), позволяющие получать нанокомпозиты при совместном помоле взаимо нерастворимых компонентов в планетарных мельницах или при распаде твердых растворов с образованием новых фаз под действием механических напряжений.
Третья группа методов основана на использовании пространственно-ограниченных систем -- нанореакторов (мицелл, капель, пленок и т.д.) . К их числу относится синтез в обращенных мицеллах, в пленках Лэнгмюра - Блоджетт и в адсорбционных слоях. Ясно, что размер образующихся при этом частиц не может превосходить размер соответствующего нанореактора, поэтому указанные методы позволяют получать монодисперсные системы. К этой группе можно отнести также биомиметический и биологический методы синтеза наночастиц, в которых в качестве нанореакторов выступают биомолекулы (белки, ДНК и др.).
В четвертую группу входят методы, основанные на формировании в растворах ультрамикродисперсных коллоидных частиц при поликонденсации в присутствии поверхностно-активных веществ, предотвращающих агрегацию.
К пятой группе относятся химические методы получения высокопористых и мелкодисперсных структур (металлы Рике, никель Ренея), основанные на удалении одного из компонентов микрогетерогенной системы в результате химической реакции или анодного растворения. К числу этих методов можно отнести также традиционный способ получения нанокомпозитов путем закалки стеклянной или солевой матрицы с растворенным веществом, в результате чего происходит кристаллизация этого вещества в матрице (стекла, модифицированные полупроводниковыми или металлическими наночастицами). При этом введение вещества в матрицу может осуществляться двумя способами: добавлением его в расплав (раствор) с последующей закалкой и непосредственным введением в твердую матрицу с помощью ионной имплантации.
Одним из наиболее распространенных химических методов получения нано материалов является золь-гель-синтез. С его помощью получают гомогенные оксидные системы, химическая модификация которых (восстановление, сульфидирование и т.д.) приводит к формированию наночастиц соответствующего материала в матрице . Следует отметить, что использование золь-гель-метода позволяет получать наноматериалы с улучшенными функциональными свойствами благодаря контролю состава и структуры промежуточных продуктов. Он привлекателен также своей реализуемостью в лабораторных условиях. Однако этот метод имеет и серьезные недостатки. Во-первых, он не обеспечивает монодисперсности частиц. Во-вторых, он не позволяет получать двумерные и одномерные наноструктуры, а также пространственно-упорядоченные структуры, состоящие из наночастиц, расположенных на одинаковом расстоянии друг от друга, или из параллельных нанопластин с прослойками инертной матрицы, которые можно синтезировать в нано реакторах. И наконец, в ряде случаев получение требуемого нанокомпозита невозможно из-за химического взаимодействия частиц с гелеобразующим агентом.
Необходимо отметить, что использование свободных наночастиц и наноструктур в качестве материалов сильно затруднено ввиду метастабильности вещества в нанокристаллическом состоянии. Как уже отмечалось выше, это связано с увеличением удельной поверхности частиц по мере уменьшения их линейных размеров до нанометровых, приводящим к возрастанию химической активности соединения и усилению процессов агрегации. Чтобы предотвратить агрегацию наночастиц и защитить их от внешних воздействий (например, от окисления кислородом воздуха), наночастицы заключают в химически инертную матрицу.
Анализ литературных данных показывает, что к настоящему времени разработаны десятки способов матричной изоляции наноструктур, которые можно условно разделить на две группы: получение свободных наночастиц с последующим включением в инертную матрицу и непосредственное формирование наноструктур в объеме матрицы в процессе ее химической модификации.
Первая группа методов отличается простотой в реализации, однако накладывает серьезные ограничения на возможности выбора матрицы. В качестве последней, как правило, используют органические полимерные соединения, не отличающиеся высокой термической устойчивостью и не всегда обладающие необходимыми физическими свойствами (например, высокой оптической прозрачностью). Кроме того, при инкорпорировании не исключены процессы агрегации наночастиц.
Вторая группа методов позволяет не только избежать этих недостатков, но и непосредственно контролировать параметры наночастиц в матрице на стадии их формирования и даже менять эти параметры в процессе эксплуатации материала. Используемые для этих целей матрицы должны содержать структурные пустоты, которые могут быть заполнены соединениями, последующая модификация которых приводит к формированию наночастиц в этих пустотах. Другими словами, эти пустоты должны ограничивать зону протекания реакции с участием внедренных в них соединений, т.е. выступать в роли своеобразных нанореакторов. Очевидно, что, выбирая соединения с различной формой структурных пустот, можно осуществлять синтез наноструктур различной морфологии и анизотропии.
В качестве примера можно привести синтез наноматериалов с использованием пористых оксидных матриц (обычно SiO 2 или Аl 2 Оз) . Однако ввиду неупорядоченности пористой структуры таких матриц и достаточно широкого распределения пор по размерам с их помощью практически невозможно получить удовлетворительно сформированные наносистемы. Обычно нанокомпозиты, полученные на основе пористых оксидных матриц, используют в катализе, где требования к монодисперсности частиц и их морфологии не столь высоки. Кроме того, жесткая пористая структура таких матриц не дает возможности менять размеры и морфологию частиц во время синтеза; последние, как правило, жестко зависят от размера и морфологии пор, т.е. при использовании одного типа матрицы можно получить лишь очень ограниченный круг наноструктур.
Иногда для быстрого направленного формирования наночастиц в матрице прибегают к дополнительным физическим воздействиям, таким как ультразвук, микроволновое и лазерное облучение.