Тип химической связи между атомами углерода. Ковалентные связи с участием атома углерода
Продолжение. Начало см. в № 15, 16/2004
Урок 5. Гибридизация
атомных орбиталей углерода
Ковалентная химическая связь образуется при помощи общих связывающих электронных пар по типу:

Образовывать химическую связь, т.е. создавать
общую электронную пару с «чужим» электроном от
другого атома, могут только неспаренные
электроны. Неспаренные электроны при записи
электронных формул находятся по одному в
клетке-орбитали.
Атомная орбиталь
– это функция, которая
описывает плотность электронного облака в
каждой точке пространства вокруг ядра атома.
Электронное облако – это область пространства, в
которой с высокой вероятностью может быть
обнаружен электрон.
Для согласования электронного строения атома
углерода и валентности этого элемента
пользуются представлениями о возбуждении атома
углерода. В нормальном (невозбужденном)
состоянии атом углерода имеет два неспаренных 2р
2 -электрона.
В возбужденном состоянии (при поглощении
энергии) один из 2s
2 -электронов может
переходить на свободную р
-орбиталь. Тогда в
атоме углерода появляется четыре неспаренных
электрона:
Напомним, что в электронной формуле атома (например, для углерода 6 С – 1s 2 2s 2 2p 2) большие цифры перед буквами – 1, 2 – обозначают номер энергетического уровня. Буквы s и р указывают форму электронного облака (орбитали), а цифры справа над буквами говорят о числе электронов на данной орбитали. Все s -орбитали сферические:

На втором энергетическом уровне кроме 2s -орбитали имеются три 2р -орбитали. Эти 2р -орбитали имеют эллипсоидную форму, похожую на гантели, и ориентированы в пространстве под углом 90° друг к другу. 2р -Орбитали обозначают 2р х , 2р y и 2р z в соответствии с осями, вдоль которых эти орбитали расположены.
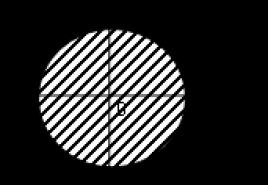
При образовании химических связей электронные орбитали приобретают одинаковую форму. Так, в предельных углеводородах смешиваются одна s -орбиталь и три р -орбитали атома углерода с образованием четырех одинаковых (гибридных) sр 3 -орбиталей:
![]()
Это – sр
3 -гибридизация.
Гибридизация
– выравнивание
(смешивание) атомных орбиталей (s
и р
) с
образованием новых атомных орбиталей,
называемых гибридными орбиталями
.
Гибридные орбитали имеют
асимметричную форму, вытянутую в сторону
присоединяемого атома. Электронные облака
взаимно отталкиваются и располагаются в
пространстве максимально далеко друг от друга.
При этом оси четырех sр
3-гибридных орбиталей
оказываются направленными к вершинам тетраэдра
(правильной треугольной пирамиды).
Соответственно углы между этими орбиталями –
тетраэдрические, равные 109°28".
Вершины электронных орбиталей могут
перекрываться с орбиталями других атомов. Если
электронные облака перекрываются по линии,
соединяющий центры атомов, то такую ковалентную
связь называют сигма()-связью
. Например, в молекуле этана
С 2 Н 6 химическая связь образуется
между двумя атомами углерода перекрыванием двух
гибридных орбиталей. Это -связь. Кроме того, каждый из
атомов углерода своими тремя sр
3 -орбиталями
перекрывается с s
-орбиталями трех атомов
водорода, образуя три -связи.
Всего для атома углерода возможны три
валентных состояния с различным типом
гибридизации. Кроме sр
3 -гибридизации
существует sр
2 - и sр
-гибридизация.
sр
2 -Гибридизация
– смешивание одной
s
- и двух р
-орбиталей. В результате
образуются три гибридные sр
2 -орбитали.
Эти sр
2 -орбитали расположены в одной
плоскости (с осями х
, у
) и направлены к
вершинам треугольника с углом между орбиталями
120°. Негибридизованная
р
-орбиталь перпендикулярна к плоскости трех
гибридных sр
2 -орбиталей (ориентирована
вдоль оси z
). Верхняя половина р
-орбитали
находится над плоскостью, нижняя половина – под
плоскостью.
Тип sр
2 -гибридизации углерода бывает у
соединений с двойной связью: С=С, С=О, С=N. Причем
только одна из связей между двумя атомами
(например, С=С) может быть -связью. (Другие связывающие
орбитали атома направлены в противоположные
стороны.) Вторая связь образуется в результате
перекрывания негибридных р
-орбиталей по обе
стороны от линии, соединяющей ядра атомов.
Ковалентная связь, образующаяся путем бокового перекрывания р -орбиталей соседних углеродных атомов, называется пи()-связью .
Образование
|
Из-за меньшего перекрывании орбиталей -связь менее
прочная, чем -связь.
sр
-Гибридизация
– это смешивание
(выравнивание по форме и энергии) одной s-
и
одной
р
-орбиталей с образованием двух гибридных sр
-орбиталей.
sр
-Орбитали расположены на одной линии (под
углом 180°) и направлены в противоположные стороны
от ядра атома углерода. Две
р
-орбитали остаются негибридизованными. Они
размещены взаимно перпендикулярно
направлениям -связей. На рисунке sр
-орбитали
показаны вдоль оси y
, а негибридизованные две
р
-орбитали– вдоль осей х
и z
.
Тройная углерод-углеродная связь СС состоит из -связи, возникающей
при перекрывании
sp
-гибридных орбиталей, и двух -связей.
Взаимосвязь таких параметров атома углерода, как
число присоединенных групп, тип гибридизации и
типы образуемых химических связей, показана в
таблице 4.
Таблица 4
Ковалентные связи углерода
| Число групп, связанных с углеродом |
Тип гибридизации |
Типы участвующих химических связей |
Примеры формул соединений |
|---|---|---|---|
| 4 | sp 3 | Четыре - связи | |
| 3 | sp 2 | Три - связи и одна - связь |
|
| 2 | sp | Две - связи и две -связи |
H–CC–H |
Упражнения .
1. Какие электроны атомов (например, углерода или азота) называют неспаренными?
2. Что означает понятие «общие электронные пары» в соединениях с ковалентной связью (например, СН 4 или Н 2 S)?
3. Какие электронные состояния атомов (например, С или N) называют основными, а какие возбужденными?
4. Что означают цифры и буквы в электронной формуле атома (например, С или N)?
5. Что такое атомная орбиталь? Сколько орбиталей на втором энергетическом уровне атома С и чем они различаются?
6. В чем отличие гибридных орбиталей от исходных орбиталей, из которых они образовались?
7. Какие типы гибридизации известны для атома углерода и в чем они заключаются?
8. Нарисуйте картинку пространственного расположения орбиталей для одного из электронных состояний атома углерода.
9. Какие химические связи называют и какие ? Укажите - и -связи в соединениях:
10. Для атомов углерода приведенных ниже соединений укажите: а) тип гибридизации; б) типы его химических связей; в) валентные углы.

Ответы на упражнения к теме 1
Урок 5
1. Электроны, которые находятся по одному на орбитали, называют неспаренными электронами . Например, в электронографической формуле возбужденного атома углерода – четыре неспаренных электрона, а у атома азота – три:
2. Два электрона, участвующие в образовании одной химической связи, называют общей электронной парой . Обычно до образования химической связи один из электронов этой пары принадлежал одному атому, а другой электрон – другому атому:

3. Электронное состояние атома, в котором соблюдается порядок заполнения электронных орбиталей: 1s 2 , 2s 2 , 2p 2 , 3s 2 , 3p 2 , 4s 2 , 3d 2 , 4p 2 и т.д., называют основным состоянием . В возбужденном состоянии один из валентных электронов атома занимает свободную орбиталь с более высокой энергией, такой переход сопровождается разъединением спаренных электронов. Схематически это записывают так:
Тогда как в основном состоянии было только два валентных неспаренных электрона, то в возбужденном состоянии таких электронов становится четыре.
5.
Атомная орбиталь – это функция,
которая описывает плотность электронного облака
в каждой точке пространства вокруг ядра данного
атома. На втором энергетическом уровне атома
углерода четыре орбитали – 2s
, 2р x
, 2р y
,
2р z
. Эти орбитали различаются:
а) формой электронного облака (s
– шар, р
–
гантель);
б) р
-орбитали имеют разную ориентацию в
пространстве – вдоль взаимно перпендикулярных
осей x
, y
и z
, их обозначают р x
, р y
,
р z
.
6.
Гибридные орбитали отличаются от
исходных (негибридных) орбиталей формой и
энергией. Например, s
-орбиталь – форма сферы, р
– симметричная восьмерка, sp
-гибридная
орбиталь – асимметричная восьмерка.
Различия по энергии: E
(s
) < E
(sр
) < E
(р
).
Таким образом, sp
-орбиталь – усредненная по
форме и энергии орбиталь, полученная смешиванием
исходных s
-
и p
-орбиталей.
7. Для атома углерода известны три типа гибридизации: sp 3 , sp 2 и sp (см. текст урока 5 ).
9.
-связь
– ковалентная связь, образующаяся путем
лобового перекрывания орбиталей по линии,
соединяющей центры атомов.
-связь –
ковалентная связь, образующаяся путем бокового
перекрывания р
-орбиталей по обе стороны от
линии, соединяющей центры атомов.
-Связи
показывают второй и третьей черточкой между
соединенными атомами.
ГЛАВА 2. ХИМИЧЕСКАЯ СВЯЗЬ И ВЗАИМНОЕ ВЛИЯНИЕ АТОМОВ В ОРГАНИЧЕСКИХ СОЕДИНЕНИЯХ
Химические свойства органических соединений обусловлены типом химических связей, природой связываемых атомов и их вза- имным влиянием в молекуле. Эти факторы, в свою очередь, определяются электронным строением атомов и взаимодействием их атомных орбиталей.
2.1. Электронное строение атома углерода
Часть атомного пространства, в котором вероятность нахождения электрона максимальна, называют атомной орбиталью (АО).
В химии широко используется представление о гибридных орбиталях атома углерода и других элементов. Понятие о гибридизации как способе описания перестройки орбиталей необходимо тогда, когда число неспаренных электронов в основном состоянии атома меньше числа образуемых связей. Примером служит атом углерода, который во всех соединениях проявляет себя как четырехвалентный элемент, но в соответствии с правилами заполнения орбиталей на его внешнем электронном уровне в основном состоянии 1s 2 2s 2 2p 2 находятся только два неспаренных электрона (рис. 2.1, а и Приложение 2-1). В этих случаях постулируется, что различные атомные орбитали, близкие по энергии, могут смешиваться между собой, образуя одинаковые по форме и энергии гибридные орбитали.
Гибридные орбитали из-за большего перекрывания образуют более прочные связи по сравнению с негибридизованными орбиталями.
В зависимости от числа вступивших в гибридизацию орбиталей атом углерода может находиться в одном из трех состояний
Рис. 2.1. Распределение электронов по орбиталям у атома углерода в основном (а), возбужденном (б) и гибридизованных состояниях (в - sp 3 , г - sp 2 , д - sp)
гибридизации (см. рис. 2.1, в-д). Тип гибридизации определяет направленность гибридных АО в пространстве и, следовательно, геометрию молекул, т. е. их пространственное строение.
Пространственное строение молекул - это взаимное расположение атомов и атомных групп в пространстве.
sp 3 -Гибридизация. При смешении четырех внешних АО возбужденного атома углерода (см. рис. 2.1, б) - одной 2s- и трех 2p-орбиталей - возникают четыре равноценные sp 3 -гибридные орбитали. Они имеют форму объемной «восьмерки», одна из лопастей которой значительно больше другой.
Каждая гибридная орбиталь заполняется одним электроном. Атом углерода в состоянии sp 3 -гибридизации имеет электронную конфигурацию 1s 2 2(sp 3) 4 (см. рис. 2.1, в). Такое состояние гибридизации характерно для атомов углерода в насыщенных углеводородах (алканах) и соответственно в алкильных радикалах.
Вследствие взаимного отталкивания sp 3 -гибридные АО направлены в пространстве к вершинам тетраэдра, и углы между ними равны 109,5? (наиболее выгодное расположение; рис. 2.2, а).
Пространственное строение изображается с помощью стереохимических формул. В этих формулах sp 3 -гибридизованный атом углерода и две его связи располагают в плоскости чертежа и графически обозначают обычной чертой. Жирной чертой или жирным клином обозначают связь, выходящую вперед из плоскости чертежа и направленную к наблюдателю; пунктирной линией или заштрихованным клином (..........) - связь, уходящую от наблюдателя за плоскость черте-

Рис. 2.2. Виды гибридизации атома углерода. Точка в центре - ядро атома (малые доли гибридных орбиталей для упрощения рисунка опущены; цветом показаны негибридизованные р-АО)
жа (рис. 2.3, а). Атом углерода в состоянии sp 3 -гибридизации имеет тетраэдрическую конфигурацию.
sp 2 -Гибридизация. При смешении одной 2s- и двух 2р-АО возбужденного атома углерода образуются три равноценные sp 2 -гибридные орбитали и остается негибридизованной 2р-АО. Атом углерода в состоянии sp 2 -гибридизации имеет электронную конфигурацию 1s 2 2(sp 2) 3 2p 1 (см. рис. 2.1, г). Такое состояние гибридизации атома углерода характерно для ненасыщенных углеводородов (алкенов), а также для некоторых функциональных групп, например карбонильной и карбоксильной.
sp 2 -Гибридные орбитали располагаются в одной плоскости под углом 120?, а негибридизованная АО находится в перпендикулярной плоскости (см. рис. 2.2, б). Атом углерода в состоянииsp 2 -гибридизации имеет тригональную конфигурацию. Атомы углерода, связанные двойной связью, находятся в плоскости чертежа, а их одинарные связи, направленные к наблюдателю и от него, обозначают, как описано выше (см. рис. 2.3, б).
sp-Гибридизация. При смешении одной 2s- и одной 2р-орбиталей возбужденного атома углерода образуются две равноценные sp-гиб- ридные АО, а две p-АО остаются негибридизованными. Атом углерода в состоянии sp-гибридизации имеет электронную конфигурацию

Рис. 2.3. Стереохимические формулы метана (а), этана (б) и ацетилена (в)
1s 2 2(sp 2) 2 2p 2 (см. рис. 2.1, д). Такое состояние гибридизации атома углерода встречается в соединениях, имеющих тройную связь, например, в алкинах, нитрилах.
sp-Гибридные орбитали располагаются под углом 180?, а две негибридизованные АО - во взаимно перпендикулярных плоскостях (см. рис. 2.2, в). Атом углерода в состоянии sp-гибридизации имеет линейную конфигурацию, например в молекуле ацетилена все четыре атома находятся на одной прямой (см. рис. 2.3, в).
В гибридизованном состоянии могут находиться и атомы других элементов-органогенов.
2.2. Химические связи атома углерода
Химические связи в органических соединениях представлены в основном ковалентными связями.
Ковалентной называют химическую связь, образованную в результате обобществления электронов связываемых атомов.
Эти обобществленные электроны занимают молекулярные орбитали (МО). Как правило, МО является многоцентровой орбиталью и заполняющие ее электроны делокализованы (рассредоточены). Таким образом, МО, как и АО, может быть вакантной, заполненной одним электроном или двумя электронами с противоположными спинами*.
2.2.1. σ- и π -Связи
Существуют два типа ковалентной связи: σ (сигма)- и π (пи)-связи.
σ-Связью называют ковалентную связь, образованную при перекрывании АО по прямой (оси), соединяющей ядра двух связывае- мых атомов с максимумом перекрывания на этой прямой.
σ-Связь возникает при перекрывании любых АО, в том числе и гибридных. На рисунке 2.4 показано образование σ-связи между атомами углерода в результате осевого перекрывания их гибридных sp 3 -АО и σ-связей C-H путем перекрывания гибридной sp 3 -АО углерода и s-АО водорода.
* Подробнее см.: Попков В.А., Пузаков С.А. Общая химия. - М.: ГЭОТАР-Медиа, 2007. - Глава 1.

Рис. 2.4. Образование σ-связей в этане путем осевого перекрывания АО (малые доли гибридных орбиталей опущены, цветом показаны sp 3 -АО углерода, черным - s-АО водорода)
Кроме осевого возможен еще один вид перекрывания - боковое перекрывание p-АО, приводящее к образованию π-связи (рис. 2.5).
р-атомные орбитали

Рис. 2.5. Образование π-связи в этилене путем бокового перекрывания р-АО
π-Связью называют связь, образованную при боковом перекрывании негибридизованных p-АО с максимумом перекрывания по обе стороны от прямой, соединяющей ядра атомов.
Встречающиеся в органических соединениях кратные связи являются сочетанием σ- и π-связей: двойная - одной σ- и одной π-, тройная - одной σ- и двух π-связей.
Свойства ковалентной связи выражаются через такие характеристики, как энергия, длина, полярность и поляризуемость.
Энергия связи - это энергия, выделяющаяся при образовании связи или необходимая для разъединения двух связанных атомов. Она служит мерой прочности связи: чем больше энергия, тем прочнее связь (табл. 2.1).
Длина связи - это расстояние между центрами связанных атомов. Двойная связь короче одинарной, а тройная короче двойной (см. табл. 2.1). Связи между атомами углерода, находящихся в разном состоянии гибридизации, имеют общую закономерность -
Таблица 2.1. Основные характеристики ковалентных связей

с увеличением доли s-орбитали в гибридной орбитали уменьшается длина связи. Например, в ряду соединений пропан CH 3 CH 2 CH 3, пропен CH 3 CH=CH 2, пропин CH 3 C=CH длина связи CH 3 -C соответственно равна 0,154; 0,150 и 0,146 нм.
Полярность связи обусловлена неравномерным распределением (поляризацией) электронной плотности. Полярность молекулы количественно оценивают величиной ее дипольного момента. Из дипольных моментов молекулы можно вычислить дипольные моменты отдельных связей (см. табл. 2.1). Чем больше дипольный момент, тем полярнее связь. Причиной полярности связи служит различие в электроотрицательности связанных атомов.
Электроотрицательность характеризует способность атома в молекуле удерживать валентные электроны. С увеличением электроотрицательности атома возрастает степень смещения в его сторону электронов связи.
Основываясь на значениях энергии связей, американский химик Л. Полинг (1901-1994) предложил количественную характеристику относительной электроотрицательности атомов (шкала Полинга). В этой шкале (ряду) типичные элементы-органогены располагаются по относительной электроотрицательности (для сравнения приведены два металла) следующим образом:
Электроотрицательность не является абсолютной константой элемента. Она зависит от эффективного заряда ядра, вида гибридизации АО и влияния заместителей. Например, электроотрицательность атома углерода, находящегося в состоянии sp 2 - или sp-гибридизации, выше, чем в состоянии sp 3 -гибридизации, что связано с увеличением доли s-орбитали в гибридной орбитали. При переходе атомов из sp 3 - в sp 2 - и далее в sp -гибридизованное состояние постепенно уменьшается протяженность гибридной орбитали (особенно в направлении, обеспечивающем наибольшее перекрывание при образовании σ-связи), а это означает, что в такой же последовательности максимум электронной плотности располагается все ближе к ядру соответствующего атома.
В случае неполярной или практически неполярной ковалентной связи разность в электроотрицательности связанных атомов равна нулю или близка к нулю. С увеличением разности в электроотрицательности возрастает полярность связи. При разности до 0,4 говорят о слабо полярной, более 0,5 - о сильно полярной ковалентной связи и более 2,0 - об ионной связи. Полярные ковалентные связи предрасположены к гетеролитическому разрыву
(см. 3.1.1).
Поляризуемость связи выражается в смещении электронов связи под влиянием внешнего электрического поля, в том числе и другой реагирующей частицы. Поляризуемость определяется подвижностью электронов. Электроны тем подвижнее, чем дальше они находятся от ядер атомов. По поляризуемости π-связь значительно превосходит σ-связь, так как максимум электронной плотности π-связи располагается дальше от связываемых ядер. Поляризуемость в значительной мере определяет реакционную способность молекул по отношению к полярным реагентам.
2.2.2. Донорно-акцепторные связи
Перекрывание двух одноэлектронных АО - не единственный путь образования ковалентной связи. Ковалентная связь может образовываться при взаимодействии двухэлектронной орбитали одного атома (донора) с вакантной орбиталью другого атома (акцептора). Донорами служат соединения, содержащие либо орбитали с неподеленной парой электронов, либо π-МО. Носителями неподеленных пар электронов (n-электронов, от англ. non-bonding) являются атомы азота, кислорода, галогенов.
Неподеленные пары электронов играют важную роль в проявлении химических свойств соединений. В частности, они ответственны за способность соединений вступать в донорно-акцепторное взаимо- действие.
Ковалентая связь, образующаяся за счет пары электронов одного из партнеров по связи, называется донорно-акцепторной.

Образовавшаяся донорно-акцепторная связь отличается только способом образования; по свойствам она одинакова с остальными ковалентными связями. Атом-донор при этом приобретает положительный заряд.
Донорно-акцепторные связи характерны для комплексных соединений.
2.2.3. Водородные связи
Атом водорода, связанный с сильно электроотрицательным элементом (азотом, кислородом, фтором и др.), способен взаимодействовать с неподеленной парой электронов другого достаточно электроотрицательного атома этой же или другой молекулы. В результате возникает водородная связь, являющаяся разновидностью донорно-
акцепторной связи. Графически водородную связь обычно обозначают тремя точками.
Энергия водородной связи невелика (10-40 кДж/моль) и в основном определяется электростатическим взаимодействием.
Межмолекулярные водородные связи обусловливают ассоциацию органических соединений, например спиртов.

Водородные связи влияют на физические (температуры кипения и плавления, вязкость, спектральные характеристики) и химические (кислотно-основные) свойства соединений. Так, температура кипения этанола C 2 H 5 OH (78,3 ?С) значительно выше, чем имеющего одинаковую с ним молекулярную массу диметилового эфира CH 3 OCH 3 (-24 ?C), не ассоциированного за счет водородных связей.
Водородные связи могут быть и внутримолекулярными. Такая связь в анионе салициловой кислоты приводит к повышению ее кислотности.
Водородные связи играют важную роль в формировании пространственной структуры высокомолекулярных соединений - бел- ков, полисахаридов, нуклеиновых кислот.
2.3. Сопряженные системы
Ковалентная связь может быть локализованной и делокализованной. Локализованной называют связь, электроны которой фактически поделены между двумя ядрами связываемых атомов. Если электроны связи поделены более чем между двумя ядрами, то говорят о делокализованной связи.
Делокализованная связь - это ковалентная связь, молекулярная орбиталь которой охватывает более двух атомов.
Делокализованные связи в большинстве случаев являются π-связями. Они характерны для сопряженных систем. В этих систе- мах осуществляется особый вид взаимного влияния атомов - сопряжение.
Сопряжение (мезомерия, от греч. mesos - средний) - это выравнивание связей и зарядов в реальной молекуле (частице) по сравнению с идеальной, но не существующей структурой.
Участвующие в сопряжении делокализованные р-орбитали могут принадлежать либо двум π-связям и более, либо π-связи и одному атому с р-орбиталью. В соответствии с этим различают π,π-сопряжение и ρ,π-сопряжение. Система сопряжения может быть открытой или замкнутой и содержать не только атомы углерода, но и гетероатомы.
2.3.1. Системы с открытой цепью сопряжения
π,π-Сопряжение. Простейшим представителем π,π-сопряженных систем с углеродной цепью служит бутадиен-1,3 (рис. 2.6, а). Атомы углерода и водорода и, следовательно, все σ-связи в его молекуле лежат в одной плоскости, образуя плоский σ-скелет. Атомы углерода находятся в состоянии sр 2 -гибридизации. Негибридизованные р-АО каждого атома углерода расположены перпендикулярно плоскости σ-скелета и параллельно друг другу, что является необходимым условием для их перекрывания. Перекрывание происходит не только между р-АО атомов С-1 и С-2, С-3 и С-4, но и между р-АО атомов С-2 и С-3, в результате чего образуется охватывающая четыре атома углерода единая π-система, т. е. возникает делокализованная ковалентная связь (см. рис. 2.6, б).

Рис. 2.6. Атомно-орбитальная модель молекулы бутадиена-1,3
Это отражается в изменении длин связей в молекуле. Длина связи С-1-С-2, а также С-3-С-4 в бутадиене-1,3 несколько увеличена, а расстояние между С-2 и С-3 укорочено по сравнению с обычными двойными и одинарными связями. Другими словами, процесс делокализации электронов приводит к выравниванию длин связей.
Углеводороды с большим числом сопряженных двойных связей распространены в растительном мире. К ним относятся, например, каротины, обусловливающие окраску моркови, томатов и т. п.
Открытая система сопряжения может включать и гетероатомы. Примером открытых π,π-сопряженных систем с гетероатомом в цепи могут служить α,β-ненасыщенные карбонильные соединения. Например, альдегидная группа в акролеине CH 2 =CH-CH=O явля- ется участником цепи сопряжения трех sр 2 -гибридизованных атомов углерода и атома кислорода. Каждый из этих атомов вносит в единую π-систему по одному р-электрону.
pn-Сопряжение. Этот вид сопряжения чаще всего проявляется в соединениях, содержащих структурный фрагмент -CH=CH-X, где X - гетероатом, имеющий неподеленную пару электронов (прежде всего O или N). К ним относятся, например, виниловые эфиры, в молекулах которых осуществляется сопряжение двойной связи с р -орбиталью атома кислорода. Делокализованная трехцен- тровая связь образуется путем перекрывания двух р-АО sр 2 -гиб- ридизованных атомов углерода и одной р -АО гетероатома с парой и-электронов.

Образование аналогичной делокализованной трехцентровой связи имеется в карбоксильной группе. Здесь в сопряжении участвуют π-электроны связи С=О и n-электроны атома кислорода группы ОН. К сопряженным системам с полностью выровненными связями и зарядами относятся отрицательно заряженные частицы, например ацетат-ион.

Направление смещения электронной плотности обозначается изогнутой стрелкой.
Существуют и другие графические способы отображения результатов сопряжения. Так, структура ацетат-иона (I) предполагает, что заряд равномерно распределен по обоим атомам кислорода (как показано на рис. 2.7, что соответствует действительности).
Структуры (II) и (III) применяются в теории резонанса. Согласно этой теории реальная молекула или частица описывается набором определенных так называемых резонансных структур, которые отличаются друг от друга только распределением электронов. В сопряженных системах основной вклад в резонансный гибрид вносят структуры с различным распределением π-электронной плотности (двусторонняя стрелка, связывающая эти структуры, является специальным символом теории резонанса).
Предельные (граничные) структуры в действительности не существуют. Однако они в той или иной степени «вносят вклад» в реальное распределение электронной плотности в молекуле (частице), которую представляют в виде резонансного гибрида, получающегося путем наложения (суперпозиции) предельных структур.
В ρ,π-сопряженных системах с уг- леродной цепью сопряжение может осуществляться при наличии рядом с π-связью атома углерода с негибридизованной р-орбиталью. Такими системами могут быть промежуточные частицы - карбанионы, карбокатионы, свободные радикалы, например, аллильной структуры. Свободнорадикальные аллильные фрагменты играют важную роль в процессах пероксидого окисления липидов.
В аллил-анионе CH 2 =CH-CH 2 sр 2 -гибридизованный атом углерода С-3 поставляет в общую сопряженную

Рис. 2.7. Карта электронной плотности группы COONa в пе- нициллине
систему два электрона, в аллильном радикале CH 2 =CH-CH 2+ - один, а в аллильном карбокатионе CH 2 =CH-CH 2+ не поставляет ни одного. В результате при перекрывании p-АО трех sp 2 -гибридизованных атомов углерода образуется делокализованная трехцентровая связь, содержащая четыре (в карбанионе), три (в свободном радикале) и два (в карбокатионе) электрона соответственно.

Формально атом С-3 в аллил-катионе несет положительный заряд, в аллильном радикале - неспаренный электрон, а в аллил-анионе - отрицательный заряд. В действительности в таких сопряженных системах имеется делокализация (рассредоточение) электронной плотности, что приводит к выравниванию связей и зарядов. Атомы С-1 и С-3 в этих системах равноценны. Например, в аллил-катионе каждый из них несет положительный заряд +1/2 и связан «полуторной» связью с атомом С-2.
Таким образом, сопряжение приводит к существенному различию в распределении электронной плотности в реальных структурах по сравнению со структурами, изображаемыми обычными формулами строения.
2.3.2. Системы с замкнутой цепью сопряжения
Циклические сопряженные системы представляют большой интерес как группа соединений с повышенной термодинамической устой- чивостью по сравнению с сопряженными открытыми системами. Эти соединения обладают и другими особыми свойствами, совокупность которых объединяют общим понятием ароматичность. К ним относятся способность таких формально ненасыщенных соединений
вступать в реакции замещения, а не присоединения, устойчивость к действию окислителей и температуры.
Типичными представителями ароматических систем являются арены и их производные. Особенности электронного строения арома- тических углеводородов наглядно проявляются в атомно-орбитальной модели молекулы бензола. Каркас бензола образуют шесть sp 2 -гибри- дизованных атомов углерода. Все σ-связи (C-C и C-H) лежат в одной плоскости. Шесть негибридизованных р-АО расположены перпендикулярно плоскости молекулы и параллельно друг другу (рис. 2.8, а). Каждая р -АО в равной степени может перекрываться с двумя соседними р -АО. В результате такого перекрывания возникает единая делокализованная π-система, наибольшая электронная плотность в которой находится над и под плоскостью σ-скелета и охватывает все атомы углерода цикла (см. рис. 2.8, б). π-Электронная плотность равномерно распределена по всей циклической системе, что обозначается кружком или пунктиром внутри цикла (см. рис. 2.8, в). Все связи между атомами углерода в бензольном кольце имеют одинаковую длину (0,139 нм), промежуточную между длинами одинарной и двойной связей.
На основании квантовомеханических расчетов установлено, что для образования таких стабильных молекул плоская циклическая система должна содержать (4n + 2) π-электронов, где n = 1, 2, 3 и т. д. (правило Хюккеля, 1931). С учетом этих данных можно конкретизировать понятие «ароматичность».
Соединение ароматично, если оно имеет плоский цикл и сопряженную π -электронную систему, охватывающую все атомы цикла и содержащую (4n + 2) π -электронов.
Правило Хюккеля применимо к любым плоским конденсированным системам, в которых нет атомов, являющихся общими более чем для

Рис. 2.8. Атомно-орбитальная модель молекулы бензола (атомы водорода опущены; объяснение в тексте)
двух циклов. Такие соединения с конденсированными бензольными ядрами, как нафталин и другие, отвечают критериям ароматичности.

Устойчивость сопряженных систем. Образование сопряженной и особенно ароматической системы - энергетически выгодный процесс, так как при этом увеличивается степень перекрывания орбиталей и происходит делокализация (рассредоточение) р -электронов. В связи с этим сопряженные и ароматические системы обладают повышенной термодинамической устойчивостью. Они содержат меньший запас внутренней энергии и в основном состоянии занимают более низкий энергетический уровень по сравнению с несопряженными системами. По разнице этих уровней можно количественно оценить термодинамическую устойчивость сопряженного соединения, т. е. его энергию сопряжения (энергию делокализации). Для бутадиена-1,3 она невелика и составляет около 15 кДж/моль. С увеличением длины сопряженной цепи энергия сопряжения и соответственно термодинамическая устойчивость соединений возрастают. Энергия сопряжения для бензола гораздо больше и составляет 150 кДж/моль.
2.4. Электронные эффекты заместителей 2.4.1. Индуктивный эффект
Полярная σ-связь в молекуле вызывает поляризацию ближайших σ-связей и ведет к возникновению частичных зарядов на соседних атомах*.
Заместители вызывают поляризацию не только «своей», но и соседних σ-связей. Этот вид передачи влияния атомов называют индуктивным эффектом (/-эффект).
Индуктивный эффект - передача электронного влияния заместителей в результате смещения электронов σ-связей.
Из-за слабой поляризуемости σ-связи индуктивный эффект затухает через три-четыре связи в цепи. Его действие наиболее сильно проявляется по отношению к атому углерода, соседнему с тем, у которого находится заместитель. Направление индуктивного эффекта заместителя качественно оценивается путем его сравнения с атомом водорода, индуктивный эффект которого принят за нуль. Графически результат /-эффекта изображают стрелкой, совпадающей с положением валентной черточки и направленной острием в сторону более электроотрицательного атома.
/в\ сильнее, чем атом водорода, проявляет отрицательный индуктив- ный эффект (-/-эффект).
Такие заместители в целом понижают электронную плотность системы, их называют электроноакцепторными. К ним относится большинство функциональных групп: OH, NH 2, COOH, NO 2 и катионных групп, например -NH 3+.
Заместитель, смещающий по сравнению с атомом водорода электронную плотность σ -связи в сторону атома углерода цепи, проявляет положительный индуктивный эффект (+/-эффект).
Такие заместители повышают электронную плотность в цепи (или кольце) и называются электронодонорными. К их числу относятся алкильные группы, находящиеся у sр 2 -гибридизованного атома углерода, и анионные центры в заряженных частицах, например -О - .
2.4.2. Мезомерный эффект
В сопряженных системах в передаче электронного влияния основную роль играют π-электроны делокализованных ковалентных связей. Эффект, проявляющийся в смещении электронной плотности делокализованной (сопряженной) π-системы, называют мезомерным (M-эффект), или эффектом сопряжения.
Мезомерный эффект - передача электронного влияния заместителей по сопряженной системе.
При этом заместитель сам является участником сопряженной системы. Он может вносить в систему сопряжения либо π-связь (карбонильная, карбоксильная группы и др.), либо неподеленную пару электронов гетероатома (амино- и гидроксигруппы), либо вакантную или заполненную одним электроном р-АО.
Заместитель, повышающий электронную плотность в сопряженной системе, проявляет положительный мезомерный эффект (+М- эффект).
М-Эффектом обладают заместители, включаю- щие атомы с неподеленной парой электронов (например, аминогруппа в молекуле анилина) или целым отрицательным зарядом. Эти заместители способны
к передаче пары электронов в общую сопряженную систему, т. е. являются электронодонорными.
Заместитель, понижающий электронную плотность в сопряженной системе, проявляет отрицательный мезомерный эффект (-М- эффект).
М-Эффектом в сопряженной системе обладают атомы кислорода или азота, связанные двойной связью с атомом углерода, как показано на примере акриловой кислоты и бензальдегида. Такие группировки являются электроноакцепторными.


Смещение электронной плотности обозначается изогнутой стрелкой, начало которой показывает, какие р- или π-электроны смещаются, а конец - связь или атом, к которым они смещаются. Мезомерный эффект, в отличие от индуктивного, передается по системе сопряженных связей на значительно большее расстояние.
При оценке влияния заместителей на распределение электронной плотности в молекуле необходимо учитывать результирующее действие индуктивного и мезомерного эффектов (табл. 2.2).
Таблица 2.2. Электронные эффекты некоторых заместителей

Электронные эффекты заместителей позволяют дать качественную оценку распределения электронной плотности в нереагирующей молекуле и прогнозировать ее свойства.
Связи между атомами, изображаемые в структурных формулах в виде черточек или палочек (стерженьков), образуются при взаимодействии внешних (валентных) электронов 2-х атомов одной молекулы. По характеру этого взаимодействия различают два основных или крайних типа связей между атомами.
1-ый тип. Ионная, или электровалентная, или солевая связь наиболее ярко (в чистом виде) представлена в случае взаимодействия атома сильного металла (например, щелочного) и атома сильного неметалла (например, галогена). Атом щелочного металла, теряя единственный внешний электрон, становится положительно заряженной частицей, а атом галогена, приобретая один внешний электрон, заряжается отрицательно: Na + - CI - . Прочность этой связи обусловлена кулоновскими силами притяжения между разнозаряженными частицами и энергией, выделяемой при образовании новой электронной пары у атома галогена. Примерами являются соли органических и неорганических кислот.
2-ой крайний тип. Более характерная для органических соединений ковалентная (или атомная) связь ярко (в чистом виде) представлена в 2-х атомных молекулах газов: Н 2 , O 2 , N 2 , С1 2 и др. в которых связь образована между совершенно одинаковыми атомами. В результате спаривания двух с противоположными спинами электронов двух атомов при их приближении друг к другу выделяется определенное количество энергии (≈ 400 кдж/моль) и новая электронная пара приобретает молекулярную орбиту, занимая в обоих атомах по одной ячейке. Причем наибольшая плотность электронного облака этой пары находится между атомами (происходит как бы перекрывание атомных орбит обоих электронов, рис. а) или образование молекулярной орбиты – рис б).

Хотя изображение б) более близко к истине, правомерны и применяются оба изображения ковалентной связи. В чисто ковалентной связи не происходит никакого отклонения центров положительных и отрицательных зарядов молекулы, они совпадают - молекула неполярна.
Кроме этих 2-х крайних типов связей (ионная и ковалентная) существуют промежуточные типы: 3) полярная, 4) полуполярная, 5) координационная, встречающаяся в основном в так называемых ониевых соединениях (оксониевых, аммониевых, сульфониевых).
В полярной связи электронная пара, находящаяся одновременно в поле центров обоих атомов (их ядер), отклонена в сторону более электроотрицательного атома, как например, в молекуле НС1 электронная пара больше находится в ячейке хлора, чем водорода:
Из-за этого отклонения электронной плотности произошло расхождение центров положительных и отрицательных зарядов молекулы. Она стала полярной, обладающей дипольным моментом (т.е. произведением заряда на половину расстояния между зарядами), неравным нулю.
Полуполярная связь наиболее ярко представлена в кислородных соединениях пятивалентного азота:
Изображение а) хотя допускается, но неправомочно, ибо у атома азота имеется только два электронных уровня (слоя), где на внешнем (2-ом) -слое имеется только четыре ячейки ипять пар электронов (пяти связей) не найдут там места. В связи с этим более верно изображение б), где показан резонанс крайних структур (I и III) и переход к более энергетически выгодной средней структуре. Таким образом, из-за симметричного распределения электронной плотности отрицательный заряд делится на половину между двумя равноценными атомами кислорода. Но в атоме азота на самом деле нет целого положительного заряда, а есть положительный заряд, близкий целому, соответственно, на атомах кислорода (структура П) имеются отрицательные заряды, близкие половине целого заряда.
Координационная связь наиболее устойчива в соединениях аммония, где атом азота становится четырехвалентным, отдавая протону (а в водной среде катиону гидроксония) один электрон, приобретая положительный заряд (или, другими словами, присоединяя протон к неподеленной паре электронов азота): Н 3 N: + Н + → Н 4 N +
аммиак протон катион аммония
В катионе аммония, образовавшаяся новая связь, видоизменяет природу ранее имевшихся у азота трех других связей N - Н, которые теперь становятся более вытянутыми, и все четыре атома водорода аммония, взаимно отталкиваясь, становятся в самые отдаленные друг от друга положения, а именно по углам правильного тетраэдра при нахождении атома азота в центре этого тетраэдра:

Образовавшаяся новая связь (координационная), ничем не отличается от видоизменившихся связей N - Н, ранее имевшихся в молекуле аммиака. Здесь имеет место s 1 р 3 - гибридизация четырех оставшихся у азота электронов (как у углерода метана).
Если молекула метана сравнительно прочное образование, не имеющее заряда, то катион аммония (отличающееся от него по строению лишь тем, что ядро центрального атома содержит на один протон и один нейтрон больше) менее устойчив и может легко диссоциировать на аммиак и катион гидроксония, преодолевая определенный энергетический барьер, обуславливающий прочность аммонийных соединений.
Понятие о σ -(сигма) и π- (пи) связях
Ковалентные связи, преобладающие в органических соединениях, в целом определяют химическую активность этих веществ. Однако большое значение имеют непрочные кратные связи (двойные, тройные) и особенности связей в функциональных группах.
Углерод - центральный элемент органического мира, углеродные скелеты (остовы молекул) определяют их устойчивость и практически безграничное их многообразие. Следует потому несколько подробнее рассмотреть электронную природу его связей.
Атом углерода имеет ядро с зарядом +6, и электронную оболочку: 1s 2 , 2s 2 , 2р 2 , где валентными являются четыре внешних электрона (2s 2 , 2р 2). Но, чтобы эти электроны могли образовать четыре связи, 2s 2 -электроны, находящиеся в объеме шара в спаренном виде, должны перейти в неспаренное состояние. И возбужденный атом углерода должен иметь оболочку: 1s 2 , 2s 1 , 2р 3 , где наряду с неспаренным s-электроном (формы шара) имеется три р-электрона (формы объемных восьмерок или гантелей), расположенные по осям координат (х, у, z) трехмерного пространства (рис. 3). Однако, чтобы образоватьчетыре равноценных между собой связи, как в метане, один s-электрон и три р-электрона должны перейти в видоизмененное гибридизированное (s 1 р 3 -гибридизация) состояние, причем все четыре внешних электрона уже имеют совершенно одинаковые направленные (гибридные) формы облаков, а атомы водорода метана находятся на равных, наиболее отдаленных друг от друга положениях:

которые соответствуют вершинам правильного тетраэдра, если в центре его поместить атом углерода метана (рис. 4). Состояние углерода, когда имеет место гибридизация валентных электронов в соотношении s 1 р 3 , и называется первым валентным состоянием углерода,
а связи такого атома с другими атомами называют б(сигма)-связями
(рис. 5, 6). 
Таким образом, σ-связь - это любая одинарная связь углерода с другим атомом. И наиболее распространенные в молекулах органических веществ C-H и C-H σ-связь имеют следующие основные данные (рис. 6б, 6в).
С-Н энергия связи ~93-96 ккал/моль (~370-380 кдж/моль).
Длина связи 1,1 А 0 (0,11 нм)
С-С энергия связи ~84-86 ккал/моль (~340-360 кдж/моль)
Длина связи 1,54 А 0 (0,154 нм)
Второе валентное состояние углерода характерно для этилена и других соединений с двойной связью. У углерода этилена имеет место гибридизация валентных электронов возбужденного атома (2s 1 , 2р 3) в соотношении s 1 p 2 , когда один р-электрон (из трех) не участвует в гибридизации и остается в р-форме. И гибридные облака направленной (вытянутой) формы располагаются в плоскости под углом друг к другу 120° (рис. 7).

А р-электроны двух углеродов спариваются в р-форме дополнительно к σ-связи между этими углеродами (рис. 7). Вот эта дополнительная (кратная) связь, образованная спариванием электронов в р-форме, и называется π (пи) - связью. Энергия, выделяемая при ее образовании, меньше энергии σ-связи, ибо энергия С = С двойной связи составляет ~140 ккал/моль (~560-580 кдж/моль). Если отсюда отнять энергию С - С σ-связи (~85 ккал/моль), то на π -связь остается ~55 ккал/моль (140-85=55).
Третье валентное состояние углерода характерно для ацетилена и других соединений с тройной связью. У углерода ацетилена из четырех валентных электронов (2s 1 , 2р 3) возбужденного атома в гибридизации участвуют по одному s- и р-электрону (s 1 p 1 - гибридизация). И гибридные (вытянутые) два облака располагаются на одной прямой, образуя σ-связи (рис. 8). То есть они занимают наиболее отдаленные положения (z-координату) уже от 2-х оставшихся в р-форме электронов, находящихся по осям координат (х,у) трехмерного пространства, спарившихся в р-форме с образованием двух π -связей во взаимно перпендикулярных плоскостях (рис. 8). Энергия, выделяемая при образовании тройной связи, составляет ~200 ккал/моль. Если отсюда отнять 85 ккал/моль - энергию σ-связи, то на две π-связи остается ~115 ккал/м, т.е. по ~57 ккал/моль на каждую π-связь. Приводим основные характеристики одинарной, двойной и тройной связей для сравнения:
С - С длина связи 1,54 А 0 , энергия образования связи ~85 ккал/моль
С = С длина связи 1,34 А 0 , энергия образования связи ~140 ккал/моль
С ≡ С длина связи 1,21 А 0 , энергия образования связи ~200 ккал/моль Электроны π-связей более объемны, слабее связаны с ядрами атомов, более доступны атаке реагента, легко подвергаются действию электрических и магнитных полей, например, падающего света или атаке заряженных частиц. Поэтому π -связи, обладая совершенно иной природой по сравнению с σ-связями, менее устойчивы и обуславливают высокую химическую активность непредельных соединений по сравнению с предельными (насыщенными) соединениями.
Многообразие неорганических и органических веществ
Органическая химия - это химия соединений углерода . К неорганическим соединениям углерода относят: оксиды углерода, угольную кислоту, карбонаты и гидрокарбонаты, карбиды. Органические вещества, кроме углерода, содержат водород, кислород, азот, фосфор, серу и др. элементы . Атомы углерода могут образовывать длинные неразветвленные и разветвленные цепи, кольца, присоединять другие элементы, поэтому число органических соединений приблизилось к 20 млн, тогда как неорганических веществ насчитывается немногим более 100 тысяч.
Основой развития органической химии является теория строения органических соединений А. М. Бутлерова. Важная роль в описании строения органических соединений принадлежит понятию валентности, которая характеризует способность атомов к образованию химических связей и определяет их число. Углерод в органических соединениях всегда четырехвалентен . Основным постулатом теории А. М. Бутлерова является положение о химическом строении вещества, т. е. химическая связь. Этот порядок отображают при помощи структурных формул. Теория Бутлерова утверждает идею о том, что каждое вещество имеет определенное химическое строение исвойства веществ зависят от строения .

Теория химического строения органических соединений А. М. Бутлерова
Подобно тому, как для неорганической химии основой развития являются Периодический закон и Периодическая система химических элементов Д. И. Менделеева, для органической химии основополагающей стала .
 Теория химического строения органических соединений А. М. Бутлерова
Теория химического строения органических соединений А. М. Бутлерова
Основным постулатом теории Бутлерова является положение о химическом строении вещества, под которым понимается порядок, последовательность взаимного соединения атомов в молекулы, т. е. химическая связь .
Химическое строение - порядок соединения атомов химических элементов в молекуле согласно их валентности.
Этот порядок может быть отображен при помощи структурных формул, в которых валентности атомов обозначаются черточками: одна черточка соответствует единице валентности атома химического элемента . Например, для органического вещества метана, имеющего молекулярную формулу СН 4 , структурная формула выглядит так:

Основные положения теории А. М. Бутлерова:
· Атомы в молекулах органических веществ связаны друг с другом согласно их валентности . Углерод в органических соединениях всегда четырехвалентен, а его атомы способны соединяться друг с другом, образуя различные цепи.
· Свойства веществ определяются не только их качественным и количественным составом, но и порядком соединения атомов в молекуле, т. е. химическим строением вещества .
· Свойства органических соединений зависят не только от состава вещества и порядка соединения атомов в его молекуле, но и от взаимного влияния атомов и групп атомов друг на друга.
Теория строения органических соединений является динамичным и развивающимся учением. По мере развития знаний о природе химической связи, о влиянии электронного строения молекул органических веществ стали пользоваться, кроме эмпирических и структурных, электронными формулами. В таких формулах показывают направление смещения электронных пар в молекуле .
Квантовая химия и химия строения органических соединений подтвердили учение о пространственном направлении химических связей (цис- и транс изомерия), изучили энергетические характеристики взаимных переходов у изомеров, позволили судить о взаимном влиянии атомов в молекулах различных веществ, создали предпосылки для прогнозирования видов изомерии и направлений и механизмов протекания химических реакций.
Органические вещества имеют ряд особенностей.
· В состав всех органических веществ входят углерод и водород, поэтому при горении они образуют углекислый газ и воду .
· Органические вещества построены сложно и могут иметь огромную молекулярную массу (белки, жиры, углеводы).
· Органические вещества можно расположить в ряды сходных по составу, строению и свойствам гомологов .
· Для органических веществ характерной является изомерия .
Изомерия и гомология органических веществ
Свойства органических веществ зависят не только от их состава, но и от порядка соединения атомов в молекуле .

Изомерия - это явление существования разных веществ - изомеров с одинаковым качественным и количественным составом, т. е. с одинаковой молекулярной формулой.
Различают два вида изомерии: структурную и пространственную (стереоизомерию). Структурные изомеры отличаются друг от друга порядком связи атомов в молекуле; стереоизомеры - расположением атомов в пространстве при одинаковом порядке связей между ними.
Основные виды изомерии:
· Структурная изомерия - вещества различаются порядком связи атомов в молекулах:
1) изомерия углеродного скелета;
2) изомерия положения:
- кратных связей;
- заместителей;
- функциональных групп;
3) изомерия гомологических рядов (межклассовая).
· Пространственная изомерия - молекулы веществ отличаются не порядком связи атомов, а положением их в пространстве: цис-, транс-изомерия (геометрическая).


Классификация органических веществ
Известно, что свойства органических веществ определяются их составом и химическим строением. Поэтому неудивительно, что в основе классификации органических соединений лежит именно теория строения - теория А. М. Бутлерова. Классифицируют органические вещества по наличию и порядку соединения атомов в их молекулах. Наиболее прочной и малоизменяемой частью молекулы органического вещества является ее скелет - цепь атомов углерода . В зависимости от порядка соединения атомов углерода в этой цепи вещества делятся на ациклические , не содержащие замкнутых цепей атомов углерода в молекулах, и карбоциклические , содержащие такие цепи (циклы) в молекулах.
Помимо атомов углерода и водорода молекулы органических веществ могут содержать атомы и других химических элементов. Вещества, в молекулах которых эти так называемые гетероатомы включены в замкнутую цепь, относят к гетероциклическим соединениям.
Гетероатомы (кислород, азот и др.) могут входить в состав молекул и ациклических соединений, образуя в них функциональные группы, например,
гидроксильную
карбонильную
 ,
,
карбоксильную
 ,
,
аминогруппу
 .
.
Функциональная группа - группа атомов, которая определяет наиболее характерные химические свойства вещества и его принадлежность к определенному классу соединений.
Номенклатура органических соединений
В начале развития органической химии открываемым соединениям присваивались тривиальные названия , часто связанные с историей их получения: уксусная кислота (являющаяся основой винного уксуса), масляная кислота (образующаяся в сливочном масле), гликоль (т. е. «сладкий») и т. д. По мере увеличения числа новых открытых веществ возникла необходимость связывать названия с их строением. Так появились рациональные названия: метиламин, диэтиламин, этиловый спирт, метилэтилкетон, в основе которых лежит название простейшего соединения. Для более сложных соединений рациональная номенклатура непригодна.

Теория строения А. М. Бутлерова дала основу для классификации и номенклатуры органических соединений по структурным элементам и по расположению атомов углерода в молекуле. В настоящее время наиболее употребляемой является номенклатура, разработанная Международным союзом теоретической и прикладной химии (IUPAC) , которая называется номенклатурой ИЮПАК . Правила ИЮПАК рекомендуют для образования названий несколько принципов, один из них - принцип замещения. На основе этого разработана заместительная номенклатура, которая является наиболее универсальной. Приведем несколько основных правил заместительной номенклатуры и рассмотрим их применение на примере гетерофункционального соединения, содержащего две функциональные группы, - аминокислоты лейцина:

1. В основе названия соединений лежит родоначальная структура (главная цепь ациклической молекулы, карбоциклическая или гетероциклическая система). Название родоначальной структуры составляет основу названия, корень слова.
В данном случае родоначальной структурой является цепь из пяти атомов углерода, связанных одинарными связями. Таким образом, коренная часть названия - пентан.
2. Характеристические группы и заместители (структурные элементы) обозначаются префиксами и суффиксами. Характеристические группы подразделяются по старшинству. Порядок старшинства основных групп:
Выявляют старшую характеристическую группу, которую обозначают в суффиксе. Все остальные заместители называют в префиксе в алфавитном порядке.
В данном случае старшей характеристической группой является карбоксильная, т. е. это соединение относится к классу карбоновых кислот, поэтому к коренной части названия добавляем -овая кислота. Второй по старшинству группой является аминогруппа, которая обозначается префиксом амино-. Кроме этого, молекула содержит углеводородный заместитель метил-. Таким образом, основой названия является аминометилпентановая кислота.
3. В название включают обозначение двойной и тройной связи, которое идет сразу после корня.
Рассматриваемое соединение не содержит кратных связей.
4. Атомы родоначальной структуры нумеруют. Нумерацию начинают с того конца углеродной цепи, к которому ближе расположена старшая характеристическая группа:

Нумерацию цепи начинают с атома углерода, входящего в состав карбоксильной группы, ему присваивается номер 1. В этом случае аминогруппа окажется при углероде 2, а метил - при углероде 4.
Таким образом, природная аминокислота лейцин по правилам номенклатуры ИЮПАК называется 2-амино-4-метилпентановая кислота.
Углеводороды. Классификация углеводородов
Углеводороды - это соединения, состоящие только из атомов водорода и углерода.




В зависимости от строения углеродной цепи органические соединения разделяют на соединения с открытой цепью - ациклические (алифатические) и циклические - с замкнутой цепью атомов.
Циклические делятся на две группы: карбоциклические соединения (циклы образованы только атомами углерода) и гетероциклические (в циклы входят и другие атомы, такие как кислород, азот, сера).
Карбоциклические соединения, в свою очередь, включают два ряда соединений: алицикличвские и ароматические .
Ароматические соединения в основе строения молекул имеют плоские углеродсодержащие циклы с особой замкнутой системой р-электронов , образующих общую π-систему (единое π-электронноеоблако). Ароматичность характерна и для многих гетероциклических соединений.
Все остальные карбоциклические соединения относятся к алициклическому ряду.
Как ациклические (алифатические), так и циклические углеводороды могут содержать кратные (двойные или тройные) связи. Такие углеводороды называют непредельными (ненасыщенными) в отличие от предельных (насыщенных), содержащих только одинарные связи.
Предельные алифатические углеводороды называют алканами , они имеют общую формулу С n Н 2n+2 , где n - число атомов углерода. Старое их название часто употребляется и в настоящее время - парафины:
Непредельные алифатические углеводороды, содержащие одну двойную связь, получили название алкены . Они имеют общую формулу C n H 2n:

Непредельные алифатические углеводороды с двумя двойными связями называют алкадиенами . Их общая формула C n H 2n-2:
Непредельные алифатические углеводороды с одной тройной связью называют алкинами . Их общая формула C n H 2n — 2:

Предельные алициклические углеводороды - циклоалканы , их общая формула С n Н 2n:

Особая группа углеводородов, ароматических, или аренов (с замкнутой общей л-электронной системой), известна из примера углеводородов с общей формулой С n Н 2n — 6:

Таким образом, если в их молекулах один или большее число атомов водорода заменить на другие атомы или группы атомов (галогены, гидроксильные группы, аминогруппы и др.), образуются производные углеводородов: галогенопроизводные, кислородсодержащие, азотсодержащие и другие органические соединения.
Гомологический ряд углеводородов
Углеводороды и их производные с одной и той же функциональной группой образуют гомологические ряды.
Гомологическим рядом называют ряд соединений, принадлежащих к одному классу (гомологов), расположенных в порядке возрастания их относительных молекулярных масс, сходных по строению и химическим свойствам, где каждый член отличается от предыдущего на гомологическую разность CH 2 . Например: CH 4 - метан, C 2 H 6 - этан, C 3 H 8 - пропан, C 4 H 10 - бутан и т. д. Сходство химических свойств гомологов значительно упрощает изучение органических соединений.
Изомеры углеводородов
Те атомы или группы атомов, которые определяют самые характерные свойства данного класса веществ, называются функциональными группами .

Галогенопроизводные углеводородов можно рассматривать как продукты замещения в углеводородах одного или нескольких атомов водорода атомами галогенов. В соответствии с этим могут существовать предельные и непредельные моно-, ди-, три- (в общем случае поли-) галогенопроизводные .
Общая формула моногалогенопроизводных предельных углеводородов:

а состав выражается формулой

где R - остаток от предельного углеводорода (алкана), углеводородный радикал (это обозначение используется и далее при рассмотрении других классов органических веществ), Г - атом галогена (F, Cl, Br, I).
Например:

Приведем один пример дигалогенопроизводного:

К кислородсодержащим органическим веществам относят спирты, фенолы, альдегиды, кетоны, карбоновые кислоты, простые и сложные эфиры. Спирты - производные углеводородов, в которых один или несколько атомов водорода замещены на гидроксильные группы.
Спирты называют одноатомными, если они имеют одну гидроксильную группу, и предельными, если они являются производными алканов.
Общая формула предельных одноатомных спиртов :

а их состав выражается общей формулой:
Например:

Известны примеры многоатомных спиртов , т. е. имеющих несколько гидроксильных групп:

Фенолы - производные ароматических углеводородов (ряда бензола), в которых один или несколько атомов водорода в бензольном кольце замещены на гидроксильные группы.
Простейший представитель с формулой C 6 H 5 OH или

называется фенолом.
Альдегиды и кетоны - производные углеводородов, содержащие карбонильную группу атомов

(карбонил).
В молекулах альдегидов одна связь карбонила идет на соединение с атомом водорода, другая - с углеводородным радикалом. Общая формула альдегидов:

Например:

В случае кетонов карбонильная группа связана с двумя (в общем случае разными) радикалами, общая формула кетонов:

Например:

Состав предельных альдегидов и кетонов выражается формулой С 2n Н 2n О.
Карбоновые кислоты - производные углеводородов, содержащие карбоксильные группы

(или -СООН).
Если в молекуле кислоты одна карбоксильная группа, то карбоновая кислота является одноосновной. Общая формула предельных одноосновных кислот:

Их состав выражается формулой С n Н 2n О 2 .
Например:

Простые эфиры представляют собой органические вещества, содержащие два углеводородных радикала, соединенных атомом кислорода: R-O-R или R 1 -O-R 2 .
Радикалы могут быть одинаковыми или разными. Состав простых эфиров выражается формулой C n H 2n+2 O.
Например:
Сложные эфиры - соединения, образованные замещением атома водорода карбоксильной группы в карбоновых кислотах на углеводородный радикал.
Общая формула сложных эфиров:

Например:

Нитросоединения - производные углеводородов, в которых один или несколько атомов водорода замещены на нитрогруппу -NO 2 .
Общая формула предельных мононитросоединений:

а состав выражается общей формулой C n H 2n+1 NO 2 .
Например:

Нитропроизводные аренов:

Амины - соединения, которые рассматривают как производные аммиака (NH 3), в котором атомы водорода замещены на углеводородные радикалы. В зависимости от природы радикала амины могут быть алифатическими, например:

и ароматическими, например:

В зависимости от числа замещенных на радикалы атомов водорода различают:
первичные амины с общей формулой:

вторичные - с общей формулой:

третичные - с общей формулой:

В частном случае у вторичных, а также третичных аминов радикалы могут быть и одинаковыми.
Первичные амины можно также рассматривать как производные углеводородов (алканов), в которых один атом водорода замещен на аминогруппу -NH 2 . Состав предельных первичных аминов выражается формулой C n H 2n + 3 N.
Например:

Аминокислоты содержат две функциональные группы, соединенные с углеводородным радикалом: аминогруппу -NH 2 и карбоксил -COOH.
Общая формула α-аминокислот (они наиболее важны для построения белков, из которых состоят живые организмы):

Состав предельных аминокислот, содержащих одну аминогруппу и один карбоксил, выражается формулой C n H 2n+1 NO 2.
Например:

Известны и другие важные органические соединения, которые имеют несколько разных или одинаковых функциональных групп, длинные линейные цепи, связанные с бензольными кольцами. В таких случаях строгое определение принадлежности вещества к какому-то определенному классу невозможно. Эти соединения часто выделяют в специфические группы веществ: углеводы, белки, нуклеиновые кислоты, антибиотики, алкалоиды и др.
В настоящее время известно также много соединений, которые можно отнести и к органическим, и к неорганическим. х называют элементоорганическими соединениями. Некоторые из них можно рассматривать как производные углеводородов.
Например:

Существуют соединения, имеющие одинаковую молекулярную формулу, выражающую состав веществ.
Явление изомерии состоит в том, что могут существовать несколько разных по свойствам веществ, имеющих одинаковый состав молекул, но разное строение. Эти вещества называют изомерами.
В нашем случае это межклассовые изомеры: циклоалканы и алканы, алкадиены и алкины, предельные одноатомные спирты и простые эфиры, альдегиды и кетоны, предельные одноосновные карбоновые кислоты и сложные эфиры.


Структурная изомерия
Выделяют следующие разновидности структурной изомерии : изомерию углеродного скелета, изомерию положения, изомерию различных классов органических соединений (межклассовую изомерию).
Изомерия углеродного скелета обусловлена различным порядком связи между атомами углерода , образующими скелет молекулы. Как уже было показано, молекулярной формуле С 4 Н 10 соответствуют два углеводорода: н-бутан и изобутан. Для углеводорода С 5 Н 12 возможны три изомера: пентан, изопентан и неопентан.

C увеличением числа атомов углерода в молекуле число изомеров быстро растет. Для углеводорода С 10 Н 22 их уже 75, а для углеводорода С 20 Н 44 - 366 319.
Изомерия положения обусловлена различным положением кратной связи, заместителя, функциональной группы при одинаковом углеродном скелете молекулы:

Изомерия различных классов органических соединений (межклассовая изомерия) обусловлена различным положением и сочетанием атомов в молекулах веществ, имеющих одинаковую молекулярную формулу, но принадлежащих к разным классам. Так, молекулярной формуле С 6 Н 12 соответствует ненасыщенный углеводород гексен-1 и циклический углеводород циклогексан.

Изомерами являются углеводород, относящийся к алкинам, - бутин-1 и углеводород с двумя двойными связями в цепи бутадиен-1,3:
Диэтиловый эфир и бутиловый спирт имеют одинаковую молекулярную формулу С 4 Н 10 O:
Структурными изомерами являются аминоуксусная кислота и нитроэтан, отвечающие молекулярной формуле С 2 Н 5 NO 2:

Изомеры этого типа содержат различные функциональные группы и относятся к разным классам веществ. Поэтому они отличаются по физическим и химическим свойствам значительно больше, чем изомеры углеродного скелета или изомеры положения.
Пространственная изомерия
Пространственная изомерия подразделяется на два вида: геометрическую и оптическую.
Геометрическая изомерия характерна для соединений, содержащих двойные связи, и циклических соединений . Так как свободное вращение атомов вокруг двойной связи или в цикле невозможно, заместители могут располагаться либо по одну сторону плоскости двойной связи или цикла (цис-положение), либо по разные стороны (трансположение). Обозначения цис- и транс- обычно относят к паре одинаковых заместителей.

Геометрические изомеры различаются по физическим и химическим свойствам .
Оптическая изомерия возникает, если молекула несовместима со своим изображением в зеркале . Это возможно, когда у атома углерода в молекуле четыре различных заместителя. Этот атом называют асимметрическим. Примером такой молекулы является молекула α-аминопропионовой кислоты (α-аланина) CH 3 CH(NH 2)OH.
Молекула α-аланина ни при каком перемещении не может совпасть со своим зеркальным отражением. Такие пространственные изомеры называются зеркальными, оптическими антиподами, или энантиомерами. Все физические и практически все химические свойства таких изомеров идентичны.
Изучение оптической изомерии необходимо при рассмотрении многих реакций, протекающих в организме. Большинство этих реакций идет под действием ферментов - биологических катализаторов. Молекулы данных веществ должны подходить к молекулам соединений, на которые они действуют, как ключ к замку, следовательно, пространственное строение, взаимное расположение участков молекул и другие пространственные факторы имеют для течения этих реакций большое значение. Такие реакции называются стереоселективными.
Большинство природных соединений являются индивидуальными энантиомерами, и их биологическое действие (начиная от вкуса и запаха и заканчивая лекарственным действием) резко отличается от свойств их оптических антиподов, полученных в лаборатории. Подобное различие в биологической активности имеет огромное значение, так как лежит в основе важнейшего свойства всех живых организмов - обмена веществ.

 Изомерия
Изомерия
Электронное строение атома углерода
Углерод, входящий в состав органических соединений проявляет постоянную валентность. На последнем энергетическом уровне атома углерода содержится 4 электрона , два из которых занимают 2s-орбиталь, имеющую сферическую форму, а два электрона занимают 2р-орбитали, имеющие гантелеподобную форму. При возбуждении один электрон из 2s-орбитали может переходить на одну из вакантных 2р-орбиталей. Этот переход требует некоторых энергетических затрат (403 кДж/моль). В результате возбужденный атом углерода имеет 4 неспаренных электрона и его электронная конфигурация выражается формулой 2s 1 2p 3 .. Так, в случае углеводорода метана (СН 4) атом углерода образует 4 связи с s-электронами атомов водорода. При этом должны были бы образовываться 1 связь типа s-s (между s-электроном атома углерода и s-электроном атома водорода) и 3 p-s-связи (между 3 р-электронами атома углерода и 3 s-электронами 3-х атомов водорода). Отсюда вытекает вывод о неравноценности четырех ковалентных связей, образуемых атомом углерода. Однако, практический опыт химии свидетельствует о том, что все 4 связи в молекуле метана абсолютно равноценны, а молекула метана имеет тетраэдрическое строение с валентными углами 109,5 0 , чего не могло бы быть при неравноценности связей. Ведь только орбитали р-электронов ориентированы в пространстве по взаимно перпендикулярным осям x, y, z, а орбиталь s-электрона имеет сферическую форму, поэтому направление образования связи с этим электроном было бы произвольным. Объяснить это противоречие смогла теория гибридизации. Л.Поллинг высказал предположение, что в любых молекулах не существует изолированных друг от друга связей. При образовании связей орбитали всех валентных электронов перекрываются. Известно несколько типов гибридизации электронных орбиталей . Предполагается, что в молекуле метана и других алканов в гибридизацию вступает 4 электрона.
Гибридизация орбиталей атома углерода
Гибридизация орбиталей — это изменение формы и энергии некоторых электронов при образовании ковалентной связи, приводящее к более эффективному перекрыванию орбиталей и повышению прочности связей. Гибридизация орбиталей происходит всегда, когда в образовании связей участвуют электроны, принадлежащие к различным типам орбиталей.


1. sp 3 -гибридизация (первое валентное состояние углерода). При sp 3 -гибридизации 3 р-орбитали и одна s-орбиталь возбужденного атома углерода взаимодействуют таким образом, что получаются орбитали абсолютно одинаковые по энергии и симметрично расположенные в пространстве. Это преобразование можно записать так:

При гибридизации общее число орбиталей не изменяется, а изменяется только их энергия и форма. Показано, что sр 3 -гибридизация орбитали напоминают объемную восьмерку, одна из лопастей которой значительно больше другой. Четыре гибридных орбитали вытянуты от центра к вершинам правильного тетраэдра под углами 109,5 0 . Связи образованные гибридными электронами (например связь s-sp 3) более прочные, чем связи, осуществляемые негибридизованными р-электронами (например, связь-s-p). Поскольку гибридная sp 3 -орбиталь обеспечивает большую площадь перекрывания электронных орбиталей, чем негибридизованная р-орбиталь. Молекулы, в которых осуществляется sp 3 — гибридизация имеют тетраэдрическое строение. К ним, кроме метана, относятся гомологи метана, неорганические молекулы типа аммиака. На рисунках показана гибридизованная орбиталь и тетраэдрическая молекула метана.


Химические связи, возникающие в метане между атомами углерода и водорода относятся к типу σ-связей (sp 3 -s-связь). Вообще говоря любая сигма-связь характеризуется тем, что электронная плотность двух связанных между собой атомов, перекрывается по линии, соединяющей центры (ядра) атомов. σ-Связи отвечают максимально возможной степени перекрывания атомных орбиталей, поэтому они достаточно прочны.
2. sp 2 -гибридизация (второе валентное состояние углерода). Возникает в результате перекрывания одной 2s и двух 2р орбиталей. Образовавшиеся sp 2 -гибридные орбитали располагаются в одной плоскости под углом 120 0 друг к другу, а негибридизованная р-орбиталь перпендикулярно к ней. Общее число орбиталей не меняется — их четыре.
Состояние sp 2 -гибридизации встречается в молекулах алкенов, в карбонильной и карбоксильной группах, т.е. у соединений, имеющих в своем составе двойную связь. Так, в молекуле этилена гибридизованные электроны атома углерода образуют 3 σ-связи (две связи типа sp 2 -s между атомом углерода и атомами водорода и одна связь типа sp 2 -sp 2 между атомами углерода). Оставшийся негибридизованным р-электрон одного атома углерода образует π-связь с негибридизованным р-электроном второго атома углерода. Характерной особенностью π-связи является то, что перекрывание орбиталей электронов идет вне линии, соединяющей два атома. Перекрывание орбиталей идет выше и ниже σ-связи, соединющей оба атома углерода. Таким образом двойная связь является комбинацией σ- и π-связей. На первых двух рисунках показано, что в молекуле этилена валентные углы между атомами, образующими молекулу этилена, составляют 120 0 (соответственно ориентации с пространстве трех sp 2 -гибридных орбиталей). На рисунках показано образование π-связи.


Поскольку площадь перекрывания негибридизованных р-орбиталей в π-связях меньше, чем площадь перекрывания орбиталей в σ-связях, то π-связь менее прочна, чем σ-связь и легче разрывается в химических реакциях.
3. sp-гибридизация (третье валентное состояние углерода). В состоянии sр-гибридизации атом углерода имеет две sр-гибридные орбитали, расположенные линейно под углом 180 0 друг к другу и две негибридизованные р-орбитали расположенные в двух взаимно перпендикулярных плоскостях. sр-гибридизация характерна для алкинов и нитрилов, т.е. для соединений, имеющих в своем составе тройную связь.
Так, в молекуле ацетилена валентные углы между атомами составляют 180 o . Гибридизованные электроны атома углерода образуют 2 σ-связи (одна связь sp-s между атомом углерода и атомом водорода и другая связь типа sp-sp между атомами углерода. Два негибридизованных р-электрона одного атома углерода образуют две π-связи с негибридизованными р электронами второго атома углерода. Перекрывание орбиталей р-электронов идет не только выше и ниже σ-связи, но и спереди и сзади, а суммарное облако р-электронов имеет цилиндрическую форму. Таким образом тройная связь является комбинацией одной σ-связи и двух π-связей. Наличие в молекуле ацетилена менее прочных двух π-связей, обеспечивает способность этого вещества вступать в реакции присоединения с разрывом тройной связи.


Справочный материал для прохождения тестирования:
Таблица Менделеева
Таблица растворимости
В основном состоянии атом углерода С (1s 2 2s 2 2p 2) имеет два неспаренных электрона, за счет которых могут образовать только две общие электронные пары. Однако в большинстве своих соединений углерод четырехвалентен. Это объясняется тем, что атом углерода, поглощая небольшое количество энергии, переходит в возбужденное состояние, в котором он имеет 4 неспаренных электрона, т.е. способен образовывать четыре ковалентные связи и принимать участие в формировании четырех общих электронных пар:
6 С 1s 2 2s 2 2p 2 6 С * 1s 2 2s 1 2p 3 .
| ↓ | ||||||||||||
| 1 | ↓ | p | ↓ | p | ||||||||
| s | s | |||||||||||
Энергия возбуждения компенсируется образованием химических связей, которое происходит с выделением энергии.
Атомы углерода обладают способностью к образованию трех видов гибридизации электронных орбиталей (sp 3 , sp 2 , sp ) и образованию между собой кратных (двойных и тройных) связей (табл. 2.2).
Таблица 2.2
Типы гибридизации и геометрия молекул
Простая (одинарная) s- связь осуществляется при sp 3 -гибридизации, при которой все четыре гибридных орбитали равноценны и имеют направленность в пространстве под углом 109°29 ’ друг к другу и ориентированы к вершинам правильного тетраэдра (рис. 2.8).

Рис. 2.8. Образование молекулы метана СН 4
Если гибридные орбитали углерода перекрываются с шарообразными s -орбиталями атома водорода, то образуется простейшее органическое соединение метан СН 4 − предельный углеводород.
Большой интерес представляет изучение связей атомов углерода между собой и с атомами других элементов. Рассмотрим строение молекул этана, этилена и ацетилена.
Углы между всеми связями в молекуле этана почти точно равны между собой (рис. 2.9) и не отличаются от углов С − Н в молекуле метана.
Следовательно, атомы углерода находятся в состоянии sp 3 -гибридизации.

Рис. 2.9. Молекула этана С 2 Н 6
Гибридизация электронных орбиталей атомов углерода может быть и неполной, т.е. в ней могут участвовать две (sp 2 -гибридизация) или одна (sp -гибридизация) из трех р -орбиталей. В этом случае между атомами углерода образуются кратныесвязи (двойная или тройная). Углеводороды с кратными связями называются непредельными или ненасыщенными. Двойная связь (С=С) образуется при sp 2 -гибридизации.
В этом случае у каждого из атомов углерода одна из трех р -орбиталей не участвует в гибридизации, в результате образуются три sp 2 -гибридные орбитали, расположенные в одной плоскости под углом 120° друг к другу, а негибридная 2р -орбиталь располагается перпендикулярно этой плоскости. Два атома углерода соединяются между собой, образуя одну s-связь за счет перекрывания гибридных орбиталей и одну p-связь за счет перекрывания р -орбиталей.
Взаимодействие свободных гибридных орбиталей углерода с 1s -орбиталями атомов водорода приводит к образованию молекулы этилена С 2 Н 4 (рис. 2.10) – простейшего представителя непредельных углеводородов.

Рис. 2.10. Образование молекулы этилена С 2 Н 4
Перекрывание электронных орбиталей в случае p-связи меньше и зоны с повышенной электронной плотностью лежат дальше от ядер атомов, поэтому эта связь менее прочная, чем s-связь.
Тройная связь образуется за счет одной s-связи и двух p-связей. Электронные орбитали при этом находятся в состоянии sp-гибридизации, образование которой происходит за счет одной s - и одной р -орбиталей (рис. 2.11).
Две гибридные орбитали располагаются под углом 180° относительно друг друга, а оставшиеся негибридные две р -орбитали располагаются в двух взаимно перпендикулярных плоскостях. Образование тройной связи имеет место в молекуле ацетилена С 2 Н 2 (см. рис. 2.11).

Рис. 2.11. Образование молекулы ацетилена С 2 Н 2
Особый вид связи возникает при образовании молекулы бензола (С 6 Н 6) – простейшего представителя ароматических углеводородов.
Бензол содержит шесть атомов углерода, связанных между собой в цикл (бензольное кольцо), при этом каждый атом углерода находится в состоянии sp 2 -гибридизации (рис. 2.12).

Рис. 2.12. sp 2 – орбитали молекулы бензола С 6 Н 6
Все атомы углерода, входящие в молекулу бензола расположены в одной плоскости. У каждого атома углерода в состоянии sp 2 -гибридизации имеется еще одна негибридная р-орбиталь с неспаренным электроном, которая образует p-связь (рис. 2.13).
Ось такой р -орбитали расположена перпендикулярно плоскости молекулы бензола.
Все шесть негибридных р -орбиталей образуют общую связывающую молекулярную p-орбиталь, а все шесть электронов объединяются в p-электронный секстет.
Граничная поверхность такой орбитали расположена над и под плоскостью углеродного s-скелета. В результате кругового перекрывания возникает единая делокализованная p-система, охватывающая все углеродные атомы цикла (рис. 2.13).
Бензол схематически изображают в виде шестиугольника с кольцом внутри, которое указывает на то, что имеет место делокализация электронов и соответствующих связей.

Рис. 2.13. -связи в молекуле бензола С 6 Н 6
Ионная химическая связь
Ионная связь − химическая связь, образованная в результате взаимного электростатического притяжения противоположно заряженных ионов, при котором устойчивое состояние достигается путем полного перехода общей электронной плотности к атому более электроотрицательного элемента.
Чисто ионная связь есть предельный случай ковалентной связи.
На практике полный переход электронов от одного атома к другому атому по связи не реализуется, поскольку каждый элемент имеет большую или меньшую (но не нулевую) ЭО, и любая химическая связь будет в некоторой степени ковалентной.
Такая связь возникает в случае большой разности ЭО атомов, например, между катионами s -металлов первой и второй групп периодической системы и анионами неметаллов VIА и VIIА групп (LiF, NaCl, CsF и др.).
В отличие от ковалентной связи, ионная связь не обладает направленностью . Это объясняется тем, что электрическое поле иона обладает сферической симметрией, т.е. убывает с расстоянием по одному и тому же закону в любом направлении. Поэтому взаимодействие между ионами независимо от направления.
Взаимодействие двух ионов противоположного знака не может привести к полной взаимной компенсации их силовых полей. В силу этого у них сохраняется способность притягивать ионы противоположного знака и по другим направлениям. Следовательно, в отличие от ковалентной связи, ионная связь характеризуется также ненасыщаемостью .
Отсутствие у ионной связи направленности и насыщаемости обуславливает склонность ионных молекул к ассоциации. Все ионные соединения в твердом состоянии имеют ионную кристаллическую решетку, в которой каждый ион окружен несколькими ионами противоположного знака. При этом все связи данного иона с соседними ионами равноценны.
Металлическая связь
Металлы характеризуются рядом особых свойств: электро- и теплопроводностью, характерным металлическим блеском, ковкостью, высокой пластичностью, большой прочностью. Эти специфические свойства металлов можно объяснить особым типом химической связи, получившей название металлической .
Металлическая связь – результат перекрывания делокализованных орбиталей атомов, сближающихся между собой в кристаллической решетке металла.
У большинства металлов на внешнем электронном уровне имеется значительное число вакантных орбиталей и малое число электронов.
Поэтому энергетически более выгодно, чтобы электроны не были локализованы, а принадлежали всему атому металла. В узлах решетки металла находятся положительно заряженные ионы, которые погружены в электронный «газ», распределенный по всему металлу:
Me ↔ Me n + + n .
Между положительно заряженными ионами металла (Me n +) и нелокализованными электронами (n ) существует электростатическое взаимодействие, обеспечивающее устойчивость вещества. Энергия этого взаимодействия является промежуточной между энергиями ковалентных и молекулярных кристаллов. Поэтому элементы с чисто металлической связью (s -, и p -элементы) характеризуются относительно высокими температурами плавления и твердостью.
Наличие электронов, которые свободно могут перемещаться по объему кристалла, и обеспечивают специфические свойства ме-
Водородная связь
Водородная связь – особый тип межмолекулярного взаимодействия. Атомы водорода, которые ковалентно связаны с атомом элемента, имеющего высокое значение электроотрицательности (чаще всего F, O, N, а также Cl, S и C), несут на себе относительно высокий эффективный заряд. Вследствие этого такие атомы водорода могут электростатически взаимодействовать с атомами указанных элементов.
Так, атом Н d + одной молекулы воды ориентируется и соответственно взаимодействует (что показано тремя точками) с атомом О d - другой молекулы воды:

Связи, образуемые атомом Н, находящимся между двумя атомами электроотрицательных элементов, называются водородными:
d- d+ d-
А − Н ××× В
Энергия водородной связи значительно меньше энергии обычной ковалентной связи (150–400 кДж/моль), однако этой энергии достаточно, чтобы вызвать агрегацию молекул соответствующих соединений в жидком состоянии, например, в жидком фтороводороде НF (рис. 2.14). Для соединений фтора она достигает порядка 40 кДж/моль.

Рис. 2.14. Агрегация молекул НF за счет водородных связей
Длина водородной связи также меньше длины ковалентной связи. Так, в полимере (HF) n длина связи F−H=0,092 нм, а связи F∙∙∙H= 0,14 нм. У воды длина связи O−H=0,096 нм, а связи O∙∙∙H=0,177нм.
Образование межмолекулярных водородных связей приводит к существенному изменению свойств веществ: повышению вязкости, диэлектрической постоянной, температур кипения и плавления.
Похожая информация.