브로마이드 부틸 얻기.
I.G. Bolesov, G.S. Zaitseva
친핵성 치환 및 제거.
체계적인 개발
컨트롤 N4
1. 다음 각 치환 반응에 대한 방정식을 작성하십시오.
2. 다음 생성물의 합성에 필요한 할로알칸 및 친핵성 시약을 쓰십시오.

3. 반응물과 생성물의 입체화학을 명확하게 나타내는 공식을 사용하여 아래의 각 방정식을 그립니다.
3.1(S)-2-브로모부탄 + MeONa(메탄올 중) 2-메톡시부탄(SN2),
3.2(R)-3-브로모-3-메틸헥산 + 메탄올 3-메톡시-3-메틸헥산(SN1),
3.3시스 2-브로모-1-메틸시클로펜탄 + NaSH 2-메틸시클로펜탄티올.
4. 1-브로모-2-메틸프로판, 브로마이드에 대한 반응성 차수 결정 터트-부틸, 2-브로모부탄과 반응:
4.1. 디메틸포름아미드 중 NaN3,
4.2. 10% 수성 다이옥산.
5. (R)-2-요오도옥탄의 아세톤 용액이 요오드화나트륨으로 처리될 때 광학 활성의 점진적인 손실을 설명하십시오.
6. (CH 3) 3 C-X(X = Cl, Br, I)의 가수분해 동안 거의 같은 양의 부틸렌(20%)과 tert-부틸 알코올(80%)이 형성되는 것을 설명하십시오.
7. 아래의 반응에서 기대할 수 있는 모든 생성물을 적으십시오. 형성 메커니즘의 계획을 제안하십시오.
7.1. 1-클로로-1-메틸시클로헥산 + 에탄올
7.2. 1-클로로-1-메틸시클로헥산 + 나트륨 에톡시드(에탄올 중)
8. 다음 변환을 두 단계로 수행합니다.
8.1. 부텐-2 메틸- 둘째- 부틸 에테르,
8.2. 2-메틸부텐-2 2-메톡시-2-메틸부탄,
8.3. 스티렌 1-페닐-1-시아노에탄.
9. 상응하는 알켄에 기초하여 (2단계로) 합성을 수행한다:
9.1. 1-페닐-1-아미노에탄,
9.2. (CH 3 CH 2) 2 CHSH.
10. 공액 디엔에 대한 1,4-친전자성 첨가 반응 및 친핵성 치환 반응을 사용하여 다음 변환을 수행합니다(2단계로).
10.1. 1,3-부타디엔 CH 3 CH \u003d CHCH 2 C N,
10.2. 1,3-부타디엔 N CCH 2 CH=CHCH 2 C N
11. 가장 선호되는 합성 방법을 제시하십시오.
11.1. N- 디부틸 에테르,
11.2. 에톡시벤젠(페네톨),
11.3. 에틸- 터트-부틸 에테르(공업적 방법).
11.4. 메틸벤질 에테르.
12. Williamson 합성법을 사용하여 디페닐 에테르를 얻을 수 없는 이유를 설명하십시오. 이 에테르는 어떻게 받습니까?
13. 알칸과 달리 에테르는 차가운 농축 황산에 용해됩니다. 이 반응은 이러한 종류의 화합물 간의 차이를 감지하기 위한 간단한 화학적 테스트입니다. 이 차이의 기초가 되는 화학은 무엇입니까(방정식 작성).
14. 아래의 각 반응에 대한 방정식을 쓰십시오. 반응이 진행되지 않는 경우를 참고하십시오.
14.1. 디 N-부틸 에테르 + 끓는 수성 NaOH
14.2. 메틸- N-프로필 에테르 + 과량의 뜨거운 HBr
14.3. 디 N-프로필 에테르 + Na
14.5. 디에틸 에테르 + 저온 농축 H 2 SO 4
14.6. 에틸페닐 에테르 + BBr 3 (1. 가열, 2. H 2 O).
15. 과량의 HBr로 가열하면 고리형 에테르가 1,4-디브로모부탄을 생성합니다. 에테르의 구조와 반응식을 쓰시오.
16. n-부틸알코올에서 1,2-부탄디올을 얻는다. 반응 메커니즘의 조건과 계획을 작성하십시오.
17. 에틸렌 옥사이드에 대한 반응식을 다음과 같이 쓰십시오.
17.1. 1 HBr 상당,
17.2. 과량의 HBr과 함께,
17.3. 페놀 및 추가로 묽은 산으로.
18. 장미 기름 냄새가 나는 2-페닐에탄올은 향수에 사용됩니다. 이 물질이 브로모벤젠으로부터 어떻게 합성될 수 있는지 쓰십시오.
19. 1,1-디메틸옥시란을 과량의 메탄올에 용해시키고 반응 혼합물을 소량의 산으로 처리하면 2-메톡시-2-메틸프로판올-1이 형성된다. 이 결과를 설명하는 메커니즘의 다이어그램을 제공하십시오. 이 반응에서 1-메톡시-2-메틸프로판올-2가 얻어지지 않는 이유를 설명하십시오.
20. 에틸렌 옥사이드 합성을 위한 최초의 산업적 방법은 에틸렌을 차아염소산으로 처리한 후 생성물을 묽은 염기와 반응시키는 것에 기반을 두었다. 이러한 반응에 대한 방정식을 작성하고 메커니즘 다이어그램을 설명하십시오.
21. 수신 메커니즘 계획의 조건을 작성하십시오.
21.1. 에틸렌 옥사이드와 메틸 알코올의 2-메톡시에탄올,
21.2. 에틸렌 옥사이드와 에틸렌 글리콜의 디에틸렌 글리콜.
22. 다음 각 쌍의 화합물을 구별하기 위해 사용해야 하는 화학적 테스트는 무엇입니까? 각 반응 테스트 동안 시각적으로 관찰할 수 있는 것을 표시하십시오.
22.1. 디 N- 프로필 에테르 및 N-헥산
22.2. 에틸 페닐 에테르 및 알릴 페닐 에테르,
22.3. 2-부탄올 및 메틸- N- 프로필 에테르,
22.4. 페놀과 아니솔,
22.5. 페놀 및 1-헥산올.
23. 과량의 HBr로 처리했을 때 단일 유기 화합물인 1,2-디브로모에탄이 얻어진다면 화합물 C 4 H 10 O 3 의 구조는 무엇입니까?
24. 에틸렌 글리콜과 묽은 황산의 혼합물을 천천히 가열하면서 동시에 반응 생성물을 증류하여 얻은 유분 화합물의 구조를 쓰십시오. 이 반응의 메커니즘을 설명하는 일련의 방정식을 제공하십시오.
25. 시클로헥산올과 페놀의 반응을 다음과 비교하십시오.
25.1. hbr,
25.2. H 2 SO 4 (가열),
25.3. PCl 3
화학식 R-OH, 원자에 부착된 OH 작용기
sp3 혼성화의 탄소
여기서 R은 알킬 또는 치환된 알킬기이다.
OH기 수에 따른 분류
단원자
메탄올
이원자
에틸렌 글리콜
삼원자
글리세린
1탄소 원자의 종류에 따른 분류,
OH기가 붙어있는
주요한
중고등 학년
제삼기
에탄올
이소프로판올
tert-부탄올
2
탄화수소 라디칼의 구조에 따른 분류: 포화, 불포화 및 방향족 알코올.
CH3H3C
CH2 C
가득한
2-메틸-2-부탄올
오
CH3
CH3
H2C
채널
씨
오
CH3
CH3
씨
오
불포화
2-메틸-2-부텐-2-올
향긋한
2-페닐-2-프로판올
CH3
3명명법
IUPAC 명명법에 따르면 포화 알코올은
알칸올. 이름에는 접미사 "OL"이 포함됩니다.
5
H3C
브르
4
와 함께
3
채널
채널3 채널2
2
채널
1
CH3
5
CH3
4
채널
그
3
채널
2
채널
1
CH3
그
CH3
4-브로모-4-메틸-3-에틸-2-펜탄올
3-펜텐-2-올
급진적 기능 명명법에 따르면
알코올의 이름은 라디칼의 이름과 단어로 구성됩니다.
술.
CH3OH
메틸
술
CH3CHCH3
그
이소프로필
술
CH2OH
벤질
술
그
시클로헥실
술
4얻는 방법
알켄의 수화
H2C
채널 채널3
+호
H+
2
H3C
채널
CH3
오
AdE 메커니즘,
마르코프니코바
재배열 가능
할로알칸의 가수분해
브르
H3C
채널 채널3
NaOH, H2O, T
-NaBr
오
H3C
채널 채널3
메커니즘 SN1, SN2
SN1이면 가능
재배열.
경쟁 반응:
분리(E1,E2)
5옥시머큐레이션-디머큐레이션(AdE)
규칙에 따른 지역별 알코올 생산
마르코프니코프. 공액 연결. 없어진
재배열
1) Hg(OAc)2; THF-H2O; 20OC
CH3
2) NaBH4; H2O
H3C C CH CH3
H3C C CH CH2
CH3
+
H3COH
3,3-디메틸-2-부탄올
(97%)
CH3
1) Hg(OAc)2; THF-H2O; 20OC
2) NaBH4; H2O
H3C 채널2 채널 채널2
H3C 채널2 채널 채널3
3
1-헥센
3
오
2-헥산올
(99,5%)
CH3
H3C C CH2 CH2 OH
CH3
3,3-디메틸-1-부탄올
+
H3C CH2 CH2 CH2 OH
3
1-헥산올
(0,5%)
6반응 메커니즘
R HC CH2 +
+
HgOAc
RHC
H2O
+
CH2
오
+
R CH CH2 Hg OAc + H
HG
OAC
주기적
수은 이온
NaBH4
R CH CH2 HgH
오
R CH CH3 + Hg
오
하이드록시알킬수소화수소
공액 연결. 외부 친핵체의 역할은 다음과 같이 수행됩니다.
용매는 물이다.
7그리냐르 시약으로 합성
알데히드 및 케톤과의 반응. 광고
(H)R1
+
와 함께
(H)R2
영형
R3
(abs. ef.) (H) R1
+
MgBr
(H)R2
H2O, HCl
와 함께
영형
R3
MgBr
-MgBrCl
(H)R1
(H)R2
와 함께
오
R3
포름알데히드→1차 알코올
알데히드→2차 알코올
케톤 → 3차 알코올
복근
시간
H2O, HCl
에테르
CH3CH2CH2OMgBr
CO+CH3CH2MgBr
CH3CH2CH2OH
시간
프로폭시마그네슘1-프로판올
진부한 생각
복근
CH3
CH3
H3C
에테르
H2O, HCl
CO+CH3CH2MgBr
H3C H2C HC OMgBr
H3C H2C HC OH MgClBr
시간
2-부톡시마그네슘2-부탄올
진부한 생각
복근
CH3
CH3
H3C
H2O, HCl
에테르
CO+CH3CH2MgBr
H3C H2C C OMgBr
H3C H2C C OH
H3C
CH3
CH3
2-메틸-2-부톡시마그네슘2-메틸-2-부탄올
진부한 생각
8산화에틸렌과의 반응
CH2
영형
+
CH2
(절대 ef.)
CH2
CH2
R1
R1
H2C 채널2
영형
+
MgBr
H2O, HCl
영형
-MgBrCl
R1
CH2CH2OH
MgBr
알코올 분자는 탄소 원자가 2개 더 큽니다.
Mg 유기 화합물보다.
(절대 ef.)
MgBr
시간
씨
시간
씨
+ 3 2
에틸마그네슘 브로마이드
H2O, HCl
H3C CH2 CH2 CH2 O MgBr
-MgBrCl
부톡시마그네슘 브로마이드
H3C CH2 CH2 CH2 OH
1-부탄올
9에스테르와의 반응
영형
C6H5
+
와 함께
C6H5
OS2H5
에틸 벤조에이트
(절대 ef.)
C6H5
+
(절대 ef.)
MgBr
C6H5
- С2Н5OMgBr
영형
+
와 함께
C6H5
+
MgBr
C6H5
영형
MgBr
와 함께
C6H5
C6H5
그
H2O, NH4Cl
-MgBrCl,
-NH4OH
C6H5
와 함께
C6H5
C6H5
트리페닐메탄올
설탕의 발효
효소
C6H12O6
2 C2H5OH + 2 CO2
10알켄의 붕소화수소산화
1) BH3
2) H2O2,NaOH-H2O
오
CH3CH2CHCH2OH
CH3CH2C CH2
+
CH3CH2C CH3
CH3(99%)
CH3
(1%) CH3
반응 메커니즘
채널3 채널 채널2
채널
CH3
에이비에이치
시간
CH2
채널3 채널2 채널2
채널3 채널 채널2
BH3
에이비에이치
시간
시간
채널3 채널 채널2
시간
채널3 채널2 채널2 B
3
2 채널3 채널 채널2
채널3 채널 채널2
비
시간
시간
시간
시간
시간
채널3 채널2 채널2 B
BH2
H2O2, 오하이오
비
채널2 채널2 채널3
채널2 채널2 채널3
트리프로필붕소
3 CH3 CH2 CH2 OH
+ B(OH)3
11반응 메커니즘
원자의 q-전하
q = - 0.2260
q = - 0.1619
CH3
CH3
채널 채널2
H BH2
전기 음성도
수소 2.1 > 붕소 1.9
입체 인자
CH3
CH3
CH2
시간
BH2
CH3
채널
시간
CH2
시간
PS1
BH2
채널
+
CH2
H2B
붕소 > 수소
+
채널
+
채널
긍정의 현지화
2차 원자의 전하
탄소(PS1)가 더 수익성이 있고,
기본(PS2)보다
CH2
BH2
시간
CH3
PS2
채널
CH2
시간
BH2
12카르보닐 화합물의 회수
알데히드→1차 알코올
케톤→2차 알코올
알데히드 및 케톤 회수
영형
H2, Ni
채널3 채널 채널 C
CH3 CH2 CH2 OH + C4H10
2
시간
카르보닐기의 선택적 환원
시간
영형
채널3 채널 채널 C
+
+
시간
알
시간
리
시간
영형
채널3 채널 채널2 오
시간
알
영형
채널2 채널 채널3
영형
채널2 채널 채널3
+
리
10% H2SO4
채널2 채널 채널3
3+
4 CH3 CH CH2 OH + Al + Li
+
13알데히드 및 케톤 회수
영형
CH2 CH CH2CH2C
시간
NaBH4
C2H5OH
CH2CH CH2CH2CH2OH
4-n 텐 -1-o l
4-p 엔 텐 알
영형
(85%)
1) LiAlH4, ýô ðr, 0-10 Α
오
2) H2O, H+, 0OC
(94%)
2-시클로헥센 -1-o l
2-시클로헥산 -1-on
LiAlH4 환원 메커니즘
R1
CO
+
+ LiAlH4
R2
R1
+
H C O 알리
R2
4
R1
+
H C O AlH3 리
R2
H2O
R1
4H COH
R2
+ Al(OH)3 + LiOH
14영형
1) NaBH4, C2H5OH
2) H2O, H+
오
오
+
시간
cyclohex-2-en-1-one
(59%)
디발-엔,
벤젠, 10 OS
영형
tricyclodec-4-en-3-one
시간
(41%)
(90%)
오
트리시클로덱-4-엔-3-올
CH3
CH3
채널3 채널 채널2
채널2 채널 채널3
알에이치
디발-엔
15카르복실산 회수
영형
CH3
CH2
씨
1) LiAlH4
2) 10% H2SO4
14
팔미트
산
CH3
CH2
14
CH2
오
오
1-헥사데칸올
1차 알코올로의 에스테르 회수. 부보-블랑 반응
Na+C2H5OH
영형
채널3 채널2
씨
14
영형
CH3
1) LiAlH4
2) 10% H2SO4
채널3 채널2
CH2OH
14
+CH3OH
메틸팔메이트
일산화탄소 회수. 산업적 방법
CO + 2H2
Cu-ZnO-Cr2O3, T
CH3OH
16물리적 특성
알코올과 탄화수소의 물리적 특성 비교
술
탄화수소
분자 Tm. OS
대량의
Tbp. OS
용해도
물 100ml, ml
CH3OH
채널3 채널3
32
30
-98,0
-172,0
65,0
-89,0
제한 없는
4,7
CH3CH2OH
CH3CH2CH3
45
44
-117,3
-189,9
78,5
-42,2
제한 없는
6,5
CH3CH2CH2OH
CH3CH2CH2CH3
60
58
-127,0
-135,0
97,2
-0,6
제한 없는
15,0
17알코올 분자의 구조
시간
공격
친핵체
친핵성
염기도
+
씨
....
영형
신맛
H+
시간
시간
OH기 치환
친핵체(SN)
OH기(E)의 분해
ECO=82kcal/mol
EOH=111kcal/mol
COH=107-109O
18수소 결합
E=3-6kcal/mol
19화학적 특성
1. 알코올의 산도
CH2
CH3
CH2
오
CH2
CH3
오
CH3
+ 나
영형
CH2
CH3
+
오나
시간
+
+ 1/2 H2
나트륨 에톡사이드
나에틸레이트
CH2
CH3
오나
+
H2O
더 강하게
산보다
에탄올
CH2
CH3
OH+NaOH
덜 강하다
산보다
물
20수용액에서 알코올의 산도
노
아르 자형
영형
+
시간
+
pKa
tert-부탄올
18,0
에탄올
15,9
메탄올
15,5
물
15,7
FCH2CH2OH
13,9
CF3CH2OH
12,4
(CF3)3COH
5,0
카
pKa=-lgKa
+I-효과
알킬기
-M 효과 F
212. 알코올의 염기도
알코올의 염기성 - 양성자를 부착하는 능력
....
시간
R O H + H
..
+
+
R O H
...
시간
누
+
R+
오
물이 좋다
이탈 그룹
알코올의 친핵성은 다음을 형성하는 능력입니다.
고독한 전자쌍을 통해 다른 원자와 결합한다.
....
....
로나
+
강한
친핵체
R O H + H
시간
+
약한
친핵체
..
+
R O H
알킬하이드록소늄 이온
강한
친전자체
시간
+
R+
...
오
물이 좋다
이탈 그룹
22기본 알코올.
그들은 Bronsted 및 Lewis 산과 염을 형성합니다.
시간
CH3OH + HBr
+
CH3 오
HBr
메틸히드록소늄
진부한 생각
시간
CH3OH + AlCl3
+
CH3 오
AlCl3
산-염기 특성에 대한 알코올 구조의 영향
CH3
CH3OH
CH3CH2OH
염기도 증가
산도 증가
CH3CH2OH
CH3
CH3 C
오
CH3
+I-알킬기의 효과
233. 알코올-친핵제
에테르 얻기
CH3CH2OH + HOCH2CH3
시간
SN2ac 반응의 메커니즘
시간
CH3CH2O:
CH3
씨
시간
친핵체
+
CH3CH2O
시간
시간
시간
시간
+
CH3CH2
영형
CH2CH3 + H2O
디 에틸 에테르
경쟁 반응 E
반응은 가역적이다
CH3
+
OH2
시간
기질
CH3
씨
+
+
CH3CH2OH2
+
CH3CH2OH +
1차 알코올.
분자간 탈수
H2O
"
CH3CH2O
씨
"
OH2
-H2O
시간
시간
시간
전이 상태
CH3CH2O
CH2CH3
+
+
H3O
24에테르를 얻습니다. A. 윌리엄슨의 합성.
대칭 및 비대칭 에테르
SN2
+
С2Н5О Na + CH3I
C2H5OCH3+
메틸에틸
강한
에테르
친핵체
나이
경쟁 반응
E2
시간
CH3O
+
나
강한
베이스
강한
친핵체
CH2
CH I
CH3
CH3 CH = CH2 + CH3OH
SN2
CH3CH
OCH3 + NaI
CH3
경쟁 반응 없음
CH3
CH O
+
CH 나
3
나
+
CH3
SN2
CH3CH
OCH3 + NaI
CH3
강한
친핵체
강한
베이스
25에테르를 얻습니다. 알코올과 알켄의 반응.
CH3
H3C
씨
CH3
+
+
CH2HO
시간
-H2O
CH3
H3C
씨
영형
CH3
CH3
고옥탄가 첨가제
SN1ac 반응 메커니즘
H3C
씨
CH3
H3C
씨
....
CH3
CH3
+H
CH2
+
H3C
씨
+
시간
CH3
+
영형
CH3
CH3
+
호
CH3
친핵체
CH3
H3C
씨
영형
CH3
+H
+
CH3
26에스테르 얻기. 에스테르화 반응.
CH3 C
영형
엑스
X=
+
시간
클
영형
OC
CH3
오
..
영형
..
시간
영형
+
CH3
CH3 C
메탄올 친핵체
+
HX
영형
CH3
메틸 아세테이트
카르복실산 염화물
카르복실산의 무수물
카르복실산
광학 활성 알코올은 키랄 원자에서 결합을 끊지 않고 반응합니다.
따라서 제품은 원래 알코올의 구성을 갖습니다.
CH3 C
영형
+
시간
오
..
영형
..
CH3
*
채널
시간
영형
+
채널2 채널3
(S)-2-부탄올
친핵체
CH3 + H2O
CH3 C
영형
*
채널
채널2 채널3
(S)-2-부틸 아세테이트
27무기산의 에스테르
영형
2CH3OH
+
H2SO4
H3C O SO CH3
+
2H2O
영형
영형
2CH3OH
+
ClSO2OH
H3C O SO CH3
Õëî ðñóëüô î í î âàÿ
êèñëî òà
영형
+
H2O
+ 염산
Äèì åòèëñóëüô àòàëêèëèðóþ ù èé àãåí ò
영형
CH3OH
+
ClSO2OH
Õëî ðñóëüô î í î âàÿ
êèñëî òà
CH3OH
+ HNO3
H3C OS OH
+
H2O
+ 염산
영형
메틸설페이트
H3C O NO2 + H2O
Ì åòèëí èòðàòâçðû â÷àòî å
âåù åñòâî
284. OH기의 친핵성 치환
알코올의 할로겐 유도체로의 전환
시약:
할로겐화수소(HCl, HBr, Na(K)Br+H2SO4, Na(K)I+H2SO4)
염화인, 브롬화물(PCl3 PBr3)
염화티오닐(SOCl2)
인과 요오드의 혼합물
옥시염화인(POCl3)
CH3CH2CH2CH2OH
CH3CH2CH CH3
오
CH3
CH3 COH
2시간
NaBr+H2SO4, 60OC
HCl, H2O, 20OC
CH3
CH3
오
48% HBr+H2SO4, 120OC
10 분
HCl(가스), 0OC
에테르
CH3CH2CH2CH2 Br + H2O
(95%)
CH3CH2CHCH3 + NaHSO4+ H2O
(60%)브르
CH3
CH3 C Cl + H2O
CH3
CH3
(90%) + H2O
클
29할로겐화수소의 작용하에 할로겐에 의한 OH기의 치환
씨
누
노
+
HX
SNac
오
수신
HI > HBr > HCl
+ H2O
X= Cl, Br, I
반응성이 감소합니다.
SN2ac 메커니즘. 1차 알코올.
시간
CH2. .
+
+ H
오
CH3
.
클
.
CH3
CH2
클
+ H2O
시간
시간
씨. + 천천히
+H
클
씨
영형
.
오
CH3
.
시간
허허허
시간
후방에서 공격
광학의 경우
활성 알코올 반전 구성
30SN1ac 메커니즘. 2차, 3차 알코올.
시간
C2H5
*CHOH
+
광학적으로
CH3
활동적인
술
느리게
-H2O
시간
+
+
C2H5 *CH2OH
CH3
시간
씨
클
+
C2H5*CH
C2H5
클
CH3
레이스메이트
CH3
탄수화물,
친핵체 공격
양쪽에
재편성
CH3
CH3CH CH CH3
시간
+
CH3C
시간
1,2-H-시프트
채널 채널3
+
CH3CH CH CH3
시간
오
CH3
CH3
+
영형
느리게
-H2O
루모 탄수화물
시간
CH3
CH3
+
+
H3C C CH2 CH3 Br
더 안정적인
3차 탄수화물
H3C
씨
CH2CH3
브르
31할로겐화수소에 대한 알코올의 반응성
벤질, 알릴 > 3차 > 2차 > 1차 > 메탄올
SN1
탄수화물의 안정성이 증가하고 반응성이
능력이 증가하다
SN2
공간
공격의 장애물
뒤에서 감소
반동적인
능력
증가
32할로겐화인 PCl5, PCl3, PBr3, PI3,
염화티오닐 SOCl2.
CH3
브르
채널
PBr3
CH3
오
채널
CH3
채널
CH3
CH3
PCl5
+
P(OH)3
CH3
클
채널
채널
채널
CH3
SOCl2
CH3
CH3
3-메틸-2-부탄올
CH3
클
채널
CH3
+ POCl3 + HCl
채널
+
SO2
+ 염산
CH3
33광학 활성 알코올과 염화 티오닐의 반응.
벤젠, 에테르
H5C2
시간
H3C
오
R-2-부탄올
H5C2
클
시간
H3C
R-2-클로로부탄
SOCl2
보존
구성
H5C2
피리딘
클
시간
CH3
항소
구성
S-2-클로로부탄
34알코올과 염화 티오닐의 반응 메커니즘.
이유없는 반응. SNi 메커니즘.
(i-내부)
CH2
CH3
CH2
CH3
+
채널
-HCl
염화티오닐
오
시간
+
CH2 O
CH3
영형
클
에스
CH3
클
씨
채널
영형
2-펜틸클로로설파이트
2-펜탄올
H3C
CH3
SOCl2
CH3
시간
에스
영형
이온 쌍을 닫습니다.
정면에서 공격합니다.
-SO2
씨
클
CH2
CH3
보존
구성
35.
+
영형
영형
로에스
SN2
Cl 1,4-디옥산
영형
+
OR + Cl
+SO2
항소
구성
클
+
로오
+
후방 공격
영형
SN2
RC1
+
영형
영형
항소
구성
슬라이드 노트 보기
36염기가 있을 때의 반응. SN2 메커니즘.
C2H5
시간
씨
오
CH3
+
H5C2
N
SOCl2
HN
클
염화티오닐
R-2-부탄올
+
+
시간
CO
클
HN
에스
CH3
+
영형
후방에서 공격
영형
C2H5
클
씨
시간
+
+
+
에스
HN
영형
클
항소
염산
구성
피리딘
CH3
37알코올과 PCl3 및 PBr3의 반응.
CH3
PCl3
CH3
3
CH3
CH3
시간
채널
씨*
CH3
CH3
*
씨
채널
클
시간
+
CH3
채널
CH3
오
PBr3
시간
씨*
CH3
POH
2
CH3
CH3
3
씨*
채널
브르
+
P(OH)3
시간
CH3
구성 반전
38알코올과 PBr3의 반응 메커니즘.
H3C
3
H3C
씨
+
오
시간
C3H7-i
PBr3
씨
-3HBr
R-3-메틸-2-부탄올
CH3
브르
씨
시간
오피
C3H7-i
시간
C3H7-i
H3C
+
오피
H Br 3 Br
SN2
3
트리(1,3-디메틸프로필)포스파이트
시간
C3H7-i
3
CH3
씨
전이 상태
피
일관되게
후방에서 브라니온 공격 3회
CH3
시간
C3H7-i
CO
3Br
2
씨
시간
C3H7-i
+
P(OH)3
구성 반전
BrΘ 음이온은 ClΘ 음이온보다 더 활동적인 친핵체입니다.
395. OH기 제거
알켄 얻기. 분자내 탈수
H2SO4, T
CH3
채널
채널2 채널3
E1ac
오
2-부탄올
그
CH3
씨
H2SO4, T
CH2
CH3
E1ac
CH3
2-메틸-2-부탄올
(tert-펜틸알코올)
CH3 CH = CH2 CH3 + H2O
트랜스-2-부텐
(주요 제품)
CH3
C=CH
CH3 + H2O
CH3
2-메틸-2-부텐
자이체프의 법칙
401차 알코올.
CH2
CH3
오
CH2
96% H2SO4, 180OC
H3C
HC CH2
-H2O
E2ac 반응 메커니즘
..
..
1) CH3 CH2 OH + H
+
채널2 채널2
시간
..시간
..오
+
H2C
CH2 + H2O + H2SO4
OSO2OH
동기화: 물 분리
그리고 양성자
영형
2) RCH2CH2OH + H2SO4
영형
RCH2CH2
HSO4-
O2SO + H2O
영형
RCH CH2 + H2SO4 + HSO4R CH CH2 O S OH
170 - 190OC
영형
시간
412차, 3차 알코올.
E1ac 메커니즘. 재배열 가능
CH3
씨
CH3
CH3
CH3
CH3
H2SO4, 80 OS
채널
오
3-메틸-2-부탄올
CH3
CH3
채널
채널
CH3
+오
씨
+
채널
CH3
더 지속 가능한
3차 탄수화물 CH3
씨
CH3
+
1,2-CH3-시프트
CH3
시간
2
CH3
CH3
CH3
CH3
-H+
씨
CH3
채널
CH3
더 안정적이고 더
알킬화 알켄
자이체프의 법칙
할로알칸과의 분열 반응의 주요 생성물
두 개의 동등하지 않은 C 원자가 가장
안정한 (가장 알킬화된, 열역학적으로
안정) 알켄.
42알코올의 촉매 탈수 반응 방향
H3C
채널2 채널2
5
채널 채널3
오
300-400OC
ThO2
Al2O3
H3C
CH2CH
5
Zaitsev에 따르면
채널 채널3
H3C
채널2 채널2 채널
5
CH2
호프만에 따르면
43알코올 산화
1차 알코올은 알데히드로 산화된 다음 산으로 산화됩니다.
H3C
오[오]
CH2
영형
CH3 C
[영형]
시간
아세트알데히드
에탄올
영형
CH3 C
오
아세트산
2차 알코올은 케톤으로 산화
H3C
영형
[영형]
채널
오
H3C
이소프로판올
CH3 C
CH3
아세톤
3차 알코올은 골격이 파괴되면서 산화된다.
441차 알코올의 알데히드로의 산화의 예
산화제: 크롬(IV) 산화물과 피리딘의 착물(Sarett-Collins 시약)
.
영형
N
+
CH2
오
영형
4-니트로페닐메탄올
4-니트로벤질 알코올
CH2Cl2 ;
영형
영형
CrO3 2C5H5N
N
25OC
+
(97%)
씨
영형
시간
4-니트로벤즈알데히드
산화제: Saretta 시약(피리디늄 클로로크로메이트,
유기용매에 잘 녹는다)
H3C
CH2 C
4
씨
CH2OH
3-옥틴-1-올
.
.
CrO3 C5H5N HCl
CH2Cl2 ; 25
OC
영형
H3C
CH2 C
씨
4
2-옥티널
(84%)
씨
시간
산화제: 망간(IV) 산화물.
영형
CH2OH
채널3 채널2
씨
시간
씨
시간
Z-2-부텐-1-올
MnO2 20OC
CH2Cl2 또는 C6H14
씨
채널3 채널2
씨
시간
씨
시간
시간
Z-2-부테날
451차 알코올의 카르복실산으로의 산화의 예
Jones 시약(수용성 H2SO4에 있는 CrO3의 용액).
영형
CH2OH
씨
CrO3-H2O-H2SO4
아세톤, 20 OS
C6H5
(1-페닐시클로펜틸)메탄올
오
C6H5
1-페닐시클로펜탄산
2차 알코올이 케톤으로 산화되는 예
오
CrO3-H2O-H2SO4
영형
아세톤, 20 OS
시클로옥탄올
시클로옥타논
46산성 매질에서 골격의 파괴와 함께 3차 알코올의 산화
CH3
CH3 C
오
CH3
시간
+
-H2O
CH3 C
CH2
[영형]
채널3 C 채널3
+ CO2 + H2O
영형
CH3
알코올의 촉매 탈수소화
영형
Cu 또는 Ag, 600 OS
H3C
오
산업
프로세스.
반응 예
α 제거.
HC
-H2
메탄올
시간
포름알데히드
오
Cu, 600OC
영형
-H2
시클로헥사놀
시클로헥사논
47SEAr 아렌의 알킬화
..
CH.OH
. +BF
3
3
+
H3C
시간
영형
+
CH3(BF3OH)
bf3
CH3
+
CH3(BF3OH)
+
시든
+ H2O + BF3
알코올 종류의 대표자 :
메탄올 - 독, 용매, 합성 시약
에탄올 - 다량의 독, 용매, 합성 시약
이소프로판올 - 용매, 합성 시약
48알코올의 화학적 변형의 주요 방향
탈수
시든
친핵성
치환
술
탈수소화
산화
알켄, 에테르
알킬 방향족
사이
할로겐 유도체,
에테르,
에스테르,
알데히드, 케톤
알데히드, 케톤,
카르복실산
49디올(2가 알코올)
CH2
호
오
채널2 채널2
오, 오
H3C 채널 CH2
오, 오
메탄디올 - 자유 형태로 존재하지 않음
1,2-에탄디올(에틸렌 글리콜)
1,2-프로안디올(프로필렌 글리콜)
오
트랜스-1,2-시클로헥산디올
오
50얻는 방법
Mylas 시약, 과산화수소를 사용한 알켄의 수산화,
Wagner 반응에 따르면 Krieg 반응
오
H2O2, OsO4, 0OC
시간
오
(마일라스 시약)
시간
시스-1,2-시클로헥산디올
H2O2, CH3COOH, H2SO4
오
KMnO4, H2O, 20OC, pH=7
시간
(바그너 반응)
오
1) OsO4, 25OC
시간
2) NaHSO3/H2O
트랜스-1,2-시클로헥산디올
(크리게 반응)
51에틸렌으로부터 에틸렌 글리콜의 제조.
Ca(OH)2
Cl2, H2O
채널2 채널2
H2C
채널2 채널2
H2O, H+
CH2
채널2 채널2
ClOH
영형
오, 오
에틸렌클로로히드린 에틸렌옥사이드
H2O, NaOH
프로필렌에서 글리세린 얻기.
NaOH, H2O
Cl2, 400
채널2 채널 채널3
OC
채널2 채널 채널2
클
H2O2, H2O
채널2 채널 채널2
오
Cl2, H2O
NaOH, H2O
채널2 채널 채널2
오오오오
채널2 채널 채널2
ClOHCl
52케톤의 고전적 환원 이량체화
(피나콘 복원).
CH3 C
CH3
1) 마그네슘, 벤젠
2) H2O
CH3
CH3 C
CH3
CCH3
오, 오
(43-50%).
피나콘
2,3-디메틸-2,3-부탄디올
영형
결점:
낮은 출구,
반응에 들어가다
케톤만.
케톤의 현대적인 환원 이량체화
THF(I. Kori)에 TiCl4가 있을 때.
O Zn, TiCl4 THF, C6H5
25 OS, 2시간
씨
H3C
CH3
영형
n-C7H15C
시간
Mg(Hg), TiCl4, THF,
0 OS, 13시간
C6H5
씨
씨
오, 오
(91%)
CH3
장점: 높음
출력, 반응할 수 있음
케톤 뿐만 아니라
그러나 또한 향기로운
지방족 알데히드
n-C7H15 CH CH n-C7H15 (80%)
오, 오
8,9-헥사데칸올
53알돌 환원에 의한 1,3-디올의 제조.
영형
R1 채널 CH2 C
오
NaBH4, DME
R2
R1 채널 CH2 채널 R2
오
오
DME-디메톡시에탄
1,3-디올
화학적 특성
다가 알코올의 경우와 동일한 반응이 특징적입니다.
1가 알코올.
1,2-디올의 탈수.
1,2-디올을 1,3-디엔으로 탈수.
CH3
CH3
씨
CH3
씨
오, 오
CH3
Al2O3, 450-470OC
H2C
씨
씨
CH2
(70-85%)
채널3 채널3
54재배열이 있는 1,2-디올의 탈수
(1,2-디올의 피나콜린 재배열).
채널3 채널3
CH3 C
씨
CH3
H2SO4, TOC
CH3
CH3 C
오, 오
씨
CH3 + H2O
R. Fittig의 반응.
OCH3
피나콜린
피나콘
35% H2SO4, TOC
채널3 채널 채널3
CH3 C
오, 오
채널2 채널3
(81%)
영형
부타논
pinacol 재배열의 메커니즘.
R1
RC
R1
씨
시간
+
아르 자형
아르 자형
오, 오
R1
R1
씨
씨
아르 자형
아르 자형
아르 자형
씨
씨
+
+오
R1
아르 자형
시간
씨
+
씨
..오
오오오2
R1
R1
-H2O
아르 자형
R1
R1
+
아르 자형
씨
씨
영형
R1
아르 자형
55환형 에테르의 형성으로 탈수.
분자간 탈수
오
H2C
H2C
호
+
오
호
영형
CH2 H2SO4, 농축, 140 OC H2C
CH2
H2C
CH2
CH2
(50-55%)
영형
1,4-디옥산
분자내 고리탈수화
고리형 에테르의 형성과 함께.
호
CH2
5
오
1,5-펜탄디올
57% H2SO4
- H2O
영형
(100%)
테트라히드로피란
56
에테르의 분류 및 명명법
에테르에테르의 분류 및 명명법
구조별
탄화수소
라디칼
H3C
명명법
IUPAC
대칭,
디알킬
디에틸
에테르
2-에톡시에탄
비대칭,
디알킬
메틸에틸
에테르
메톡시에탄
비대칭,
알킬아릴
메틸페닐에테르
메톡시벤젠
대칭,
디아릴
디페닐
에테르
페녹시벤젠
테트라히드로푸란
테트라히드로푸란
영형
주기적,
알킬
푸란
영형
주기적,
향긋한
옥사시클로펜타디엔
영형
CH2
CH2
H3C
하찮은
명명법
CH3
CH2
CH3
영형
영형
CH3
영형
57얻는 방법
알코올의 분자간 탈수.
대칭 디알킬 에테르.
CH3CH2OH + HOCH2CH3
시간
+
CH3CH2
영형
CH2CH3 + H2O
디 에틸 에테르
윌리엄슨 반응.
대칭 및 비대칭 디알킬 및 알킬아릴 에테르
SN2
+
С2Н5О Na + CH3I
C2H5OCH3+
메틸에틸
강한
에테르
친핵체
나이
NO2
O2N
브르
NO2
+
H3C
확인
+
DMF
-KBr
O2N
OCH3
1-메톡시-2,4-디니트로벤젠
58크라운 에테르 얻기
오나
오나
+
영형
CH2
CH2
CH2
CH2
클
클
클
CH2
영형
+
클
CH2
CH2
영형
이나트륨
CH2
카테콜 소금
(이나트륨 1,2디-(2-클로로에틸)에테르
벤젠디올레이트)
오
C4H9OH-H2O
오나
100
오나
OC
+
영형
영형
디벤조-18-크라운-6
영형
KOH, H2O-THF
영형
오
(45%)
퍼스트 크라운 에어,
K. 페더슨 (1967)
영형
영형
영형
영형
클
영형
영형
영형
영형
영형
영형
(Ä.Êðàì)
영형
클
18-크라운-6
(40-60%)
알코올과 알켄의 반응.
CH3
H3C
씨
CH3
+
+
CH2HO
시간
CH3
-H2O
H3C
씨
영형
CH3
CH3
메틸 tert-부틸 에테르(MTBE).
고옥탄가 첨가제
59물리적 특성.
T pl., OS
티보일, OS
CH3OCH3
-138,5
-23,2
CH3CH2OH
-117,3
64,7
CH3CH2OCH2CH3
-116,3
34,6
CH3CH2CH2CH2OH
-89,5
117,7
에스테르 분자의 구조
.. ..
시간
약한 염기
약한 친핵체
0.142nm
시간
영형
씨
111오
씨
시간
1) 산소 원자에서의 반응
2) a-탄소 원자에서의 반응
3) C-O 결합 절단 반응
시간
시간
시간
60화학적 특성
산소 원자에서의 반응
아르 자형
R1
..
오.. + HX
아르 자형
X=Cl, HSO4 R1
..
오
.
행동 중 양성자
약산. 교육
수소 결합.
HX
강산과의 전하 이동 착물(CTC) 형성.
아르 자형
..
오.. + HX
R1
(C2H5)2O
X=Br,I
+BF3
+
아르 자형
오
.
엑스
브론스테드산
R1
디알킬옥손 양이온
+
(C2H5)2O
bf3
루이스산
삼불화에테르산염
붕소. 환승이 복잡한
차지(불펜)
61트리알킬옥소늄염의 형성.
C2H5
..
.. + 채널
영형
C2H5
아르 자형
아르 자형
2
5
에프
C2H5
+BF3
..
영형
+
C2H5 BF4
C2H5
트리플루오로보레이트
트리에틸옥소늄
.O+.
아르 자형
+ .. 누
누
bf4
bf4
C2H5
아르 자형
+
..
영형
+
아르 자형
..
..
아르 자형
+
C2H5 BF4
C2H5
노
강한
알킬화제.
반응
약한 친핵체.
영형
C2H5
ROC2H5
+
C2H5
..
.. +
영형
bf3
트리플루오로보레이트
트리에틸옥소늄
62α-탄소 원자에서의 반응
알콕시 라디칼 - 더
알킬보다 안정
짝을 이루지 않은 전자의 비편재화 때문입니다.
SR 메커니즘.
아르 자형
..
영형
..
시간
시간
씨
R1
+
시간
아르 자형
아르 자형
-인사
..
영형
..씨.
R1
라디칼 할로겐화
CH3
CH2
영형
CH2
CH3+
Cl2
시간, -20
클
OC
-HCl
채널
CH3
영형
CH2
CH3
1-클로로-1-에톡시에탄
63자가산화
아르 자형
.. 시간
영형
.. 씨
R1
시간
아르 자형
.. 시간
OC.
..
아르 자형
.. 시간
영형
.. 씨
R1
R1
오오
+R
-인사
+. 영형
오
+R
.. 시간
OC
..
시간
아르 자형
.. 시간
OC.
..
아르 자형
R1
R1
.. 시간
OC
..
R1
오오
아르 자형
.. 시간
OC
..
R1
오오
+R
.. 시간
OC
.
..
R1
과산화수소는 가열되거나 충격을 받으면 쉽게 폭발합니다.
64C-O 결합 절단 반응.
반응 조건:
1) 농축 HBr, HI; 120-150OC
2) BCl3, BI3; -20 OS
엑스
아르 자형
..
영형
+
SN2
아르 자형
엑스
+
R1
오
R1
시간
양성자 - SN1
에테르
+
R O R1 X
양성자화되지 않은 에테르
R1
+
+R
엑스
아르 자형
오
R1
엑스
엑스
+R
영형
R,R1-기본,
2차 알킬,
페닐.
SN2 메커니즘.
약한 기반.
알코올 좋은 떠나기
그룹
R-기본,
2차 알킬,
페닐.
R1-3차
알킬, 알릴,
벤질.
SN1 메커니즘.
알콕사이드
음이온
탄탄한 기초.
나쁜 떠나
그룹.
65....
SN2
+H
C6H5 O C2H5
에톡시벤젠
페네톨
..
H3C
브르
시간
시간
씨
..
+
+
C6H5 오
시간
CH3
브르
+
영형
씨
시간
시간
C2H5
..
O C6H5
시간
CH3
브르
시간
씨
시간
시간
+
호
C6H5
SN1
....
CH3
CH3 C
영형
CH3
+
시간
CH3
..
CH3 C
+
영형
CH3
H3CH H
느린 -CH3OH
MTBE
CH3
CH3 C
+
CH3
오
CH3
+
+ 채널3
CH3
CH3 C
+
CH3
+
브르
빠르게
CH3
CH3 C
브르
CH3
66에테르는 저온에서 Na와 반응하지 않습니다.
고온에서 에테르(특히 더 높은 동족체)
방정식에 따라 분할
아르 자형
영형
R1
+ 2나
로나
나트륨 알콕사이드
+
R1 나
알킬나트륨
활성 알킬 나트륨은 반응할 수 있습니다.
디에틸 에테르(P.P. Shorygin)
H5C2
영형
C2H5
+HC
5
2
나
H5C2 오나
나트륨 에톡사이드
+
C2H6
+
C2H4
에테르의 사용.
용제. 다양한 복합체의 합성. 녹 방지 첨가제
연료로.
67순환 에테르.
CH2
CH2
영형
산화 에틸렌,
옥시란
채널3 채널
CH2
영형
산화물
프로필렌, 2메틸옥시란
채널2 채널2
CH2 O
1,3-에폭시프로판,
옥세탄
채널2 채널2
CH2
CH2
영형
테트라히드로푸란,
테트라메틸렌 옥사이드
영형
CH2
CH2
CH2
영형
CH2
1,4-디옥산
68오시란(에폭사이드).
얻는 방법
에텐의 직접 산화.
H2C
CH2
+ O2
Ag
H2C 채널2
250-300 OC
산업 방식
에틸렌 옥사이드 얻기
알켄의 에폭시화(N.A. Prilezhaev의 반응).
아르 자형
채널 채널2
+
영형
아르 자형
씨
영형
에테르, 벤젠,
CH2Cl2
오
+
CH2Cl2
오오 0
시클로헥센
클
채널 채널2
+
아르 자형
씨
영형
옥시란
과산
(과산)
영형
아르 자형
영형
영형
OC
(80%)
오
영형
+
오
클
m-클로로퍼벤조산-7-옥사비시클로헵탄
(시클로헥센옥사이드,
나야산
시클로헥센옥사이드)
69할로히드린의 탈수소 할로겐화.
영형
H3C
HC CH2
+
NBr
NBS
영형
H2O, DMSO
오
H2C
브르
HC CH3
비..
H3C
HC CH2
영형
70분자의 구조
시간
0.150nm
시간
씨
시간
씨
영형
61O
시간
0.146nm
에너지
전압
105kJ/몰
(25kcal/mol)
H2C
CH2
..영형..
시간
공격
친핵체
+
71화학적 특성
친핵체와의 상호작용
약한 친핵체와의 반응. 산 촉매
+
H2C
H, H2O
CH2
영형
CH2 1,2-에탄디올
에틸렌 글리콜
오, 오
H2C
+
H3C HC
CH2
H, CH3OH
H3C HC
영형
CH2 O CH3
오
1-메톡시-2-프로판올
메틸셀로솔브
SN2 메커니즘
CH2+H
RHC
영형
+
RHC
..
CH2+H2O
시간
CH3
+오
시간
친핵체에 의한 공격
입체적으로 접근 가능
원자적 고려사항
아르 자형
+
CH2CH2O
오
CH3 -H+
아르 자형
CH2CH2O
CH3
오
72메커니즘 SN1
H3C
H3C
+
채널
씨
2
오
덜 안정적
1차 탄수화물
빠르게
H3C
씨
H3C
CH2
시간
영형
+
H3C
H3C
느리게
CH2
씨
H3C
+
영형
시간
시간
H3C
영형
씨
+
CH3
시간
+
H3C
+
씨
CH2
+
.
.
호
CH3
오
더 안정적인
3차 탄수화물
CH3
CH3
CH2OH
H3C
영형
씨
CH2OH
CH3
2-메틸-2-메톡시-1-프로판올
73강한 친핵체와의 반응. SN2 메커니즘.
C2H5ONa
C2H5OH
CH2 CH2 O C2H5
오
NaOH, H2O CH2CH
2
2
오, 오
H2C
CH2
NH3
영형
채널2 채널2
2-에톡시에탄올
모노에틸
에틸렌 글리콜 에테르
1,2-에탄디올
에틸렌 글리콜
2-아미노에탄올
OH NH2
NH2C2H5
CH2 CH2 NH C2H5
2-N-에틸에탄올아민
오
CH3MgI
CH2 CH2 CH3 + MgIOH
오
74SN2 메커니즘
..
..
CH3 CH CH2 + NaO CH3
나트륨 메톡사이드
영형
CH3 CH CH2 O CH3
오 나
CH3OH
+
CH3 CH CH2 O CH3 + CH3ONa
오
..
H3C
C 채널2 + H2N 채널3
H3C
영형
CH3
시간
+
H3C C CH2 N CH3
영형
시간
CH3
H3C C CH2 NH CH3
오
2-메틸-1-메틸아미노-2-프로판올
75중합
호
+
H2C
CH2
H2O CH2 CH2 O
영형
H2C
H2C
N
CH2
영형
CH2
영형
HO CH2 CH2 O CH2 CH2 O
H2O CH2 CH2 O
시간
n+2
폴리에틸렌 글리콜,
카보박스
애플리케이션
다양한 화합물 합성을 위한 초기 시약.
76페놀
오
오
오
호
오
오
페놀,
단원자
페놀
하이드로퀴논,
이원자
페놀
플루로글루시놀,
삼원자
페놀
77얻는 방법
방향족 할로겐 유도체의 가수분해
활성화되지 않은 치환-아린 메카니즘
클
오나
+ NaOH
오
염산
360oC, P
-NaCl
클로로벤젠
페놀
활성화된 치환, SNAr
클
오나
+ 2 NaOH
NO2
p-니트로클로로벤젠
오
160oC, P
염산
- 염화나트륨,
-H2O
-NaCl
NO2
NO2
p-니트로페놀
78이소프로필벤젠 하이드로퍼옥사이드로부터 페놀의 제조
시간
오오
H3C CH3
H3C 채널 CH3
O2
오
과산화수소
쿠멘
쿠몰
영형
Н2SO4, H2O
+
H3C CH3
페놀
아세톤
설포네이트기의 치환, 설포네이트의 알칼리 용융
SO2ONa
300OC
+
오
오나
NaOH
-Na2SO3
H2SO4, H2O
-NaHSO4
벤젠술포네이트
나트륨
79히드록실에 의한 디아조기의 치환
+
NH2
N2OSO3H
NaNO2 + 2H2SO4
H2O
+ N2 + H2SO4
5℃
아닐린
오
페닐디아조늄
황산수소염
80물리적 특성
이름
T pl.,
OS
끓이다.,
OS
용해도
물 100ml에
25 °C에서, g
가∙1010
페놀
43
182
9,3
1,1
p-크레졸
35,5
201
2,3
0,07
p-플루오로페놀
48
185
-
5,2
p-클로로페놀
43
220
2,7
6,3
p-브로모페놀
33
236
-
14
o-니트로페놀
45
217
600
m-니트로페놀
96
194
p-니트로페놀
114
279 차이
피로카테킨
104
246
0.2 휘발성
증기
1.35 비휘발성
증기
1.69 비휘발성
증기
46
레조르시놀
110
281
123
600
600
1
3
81수소 결합
시간
영형
N
영형
영형
N
영형
영형
영형
N
시간
영형
시간
영형
영형
관련 p-니트로페놀
시간
시간
영형
시간
영형
영형
시간
+
CO
아니요
영형
시간
시간
영형
영형
분자의 구조
..영형. 시간
.
.
+엠>-나
.
.
.
.
. .. ..
영형
sp2-® 리탈
시간
2pz-o 리탈
82화학적 특성
페놀의 산 특성
..
영형
RH
술
약하다
산
.. ....
오
.. .. ..
영형
.. .
+
로오
+ H
.. .
전하가 산소에 국한됨
더 강력한 기반
..
....
....
.
.영형
영형
영형
..
..
+H+
..
페놀
나
II
III
IV
더
강한
지역화되지 않은 요금
산
약한 기반
영형
염기도 증가
< ArO < HO < RO
RC
영형
영형
> ArO H >HO H > RO H 탈산성화
RC
오
83염 형성
+ H2O
+ NaOH
페놀, 물에 불용성
오
디
산성
속성
묽게 하다
페녹사이드
나트륨, 용해성
물 속
오
ㅏ
산성
속성
증가하다
오나
오
오나
오
+ NaHCO3
+ H2CO3
더 강하게
산
페놀에 대한 정성적 반응.
착색 복합체 형성
FeCl3와 화합물:
페놀 - 적자색
크레졸 - 블루
레조르시놀 - 짙은 보라색
살리실산 - 빨강
페놀의 상대적으로 높은 산도는 다음에 의해 결정됩니다.
1. 산소의 n전자와 방향족의 p전자의 p-p-컨쥬게이션
커널. 요금이 현지화되지 않았습니다.
2. 페놀의 О-Н 결합은 더 극성을 띠고 있습니다. O 원자는 C 원자에 결합되어 있습니다.
sp2 혼성화 상태.
84페녹사이드 이온 - 주변
친핵체
페녹사이드 이온의 O-알킬화.
CH3I
- 나이
오
+
NaOH
오나
CH3
SN2
H3C O SO2 O CH3
영형
메톡시벤젠
아니졸
+
- NaOSO2OCH3
페녹사이드 이온의 C-알킬화.
O CH2 CH CH2
SN
CH2 CH CH2 Br
아세톤
O-알킬화
+
오나
오나
SN
CH2 CH CH2 Br
CH2CH CH2
벤젠
C-알킬화
산소 차단
때문에 반응 센터
수소의 형성
페놀레이트 이온 사이의 결합
및 과잉 페놀.
85페녹사이드 이온(SN)의 O-아실화.
영형
H3C C
..
호
..
영형
H3C C
+
오
+
영형
..
호
..
영형
채널2 채널3
+
H3C C
H2O H2O=+1.5kcal/mol
H2O H2O=-4.6kcal/mol
ㅇ CH2 CH3
영형
H3C
NaOH
H2O
오
중립적
분자 약
친핵체
씨
클
H3C CO O CO CH3 , H+
영형
H3C
씨
영형
+
오 나
SO2Cl
음이온
친핵체
페닐아세테이트
SO2O
페닐벤젠술포네이트
86감자 튀김 재배치
영형
H3C
오
오
씨
영형
AlCl3, T
CH3
+
시든
영형
o-히드록시아세토페논
페닐 아세테이트
H3C
영형
p-하이드록시아세토페논
반응 방식
영형
OC(O)CH3
+
영형
씨
H3C
OC(O)CH3
+
CO
AlCl3
H3C
영형
C6H5OH
OC(O)CH3 + H2O
씨
CH3
87Claisen pergrouping
시그마트로픽 재배열의 예 - s-결합 변위
영형
CH2
채널
영형
CH2
CH2 190-220OC
=
오
영형
채널
채널2 채널 채널2
CH2
시간
알릴페닐에테르
알릴옥시벤젠
시클로헥사디에논
O CH2 CH CH CH3
220 OS
채널2 채널 채널2
2-알릴페놀
오
CH HC CH2
CH3
페닐-(1-부트-2-에닐)
에테르
1-(부트-2-에닐옥시)벤젠
2-(1-메틸알릴)페놀
88친전자성 치환 SEAr
오
오
오
이자형
+E+
+
+
o-이성질체
시간
+
이자형
p-이성질체
페녹사이드 음이온의 SEAr 반응
영형
영형
영형
이자형
+
E+
시간
+
이자형
시간
s-복합체
s-복합체는 중성 입자이며,
안정성이 높아졌습니다
89할로겐화, SEAr
고극성 용매 - 페놀의 해리
오
+
-H3O
+
영형
오
브르
H2O
+ 3Br2
페녹시다이온
브르
H2O
+ 3HBr
브르
2,4,6-트리브로모페놀
약한 극성 용매, 페놀은 해리되지 않습니다.
오
오
오
+ Cl2
클
OOC
+
CCl4
(74%)
o-클로로페놀
(26%)
Clp-클로로페놀
90페녹사이드 이온의 브롬화 메커니즘
영형
영형
시간
Br2.5OC
오
영형
브르
브르
브르
브르
-HBr
브르
...
H2O
브르
2,4,6-트리브로모페놀
강산 존재하에서 페놀의 할로겐화
오
오
+
br2,
HBr, 5OC
H2O
+
HBr
완전히 압도
페놀 해리
(81%)
브르
4-브로모페놀
91질화, SEAr
오
오
오
NO2
20% HNO3, 10OC
+
-H2O
+
o-이성질체가 분리됨
물로 증류하는 동안
나룻배.
NO2
입소화
오
제품
산화
오
SO3H
HNO3, 0OC
H2SO4, 100OC
SO3H
오
O2N
오
SO3H
HNO3,100OC O2N
NO2
입소 대체
SO3H
NO2
(70%)
92설폰화, SEAr
오
오
SO3H
20OC
+
오
H2SO4,
농축
키네틱
제어
SO3H(51%)
(49%)
오
오
SO3H
120OC
열역학적
제어
+
(4%)
SO3H(96%)
93Friedel-Crafts 알킬화, SEAr.
오
+
CH3
H2C
씨
CH3
KU-2
H3C
H3C
CH3
CH3
CCH3
CH3
오
씨
CH3
CH3
p-크레졸
2,3-디-tert-부틸-4-메틸페놀
이오놀
오
H3C
+
H3C
채널
CH3
HF, 0-8 OC H C
3
오
HC
CH3
채널
CH3
오
채널
CH3
CH3
2,4,6-트리이소프로필페놀
94Friedel-Crafts 아실화, SEAr
오
영형
+
H3C
씨
영형
AlCl3; 140OC
영형
AlCl3
CH3 감자 튀김 재배열
클
CH3
영형
영형
+호
호
CH3
1-(2-히드록시페닐)에타논
1-(4-히드록시페닐)에타논
오
+
CH3COOH BF3
20
OC
영형
씨
호
CH3
(95%)
95프탈산 무수물과 페놀의 축합, SEAr
Friedel-Crafts 아실화 반응의 변형(A. Bayer).
오
호
영형
오
씨
2
+
영형
H2SO4, 120OC
씨
영형
씨
씨
영형
영형
페놀프탈레인
프탈산
무수물
아조 콤비네이션 SEAr
+
N2Cl
염산
페닐디아조늄
(친전자체)
+
오 나
+
N
N
오
4-페닐아조페놀
96페놀의 포르밀화.
리마이어-티만 반응.
오
오
60
오
조
OC
클
+
+ CHCl3 + NaOH CH2Cl -H2O
3
CHCl3OH-
2
(20%)
o-히드록시벤즈알데히드
조
(10%)
+
+ .CCl2
H2O
+ .CCl3
디클로로카르벤 친전자체, 아님
요금이 있습니다.
탄소는
6개의 전자
다른 시약을 사용한 페놀의 포르밀화
오
오
+ HCN + HCl
AlCl3
4-옥시벤잘베하이드
벤젠, 40
OS
(30%)
조
오
영형
+
시간
씨
N
CH3
CH3
DMF
오
POCl3
DMF, 20
4-옥시벤잘베하이드
OS
(85%)
조
97알데히드 및 케톤과 페놀의 축합
오
오
+
시간
씨
오
CH2OH
O NaOH, H2O
2
4-하이드록시메틸페놀
+
시간
2-하이드록시메틸페놀
반응 메커니즘
CH2OH
오
영형
CH2OH
CH2 O
영형
영형
"-
C+
시간
시간
"-
시간
NaOH, H2O
영형
시간
오
CH2 O
CH2OH
오
영형
2
+
H3C
씨
염산
CH3
CH3
호
씨
오
CH3
2,2-디(4-히드록시페닐)프로판
비스페놀 A
98페놀-포름알데히드 수지(L. Backelund, 1909).
최초의 합성 고분자 물질.
오
N
+
NH4OH
오
20-150OC
NaOH, H2O
오
오
베이클라이트
오
N
호
호
오
99페녹사이드 이온의 카르복실화.
콜베-슈미트 반응.
오나
산화.
+
이산화탄소
Na2Cr2O7
쿠나
180OC, 5atm
영형
오
오
H2SO4, H2O
영형
오
확인
영형
오
+
이산화탄소
p-퀴논
250OC, 5기압
OH NaCrO
2
2 7
영형
H2SO4, H2O
요리하다
회복
오
오
H2, Ni, T, P
시클로헥사놀
100에폭시 수지
N
영형
영형
+
nCl
CH2
영형
에피클로로히드린
CH3
H2C
CH2CH2O
영형
씨
CH3
씨
O CH2 CH CH2 O
CH3
오
영형
CH3
N
CH2CH CH2
영형
탄성 소재
영형
영형
H2C
CH2CH CH2
채널 채널2
H2N CH2 CH2 NH CH2 CH2 NH2
CH2CH CH2
영형
고분자 사슬 가교, 고체 물질 형성
브롬화 부틸 얻기
이 작업에서 제조 방법이 설명된 부틸 브로마이드가 유기 합성에 사용됩니다.
) n-옥탄 합성의 경우:
2CH3CH2CH2CH2Br + 2Na CH3(CH2) 6CH3 + 2NaBr 2) 합성 고무 생산에서 촉매로 사용되는 부틴-1을 얻기 위해(아세틸렌과 포름알데히드의 축합): 브로모부탄 -> 부텐 -> 디브로모부탄 -> 부틴 n-부틸알코올의 성질 채널 3-CH 2-CH 2-CH 2-오 부틸알코올(n-butanol)은 1가알코올의 대표적인 물질이다. 퓨젤유 특유의 냄새가 나는 무색의 점성 액체. 유기 용제와 혼합 가능. 애플리케이션 부탄올이 사용됩니다. · 페인트 및 바니시 산업의 용제, 수지 및 가소제 생산 · 요소 및 멜라민-포름알데히드 수지의 개질제. · 가소제를 얻기 위해: 디부틸 프탈레이트, 트리부틸 포스페이트. · 부틸 아세테이트 및 부틸 아크릴레이트 및 글리콜과 에테르를 얻기 위해. · 많은 유기 화합물의 합성에서. 자동차 연료로 응용 필수는 아니지만 기존 연료와 혼합할 수 있습니다. 부탄올의 에너지는 가솔린에 가깝습니다. 부탄올은 연료 전지에서 수소 생산을 위한 공급원료로 사용할 수 있습니다. 2007년에 바이오부탄올은 영국에서 가솔린 첨가제로 판매되기 시작했습니다. 몰 질량 74.12g/mol 밀도 0.81g/cm 3 끓는 온도 117.4º 와 함께 물에 대한 용해도 7.9 g / 100 ml 굴절률 1.399 부탄올을 얻는 방법 1)HCo(CO)가 있는 상태에서 프로필렌으로부터 산화 합성 4120-160°С 및 20-35 MPa에서: 채널 3 -채널 =채널 2+ CO + H 2® 채널 3채널 2채널 2CHO + (CH 3)2CHCH =영형 채널 3(CH 2)3OH + (CH 3)2CHCH 2오 2)압력 하에서 한 단계의 프로필렌에서. 1.0-1.5 MPa(Reppe에 따름): 채널 3 -채널 =채널 2+ 3CO + 2H 2영형 채널 3(CH 2)3OH + (CH 3)2CHCH 2OH+2CO 2
)아세트알데히드에서 구리, 구리-크롬 또는 니켈 촉매에 수소화되는 아세탈돌 및 크로톤알데히드를 통해: 2채널 3조 채널 3CH(OH)CH 2조 채널 3채널 =쵸쵸 채널 3(CH 2)3오 )식품의 아세톤-부틸 발효. 원료; 생성된 생성물의 비율 - 아세톤: n-부탄올: 에탄올 = 3:6:1 부틸 브로마이드 속성 부틸 브로마이드(CH 3채널 2채널 2채널 2Br)은 무색의 점성 액체입니다. 물에 약간 녹고 에탄올, 아세톤, 에테르에 잘 녹습니다. 몰 질량 137.02 g/mol 밀도 1.299g/cm 3
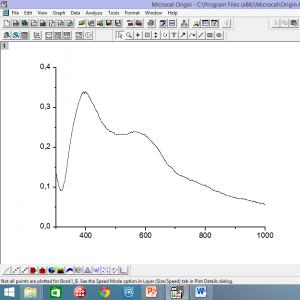
녹는점 -112.4 º 와 함께 끓는점 101.6 º 와 함께 굴절률 1.4398 접수방법 KBr + H 2그래서 4® HBr + KHSO 43채널 2채널 2채널 2OH+HBr ® 채널 3채널 2채널 2채널 2Br+H 2영형 부틸알코올 황산 브롬화물 반응 메커니즘은 친핵성 치환(S N 2)
3채널 2채널 2채널 2OH + KBr + H 2그래서 4® 채널 3채널 2채널 2채널 2Br+KHSO 4+ H 2영형 시약: n-부틸알코올 ........................................... 11.5ml(9g) 브롬화칼륨 ........................................... 18.5g 황산( ρ=1.84) ...........................................15 ml 염화칼슘 그릇 및 장비: 가열 맨틀, 둥근 바닥 플라스크, 환류 콘덴서, 깔때기, 수신기, 온도계. 합성 진행 히터, 둥근 바닥 플라스크 및 환류 콘덴서로 구성된 합성 설정을 조립합니다. 둥근바닥플라스크에 물 17.5ml를 붓고 브롬화칼륨 및 부틸알코올을 가하고 환류냉각기를 부착한다. 깔때기를 냉장고의 forshtos에 삽입하고 15ml의 진한 황산을 일정한 교반과 함께 소량(각각 2-3ml)으로 붓습니다. 플라스크에 보일러를 넣고 혼합물을 조심스럽게 약간 끓일 때까지 가열하여 1시간 동안 끓인 다음 환류 냉각기를 하강식 응축기로 교체하고(리빅 냉장고) 가열을 증가시키고 브롬화 부틸을 증류수로 물. 부틸 브로마이드의 오일 방울이 수신기 바닥으로 가라 앉지 않으면 증류가 완료된 것입니다. 리시버의 내용물을 분리 깔때기로 옮기고 바닥 층을 물에서 조심스럽게 분리하여 건조한 플라스크에 수집합니다. 미량의 물을 제거하기 위해 브롬화 부틸을 무수 염화칼슘으로 10-15분 동안 "배출"하고 주기적으로 콘을 흔듭니다. 액체가 투명해지면 건조 과정이 완료된 것으로 간주됩니다. 부틸 브로마이드를 증류 플라스크로 경사분리(가장자리 위로 배수)하여 염화칼슘의 고체 침전물에서 분리합니다. 단순증류장치는 미리 충분히 건조시킨다. 수신기의 무게가 측정됩니다. 부틸 브로마이드를 천천히 증류하여 98-103 범위에서 끓는 부분을 취합니다. º C. 얻은 제품의 부피를 결정하고 굴절률을 측정합니다. 설명서에 따라 종료 12.5 g. 실험 과정의 관찰. 브롬화칼륨과 n-부탄올을 황산과 반응시킨 후 혼합물은 두 개의 층으로 분리됩니다. 상부 유성층은 밝은 갈색이고 하부 유성층은 투명합니다. 오일 방울이 리시버 바닥으로 떨어지는 것을 멈출 때까지 증류를 수행했습니다. 건조되면 염화칼슘 조각이 크게 부풀어 오르며 결과 제품에 많은 양의 물이 있음을 나타냅니다. 증류하는 동안 생성물은 거의 투명해졌다. 생성된 생성물을 IR 스펙트럼으로 식별하였다. 스펙트럼을 기반으로 다음과 같은 결론이 내려졌습니다. · sp에는 강한 C-H 흡수 밴드가 있습니다. 3- 2900cm 영역의 하이브리드 상태 -1, 존재를 나타내는 - CH 2- 탄화수소 라디칼 · 1250cm의 흡수 밴드가 있습니다 -1, 알코올의 분자간 탈수 가능성으로 인해 원료에 존재할 수 있는 에테르 화합물 부류의 특성 · 1050 cm에서 중간 강도의 밴드 관찰 -1, 1차 알코올의 존재를 나타냅니다.