3.2. Парциальные давления в газовой смеси. Закон Дальтона
Газовая смесь находится в состоянии равновесия, если концентрации компонентов и её параметры состояния во всём объёме имеют одинаковые значения. При этом температура всех газов, входящих в смесь, одинакова и равна температуре смеси Т см.
В равновесном состоянии молекулы каждого газа рассеяны равномерно по всему объёму смеси, то есть имеют свою определённую концентрацию и, следовательно, своё давление р i , Па, которое называется парциальным . Оно определяется следующим образом.
Парциальное давление равно давлению данного компонента при условии, что он один занимает весь объём, предназначенный для смеси при температуре смеси Т см .
По закону английского химика и физика Дальтона, сформулированному в 1801 году, давление смеси идеальных газов р см равно сумме парциальных давлений её компонентов р i :
где n – число компонентов.
Выражение (2) также называется законом парциальных давлений.
3.3. Приведённый объём компонента газовой смеси. Закон Амага
По определению приведённым объёмом i -го компонента газовой смеси V i , м 3 , называется объём, который один этот компонент мог бы занимать при условии, что его давление и температура будут равны давлению и температуре всей газовой смеси.
Закон французского физика Амага, сформулированный примерно в 1870 году, гласит: сумма приведённых объёмов всех компонентов смеси равна объёму смеси V см :
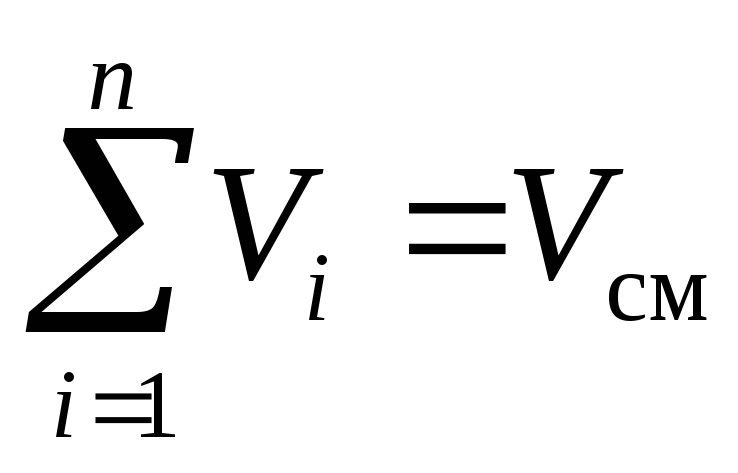 ,
м 3 . (3)
,
м 3 . (3)
3.4. Химический состав газовой смеси
Химический состав газовой смеси может задаваться тремя различными способами.
Рассмотрим газовую смесь, состоящую из n компонентов. Смесь занимает объём V см, м 3 , имеет массу М см, кг, давление р см, Па и температуру Т см, К. Также число молей смеси равно N см, моль. При этом масса одного i -го компонента m i , кг, а число молей этого компонента ν i , моль.
Очевидно, что:
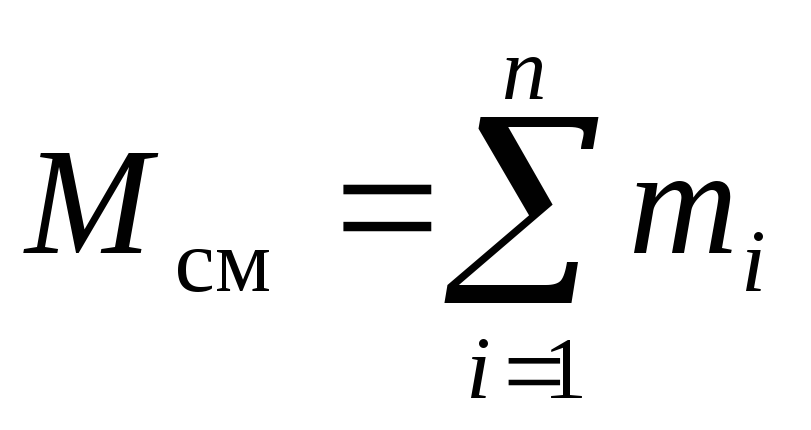 , (4)
, (4)
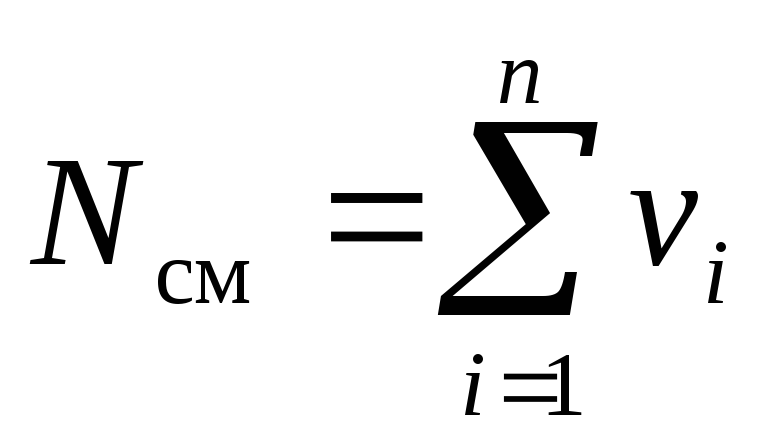 . (5)
. (5)
Используя для рассматриваемой смеси закон Дальтона (2) и Амага (3) можно записать:
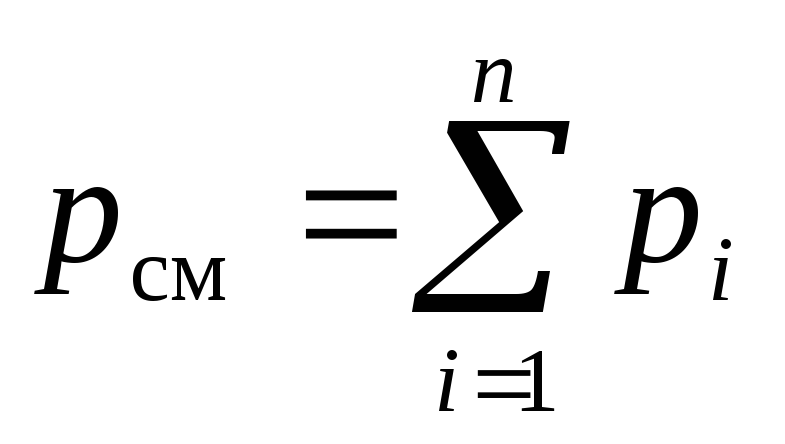 , (6)
, (6)
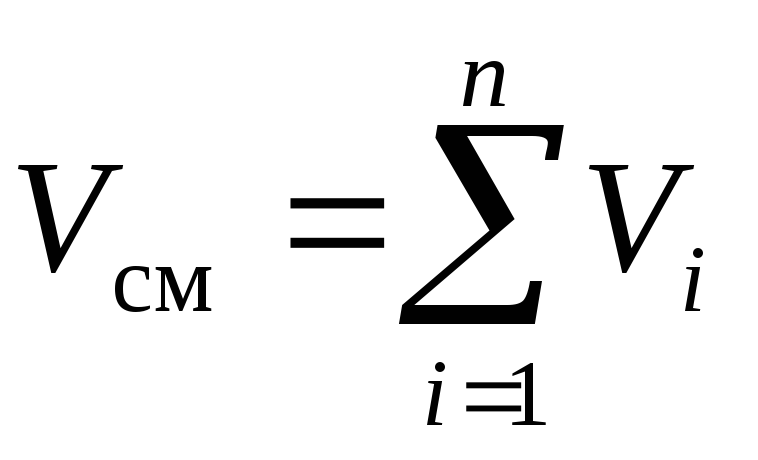 , (7)
, (7)
где р i – парциальное давление i -го компонента, Па; V i – приведённый объём i -го компонента, м 3 .
Однозначно химический состав газовой смеси может быть задан либо массовыми, либо мольными, либо объёмными долями её компонентов:
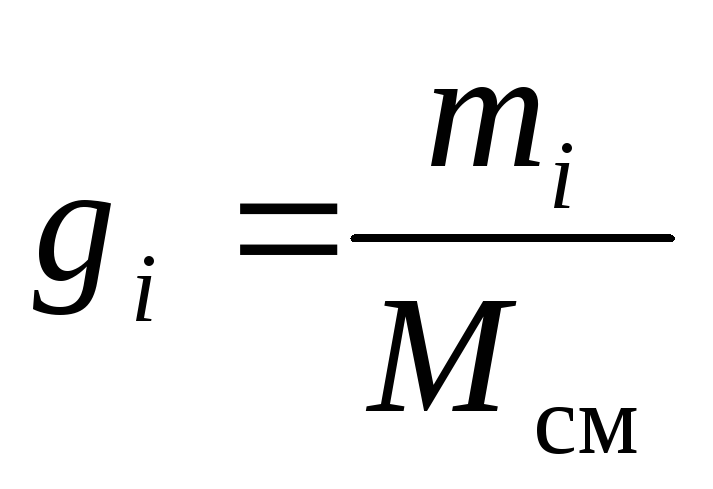 , (8)
, (8)
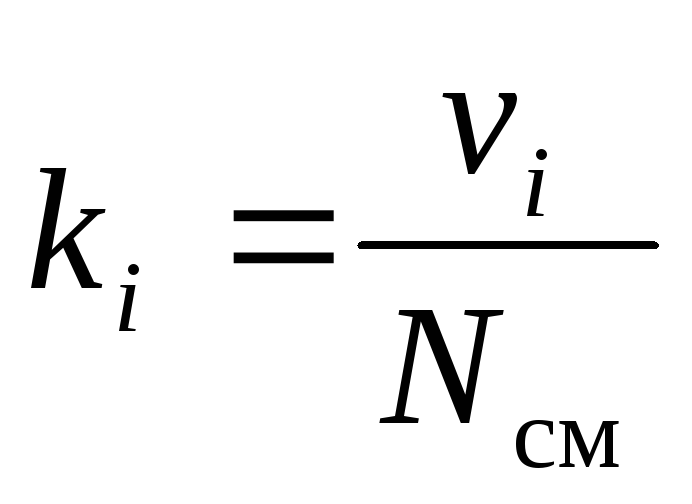 , (9)
, (9)
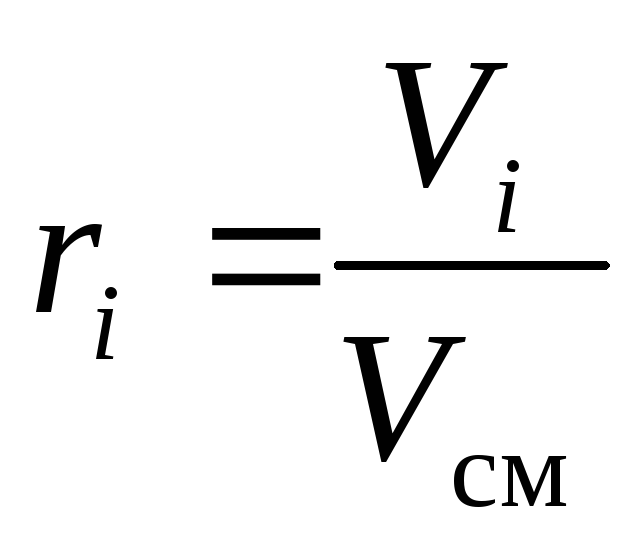 , (10)
, (10)
где g i , k i и r i – массовая, мольная и объёмная доли i -го компонента смеси соответственно (безразмерные величины).
Очевидно, что:
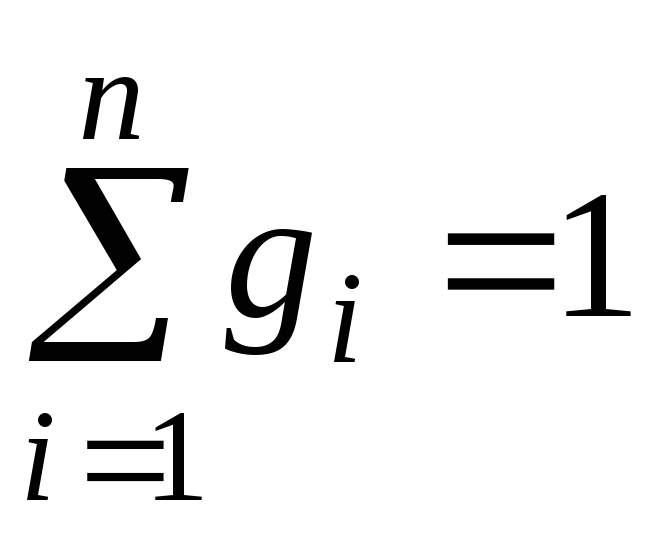 ,
,
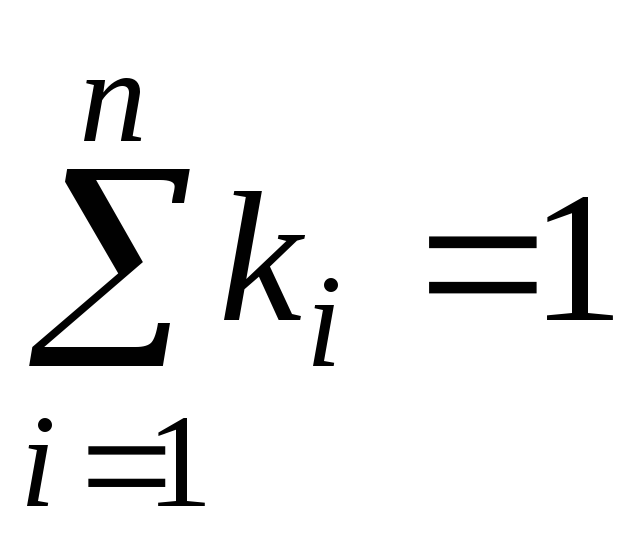 ,
,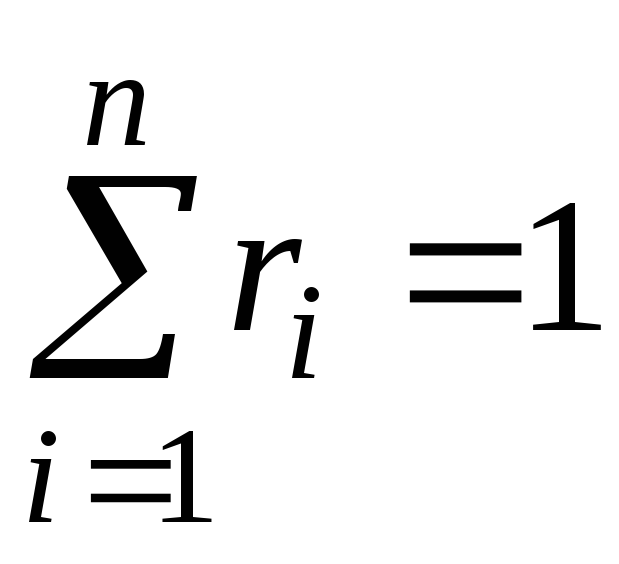 . (11)
. (11)
Часто на практике химический состав смеси задаётся не долями i -го компонента, а его процентами.
Например, в теплотехнике приближённо принимается, что сухой воздух состоит из 79 объёмных процентов азота и 21 объёмного процента кислорода.
Процент i -го компонента в смеси вычисляется путём умножения его доли на 100.
Для примера с сухим воздухом будем иметь:
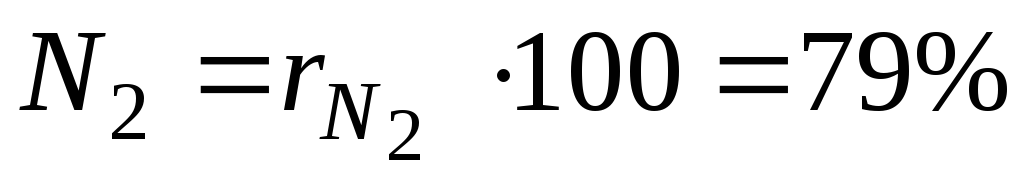 ,
,
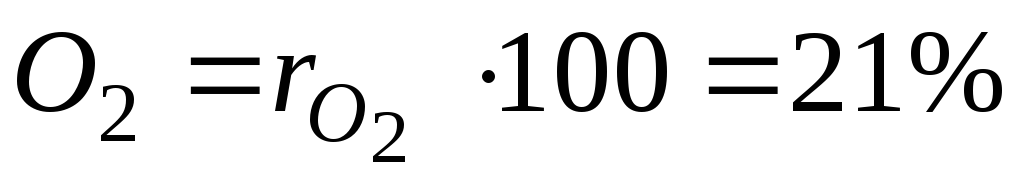 . (12)
. (12)
где
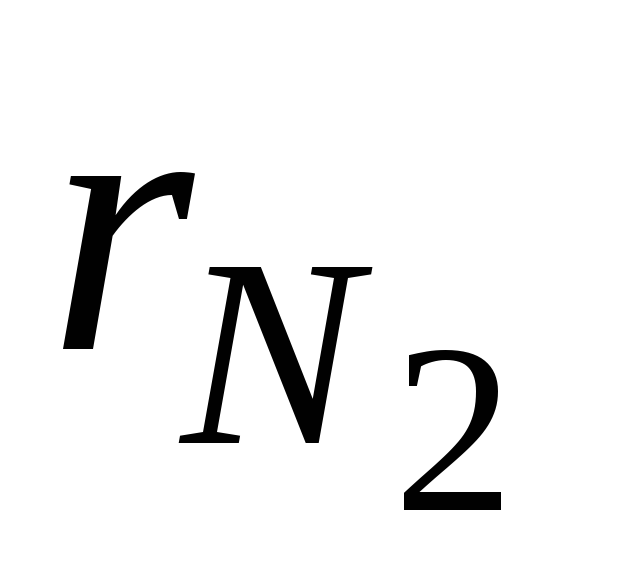 и
и
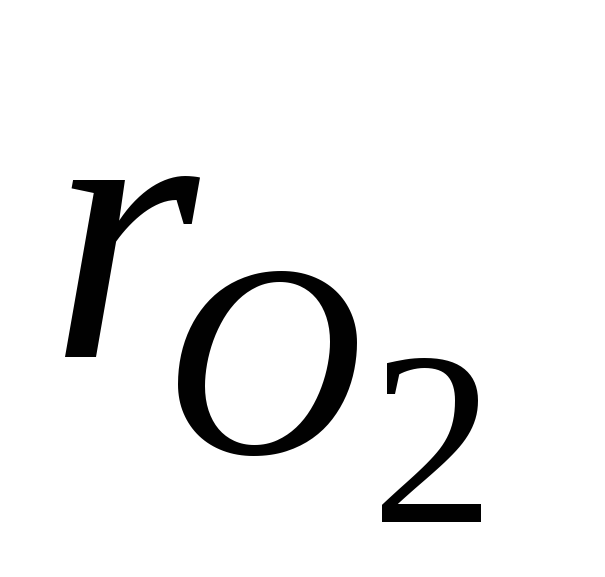 –
объёмные доли азота и кислорода в сухом
воздухе; N 2
и О 2
– обозначение объёмных процентов азота
и кислорода соответственно, % (об.).
–
объёмные доли азота и кислорода в сухом
воздухе; N 2
и О 2
– обозначение объёмных процентов азота
и кислорода соответственно, % (об.).
Примечание:
1) Мольные доли идеальной смеси численно равны объёмным долям: k i = r i . Докажем это.
Пользуясь определением объёмной доли (10) и законом Амага (3) можем записать:
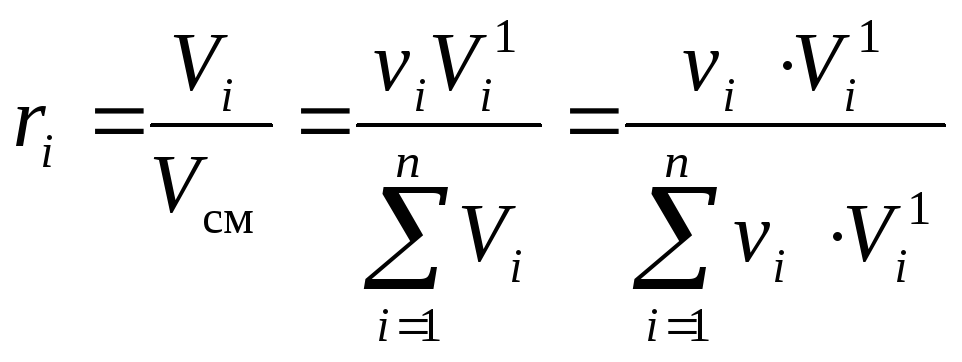 ,
(13)
,
(13)
где
V
i
– приведённый объём
i
-го
компонента, м
3
;
ν
i
– число молей
i
-го
компонента, моль;
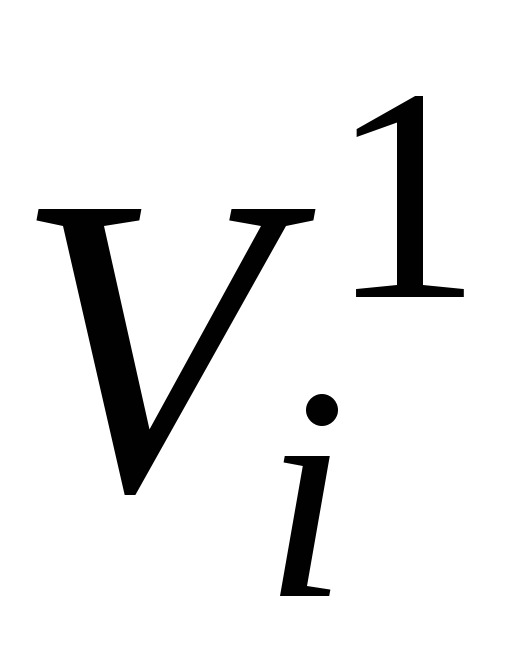 –
объём одного моля
i
-го
компонента при давлении смеси р
см
и температуре
смеси Т
см ,
м
3
/моль.
–
объём одного моля
i
-го
компонента при давлении смеси р
см
и температуре
смеси Т
см ,
м
3
/моль.
Из закона Авогадро (см. п. 2.3 данного приложения) следует, что при одинаковых температуре и давлении один моль любого газа (компонента смеси) занимает один и тот же объём. В частности, при Т см и р см это будет некоторый объём V 1 , м 3 .
Сказанное позволяет записать равенство:
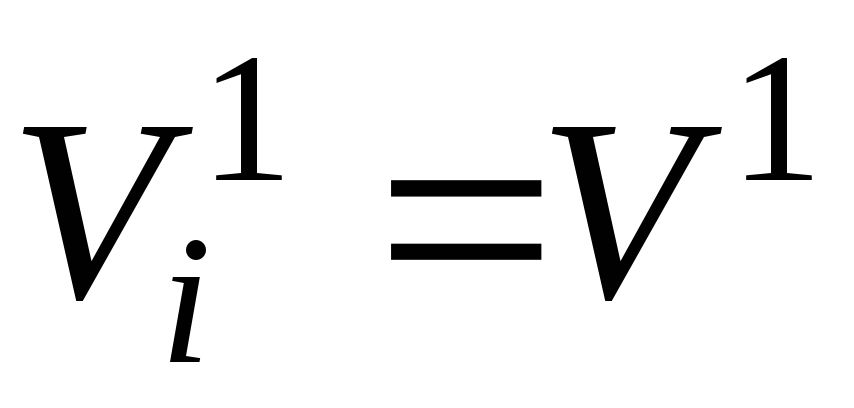 .
(14)
.
(14)
Подставляя (14) в (13) получаем требуемое:
![]() .
(15)
.
(15)
2) Объёмные доли компонентов газовой смеси можно рассчитать, зная их парциальные давления. Покажем это.
Рассмотрим i -ый компонент идеальной газовой смеси в двух различных состояниях: когда он находится при своём парциальном давлении р i ; когда он занимает свой приведённый объём V i .
Уравнение состояния идеального газа справедливо для любых его состояний, в частности, и для двух, названных выше.
В соответствии с этим, и учитывая определение удельного объёма, можем записать:
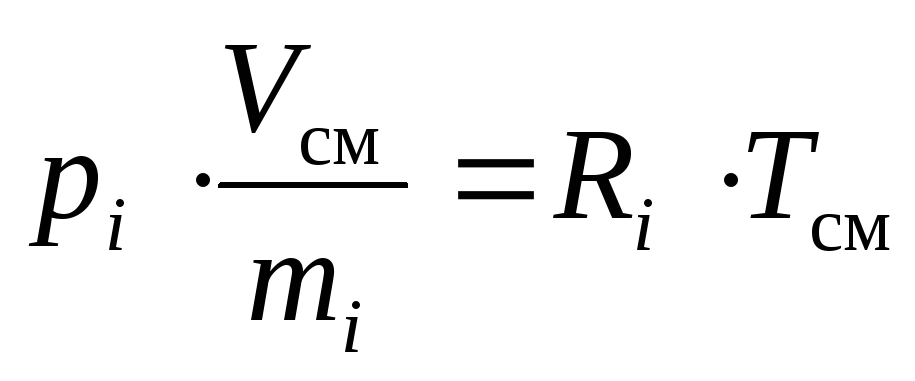 ,
(16)
,
(16)
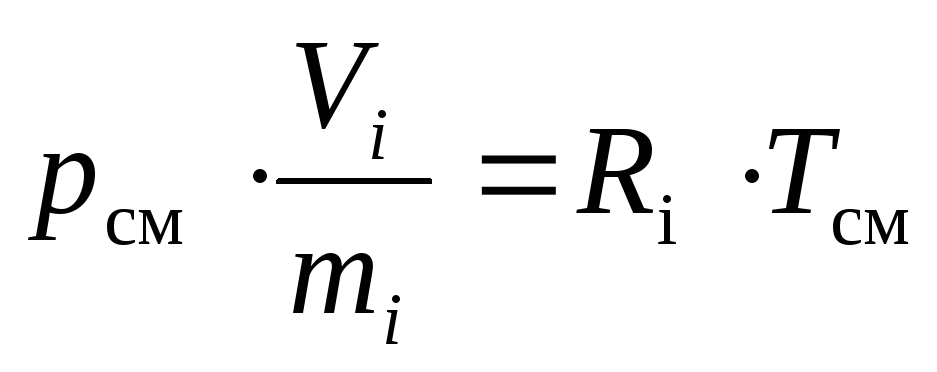 ,
(17)
,
(17)
где R i – газовая постоянная i -го компонента смеси, Дж/(кг·К).
После деления обоих частей (16) и (17) друг на друга получаем требуемое:
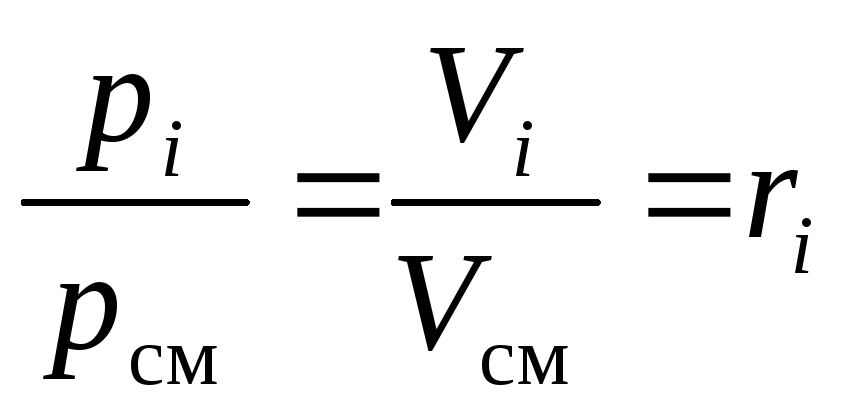 .
(18)
.
(18)
Из (18) видно, что парциальные давления компонентов смеси можно рассчитать по её химическому составу, при известном общем давлении смеси р см :
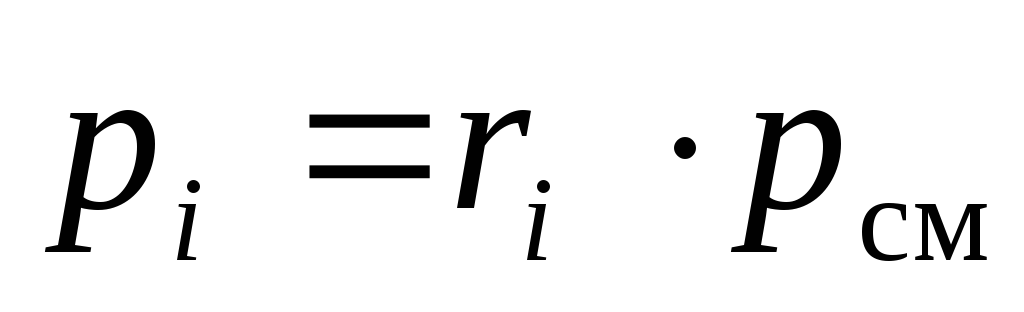 .
(19)
.
(19)